九年级化学科学探究
1.依据所给资料提出有探究价值的问题。★★★
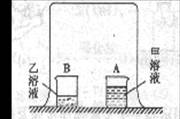 1.如图所示,在烧杯A中装入20mL无色甲溶液,在烧杯B中装入10mL无色乙溶液。用一只大烧杯把A、B两烧杯罩在一起。过几分钟,看到小烧杯A中装有的溶液变成红色。
1.如图所示,在烧杯A中装入20mL无色甲溶液,在烧杯B中装入10mL无色乙溶液。用一只大烧杯把A、B两烧杯罩在一起。过几分钟,看到小烧杯A中装有的溶液变成红色。
提出问题:上述现象说明了什么 。对上述现象看法不一,可能作出不同的假设。请你仔细阅读下表中的示例,然后填写表中空格。
| 提出假设 | 实验探究 | |
| 示例 | A烧杯中的溶液要过一会儿才变色,与B烧杯无关 | 用洁净烧杯配好20mL甲溶液。静置、观察现象;将其单独罩在烧杯里,观察现象 |
| (1) | 大烧杯壁上沾有某种物质,散发出的肉眼看不见的粒子与A烧杯中溶液接触,使其变红 | |
| (2) |
2.科学探究:铁、铜、银是初中化学课上学过的三种金属,实验设计如图所示。请回答:
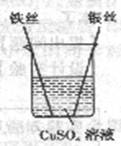 (1)猜想该实验在探究的问题是
(1)猜想该实验在探究的问题是
;
(2)所用的科学探究的方法是 ;
(3)观察到的实验现象是 ;
从而得出的实验结论为 。
2.对问题可能的答案作出猜想或假设,并作出论证。★★★
1.今天是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是 |
产生此气体的化学方程式可能是 ;
②我想制取该气体,采用的发生装置可选取图中的(填序号),收集装置是
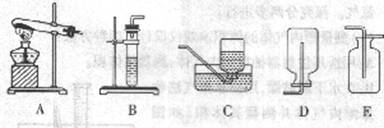
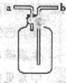 ③用如图装置收集该气体,气体由 端(填“a”或“b”)导入。
③用如图装置收集该气体,气体由 端(填“a”或“b”)导入。
(2)我猜想此无色气体还可能是另外一种气体,可以产生它的化学方程式是 。
2.已知过氧化钠加入水中能发生如下反应:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)检验过氧化氢的实验方法是: ,溶液中,发生的反应的化学方程式是: 。
(2)小华为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色。请你对此现象进行探究。(只要提出假设、方案,不需要说出方案实施的具体结果)
假设一:生成的过氧化氢使溶液褪色。
方案一:在稀氢氧化钠溶液中滴加酚酞试液,再滴加过氧化氢溶液,观察溶液颜色变化。
假设二: 。
方案二: 。
若还能提出新的合理的假设和方案。
假设: 。
方案: 。
3.小盈同学做硫在氧气中燃烧的实验前,预先在集气瓶底装有少量水。实验过程中她联想到老师介绍过二氧化硫排放到空气中会形成酸雨,于是想了解燃烧后集气瓶底部残留的“水”是否也呈酸性。她取“水”多次测其pH,发现其pH始终小于7并逐渐减小,直至稳定在pH=4,证明集气瓶底残留液呈 性。为了进一步了解该残留液的性质,请你与小盈同学一起探究:
【提出问题】残留液还能与哪些不同类别的物质反应呢?
【猜想】① ;
② ;
【设计方案】请你没计实验来验证你的一种猜想:
| 实验方法 | 可能观察到的现象 | 结论 |
3.从所给资料中获取信息。★★★
1.下表是生活中常见金属的部分性质。
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
该金属投入盐酸中,可以产生大量无色气体。根据上述信息回答以下问题:
(1)试推断金属可能的一种用途 ;
(2)该金属的活动性比铜 (填“强”或“弱”)
(3)请自选试剂,设计实验探究该金属与铁的活动性强弱,并完成下表:
| 你的一种猜想 | 验证方法 | 现象 | 结论 |
| 假设该金属比铁活泼 |
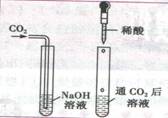
2.下表是空气中的气体成分和人体呼出的气体成分含量对照表:
| 气体成分 | 氮气 | 氧气 | 二氧化碳 | 水 | 其他气体 |
| 空气中的气体(%) | 78 | 21 | 0.03 | 0.07 | 0.9 |
| 呼出的气体(%) | 78 | 16 | 4 | 1.1 | 0.9 |
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入的气体成分的含量有什么不同,其主要操作步骤如图所示。
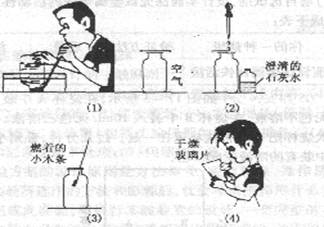
请依据图示将主要实验操作步骤及验证依据填入下表中:
| 实验步骤 | 验证依据 |
| (1) | |
| (2) | 根据 判断CO2含量不同 |
| (3) | 根据 判断O2含量不同 |
| (4) | 根据 判断水含量不同 |
 4.根据所要探究的问题设计简单的化学实验方案。★★★
4.根据所要探究的问题设计简单的化学实验方案。★★★
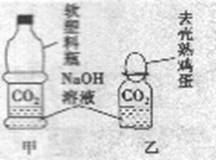
1.化学课上,老师将CO2分别通入澄清石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象。CO2和NaOH是否确实发生了化学反应?
(1) 我设计了甲、乙两个实验装置来验证,如图所示,实验现象为:甲―软塑料瓶变瘪,乙―“瓶吞鸡蛋”,小虎同学认为上述实验是可行的,其共同原理是 。
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是
。
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
|
| 实验步骤和方法 | 实验现象 | 实验结论 |
| 方案1 |
| C02和NaOH 确实发生了 化学反应 | |
| 方案2 |
写出方案2中所涉及的化学方程式
2.玲玲在使用“除垢净”去除热水瓶中的水垢时,发现有大量的气泡产生。联想水垢的主要成分是碳酸钙,玲玲猜想“除垢净”的成分中可能有酸。
(1)为证实自己的猜想,玲玲从家中又找来两类不同的物质中的进行实验。
实验一: ;
实验二: 。
经实验,小明得出“除垢净”的有效成分中一定有酸的结论。
(2)玲玲想试制一瓶“除垢净”,你认为HCl、H2SO4两种酸中 更合适,理由是 。
(3)结合上面对“除垢净”的了解,在使用“除垢净”时应注 。
3.某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案所用试剂如下,其中你认为不可行的是( )
A.Cu、Ag、FeSO4溶液 B.Fe、Ag、CuSO4溶液
C.Fe、Cu、稀盐酸、AgNO3,溶液 D.Cu、FeSO4溶液、AgNO3溶液
5.评价化学实验方案。★★★
1.高洁同学为确定实验室某一失去标签的液体物质,设计如下探究实验方案,其中你认为错误是( )
A.将液体倒入试管中观察其颜色
B.测量液体的密度
C.滴加紫色石蕊试液检测液体的酸碱性
D.用嘴尝尝液体是甜味还是酸味
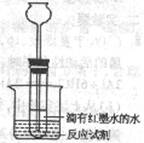 2.为了便于观察化学反应过程中放热、吸热的现象,某同学设计了如图所示装置(在烧杯内进行化学反应),有关此装置使用和评价的说法错误的是 ( )
2.为了便于观察化学反应过程中放热、吸热的现象,某同学设计了如图所示装置(在烧杯内进行化学反应),有关此装置使用和评价的说法错误的是 ( )
A.可以通过观察长颈漏斗内液面的变化,判断反应的放热或吸热
B.试管内的液体要浸没长颈漏斗的末端
C. 向试管内的水中滴加红墨水的目的是便于实验观察
D. 若直接在试管内加入锌粒和稀硫酸,通过观察长颈漏斗内液面的变化也可以判断反应的放热或吸热
3.下列实验方案可行的是 ( )
A.加足量稀盐酸,过滤,以除去铁粉中混有的铜粉
B.加适量稀盐酸,过滤,以除去氧化铁中混有的氧化铜
C.加适量稀盐酸,以除去氯化钠溶液中混有的氢氧化钠
D.将二氧化碳和一氧化碳的混合气体通过石灰水,以除去一氧化碳
6.分析实验现象和处理实验数据,得出结论。★★★
1.小超同学在探究铜、银、铝三种金属的活动性顺序时,有关实验记录如下:
2Al+6HCl=2AlCl3+3H2↑,Cu、Ag与盐酸不反应。
(1)从上述实验中,你得出的结论是
(2)请你补充一个实验探究铜、银的活动性顺序。
操作步骤 ,
现象 ,
结论 。
2.已知明矾的化学式为[K2SO4・Al2(SO4)3・24H2O]是农村常用的一种净水剂,它在水中离解出K+、Al3+和SO42-。甲同学为了探究明矾中哪种离子具有净水作用,进行了如下实验,请填写表中空白。
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加少量KCl,搅拌后静置 | 烧杯中的水仍然浑浊 | |
| 在一杯浑浊的水中加少量Al2(S04)3,搅拌后静置 | 烧杯中的水变澄清 | |
| 在一杯浑浊的水中加少量A1C13,搅拌后静置 | A1C13能净水 |
根据上述方程式答案你认为明矾中有静水作用的离子是 (写符号),乙同学看到甲的方案后,认为该方案不完善,他对甲同学的方案进行了补充完善。请你把乙同学补充方案中达到的目的和所使用的试剂填入下表。
| 实验目的 | 使用的试剂 |
7.反思探究过程,评价探究结果。★★★
1.在点燃蜡烛时,小红发现有一根烛芯沾有食盐的蜡烛比普通蜡烛燃烧的时间长一些。请
你与小红一起探究,并回答相关问题。
【提出问题】盐是否能延长蜡烛的燃烧时间。
【猜想】①一定量的食盐可延长蜡烛的燃烧时间;②其他盐也可以延长蜡烛的燃烧时问。
【实验探究】
实验一 探究不同量的食盐对蜡烛燃烧时间的影响
实验方案:取6支相同的蜡烛,在其中5支的烛芯周围分别放入不同量的食盐,另1支作对照实验,分别测定它们的燃烧时间。
实验结果:
| 食盐质量(g) | 0 | 0.1 | 0.5 | 0.7 | 0.9 | 1.0 |
| 燃烧时间(分钟) | 10 | 15 | 18 | 28 | 25 | 27 |
| 燃烧稳定性 | 正常 | 正常 | 正常 | 正常 | 易灭 | 极易灭 |
实验结论:从所得实验结果可初步分析出两点结论:
①
②
实验反思:
① 此实验方案还存在一些问题值得进一步研究,如(至少写出一点):
②你认为此实验结果有什么实际应用价值:
实验二 探究不同种类的盐对蜡烛燃烧时间的影响
要求:请参照实验一,设计实验方案和实验记录表格。
实验方案:
实验记录表格:(注意:使用到具体盐时。必须用它的化学式表示,否则不能得分。)
2.长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
进行猜想:甲同学认为:生成氧化钙和氧气;乙同学认为:生成氢氧化钙和氧气。
(1)你认为 同学的猜想是错误的,其理由是 。
(2)请设计一个实验方案来验证另一个同学的猜想是正确的,并填入下表空格中。
| 实验步骤及操作方法 | 预期的实验现象 | 结论 |
| 1.取少量过氧化钙放入试管中,加足量水, | 有氧气生成 | |
| 2. |
3.请你参与某学习小组的探究活动,并回答相关问题。
某化学兴趣小组的同学把氢氧化钠的片状固体放在表面皿中,离开实验室。三天后进行观察。
【发现问题】三天后片状固体粉末状固体变成白色粉末状固 体了。
【提出问题】“白色粉末状固体物质是什么?”
【设计实验】请你来完成以下实验,把相关内容填写在表格中。
| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
【反思与应用】我们学过的哪些物质还具有这样性质? ,
应该如何保存这些物质 。
8.准确表述探究过程和结果。★★★
1.为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验。实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。按图示连接好仪器装置,点燃蜡烛,同时从a导管口抽气。一段时问后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。实验数据如下表。
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
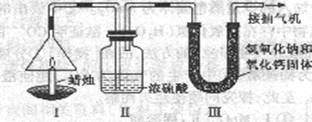 a
a
(1)该实验中测得水的质量为 g,二氧化碳的质量为 g。
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为 。
(3)装置Ⅱ和装置Ⅲ的顺序能否颠倒? (填“能”或“不能”)。
(4)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是
。
(5)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量? (填“能”或“不能”),理由是
。
2.将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”。请你协助课外活动小组的同学对“假黄金”进行探究,并回答有关问题:
【提出问题】“假黄金”的化学组成是什么?
【查阅资料】高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO3,高温可分解成金属氧化物。
【猜想】①“假黄金”可能由C、Zn、Cu三种单质组成;
②“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成;
③“假黄金”可能是单质和氧化物组成的混合物。
【论证】他们经思考和推理后,首先排除了猜想(选填①②或③),你觉得他们的理由是 。进而再排除了猜想 (选填①②或③)。对余下的一种猜想,该同学又排除了其中的一种物质,你认为他们的依据是 。
【进行实验】他们用实验鉴定了“假黄金”中所含的两种物质,请将实验过程填人下表中:
| 实验方法 | 观察到的现象 | |
| 步骤1 | ||
| 步骤2 |
【得出结论】“假黄金”的化学组成是 。
3.在学校的元旦联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小军很感兴趣,于是,他和同学们进行探究。
 【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
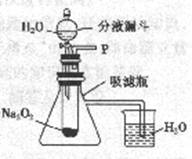
【设计装置】如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是 。
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生原因 。
实验二:继续探究反应后生成的另一种物质是什么?
小张猜想另一种物质是Na2CO3,小军认为不可能。小军的依据是 。
为了证明小军的看法,请你设计一个证明CO32-不存在的实验。
| 实验步骤 | 实验现象 | 实验结论 |
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈 性。
【表达】
由实验探究的结果,写出过氧化钠和水反应的化学方程式 。
5.几位同学对蜡烛燃烧火焰的焰心进行了以下探究,请你完成其中的步骤:
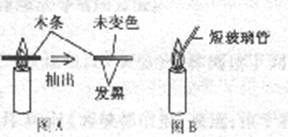
(1)点燃蜡烛,将一根小木条迅速平放入火焰中,约1s后取出,现象如图,这证明焰心 。
(2)向焰心斜向插入一支细短玻璃管,发现玻璃管中无明显现象如图,在玻璃管的上口点燃,上口产生火焰,这说明焰心物质的性质是 、 。
(3)猜想和验证
| 猜想 | 操作 | 现象 | 结论 |
| 假设①:焰心气体含CO2 | 在未点燃的短玻璃管上口 | 假设①不成立 | |
| 假设②:焰心气体含CO | 用表面烧黑的灼热铜丝迅速插入短玻璃管上口 | 烧黑的铜丝变成红色 | |
| 假设③:焰心气体含石蜡蒸气 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心 | 假设③不成立 | |
| 试用火焰点燃。取下长玻璃管,打开湿毛巾 |
 (4)若蜡烛的分子式用CxH4y,表示,则其燃烧的化学方程式为:
。
(4)若蜡烛的分子式用CxH4y,表示,则其燃烧的化学方程式为:
。