中考化学模拟考试集锦
班级 姓名
一、选择题
1.食盐、纯碱、食醋等均为家庭厨房中常用的物质,利用这些物质在家庭中你能完成的实验是:①检验鸡蛋壳能否溶于酸 ②除去热水瓶中的水垢 ③检验自来水中是否含有盐酸 ④鉴别食盐和纯碱 ⑤检验汽水中逸出的气体是二氧化碳……………( )
A、全部 B、③④⑤ C、①②③ D①②④
2.有一浓度为15%的氯化钾溶液,蒸发掉100g水后,溶液的浓度增大一倍,原溶液中溶质的质量是 ( )
A.15g B. 20g C .25g D. 30g
3.重要的文件资料需长期保存,比如同学们的毕业生登记表等,因此书写时应使用( )
A.铅笔 B .蓝墨水笔 C.碳素墨水笔 D. 圆珠笔
4.油.盐.酱.醋是家庭中常用的调味品,下列调味品与水充分混合后不能形成溶液的是( )
A..味精 B..酱油 C..黄酒 D..大豆油
5.科学家致力于CO2的“组合转化”技术研究,把过多的CO2转化为有益于人类的物质,如将CO2和H2混合在一定条件下以1:3(分子数比)比例发生反应,生成某种重要化工原料和水,该化工原料可能是……………………………………………………( )
A、CH4 B、C2H2 C、C2H4 D、C2H6
6.下列各组溶液不加任何其他试剂,就能通过实验鉴别的是( )
(A)CuSO4, BaCl2, KNO3 (B)NaOH, BaCl2, Mg(NO3)2
(C)Na2SO4, KOH, H2SO4 (D)K2CO3, HCl, H2SO4
7.欲用98%的浓硫酸(密度为1. 84g/ cm3) 和水配制100克10%的稀硫酸,下列仪器中不需使用的是( )
(A)10毫升量筒 (B)托盘天平 (C)100毫升量筒 (D)250毫升烧杯
8、由于易燃易爆而严禁携带上列车的是( )
A,矿泉水 B,液化石油气 C,食盐水 D,石灰水
9、防毒面具中用来去除有毒气体的物质是( )
A,炭黑 B,焦炭 C,活性炭 D,石墨
10.在一定温度下,将少量无水硫酸铜加入一定量饱和硫酸铜溶液中,保持温度不变,下列说法正确的是-----------------------------------------------------------------------------( )
A.溶质质量不变 B. 溶剂质量不变
C.溶液浓度不变 D.析出的晶体质量与加入的无水硫酸铜质量不变
11. 将一严重锈蚀而部分变成铜绿[Cu2(OH)2CO3]的铜块研磨成粉末,在空气中充分灼烧成氧化铜,发现固体质量在灼烧前后保持不变,则灼烧前粉末中铜元素的质量百分含量( )
A.52.8% B.80% C.50% D.48.3%
12. 常温下,取某种纯净的化合物10 g与90 g 水充分混合,所得溶液的质量百分比浓度将会( )
A、 小于10% B、大于10% C、等于10% D、 以上三种情况均可能
13、“绿色化学工艺”是消除污染的重要手段,其理想工艺是反应物里的原子全部转化到欲制取的物质中。下列化学反应类型一定属于“绿色工艺”的是…………………( )
A、置换反应 B、化合反应 C、分解反应 D、复分解反应
14、在初三的“科学”主题班会上,小明同学表演了下面的魔术:甲、乙、丙三个烧杯中均盛有无色液体,小明先将乙杯中的一半液体倒入甲杯中,液体立即变成红色。然后小明又将丙杯中的无色液体倒入乙杯剩下的液体中立即产生大量气泡。同学们经过讨论得出下列结论(甲、乙、丙三杯无色液体依次是)正确的是…………………………………( )
A、石蕊试液、氢氧化钠溶液、硫酸 B、硫酸、碳酸钠、酚酞试液
C、硫酸、酚酞、氢氧化钠溶液 D、酚酞试液、碳酸钠溶液、硫酸
15、将一块5克重的合金,投入足量的稀硫酸中,充分反应产生氢气0.2克,则合金的组成可能是………………………………………………………………………………( )
A、Al、Fe B、Cu、Zn C、Mg、Al D、Fe、Ag
16、将60℃的硫酸铜饱和溶液100克,冷却到20℃,下列说法正确的是……( )
A、溶液质量不变 B、溶剂的质量发生变化
C、溶液为饱和溶液,浓度不变 D、有晶体析出,溶剂质量不变
17.近来新闻媒体不断报道,我国频频发生小煤窑爆炸,造成重大的人员伤亡恶性事故,引起小煤窑爆炸的气体主要是…………………………………………………( )
A.CO B.CO2 C.H2 D. CH4
18.温室中的绿色植物受阳光的照射生长,下列表示温室中氧气昼夜含量的示意图中正确的是……………………………………………………………………………( )
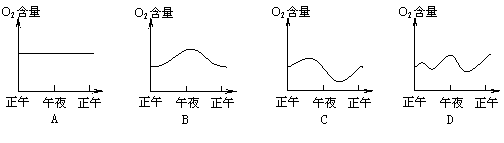 |
19.鲜蛋呼吸时会排出二氧化碳,下列物质中能在蛋壳表面形成难溶性固态保护膜,因而可作为鲜蛋保鲜剂的是…………………………………( )
A、食醋 B、食盐水 C、石灰水 D、纯碱
20.人的汗液有盐分,法医做指纹实验常用某溶液喷洒指纹,你认为应选用的试剂是…( )
A、NaCl 溶液 B、酒精 C、AgNO3 溶液 D、碘酒
21. 2003年2月1日,美国“哥伦比亚”号航天飞机在空中失事。有专家分析认为,其原因可能是航天飞机机壳底部的石墨瓦在空中脱落,击中机翼。航天飞机表面覆盖石墨瓦可以起隔热和保护作用,这主要是因为石墨 ……………………………………( )
A、能导电 B、密度小
C、熔点高、耐高温,化学性质稳定 D、硬度小,有润滑作用
22.某有机物在氧气中完全燃烧,生成二氧化碳和水的质量比为22:9,则该有机物可能是…………………………………………………………………………… ( )
①C6H12O6 ②C3H6 ③C2H2 ④C2H5OH
A.①② B.②③ C.①③ D.②④
23.欲将含有盐酸的氯化钙溶液中和至中型,得到氯化钙溶液,在没有指示剂的情况下,
应加入的试剂是……………………………………………………………………( )
A、氧化钙 B、氢氧化钙 C、石灰石 D、碳酸钠
24.在一个大萝卜上挖一大孔,向其中注入饱和食盐水,过一段时间后将食盐水倒出,在
相同的温度下发现倒出的溶液还可再溶解少量食盐,这说明倒出的溶液………( )
A、食盐的溶解度增大 B、食盐的溶解度减小 C、饱和溶液 D、不饱和溶液
25. 现有一瓶工业酒精和一瓶食盐水 , 区别它们的最简便的方法是……………( )
A. 闻气味 B. 品尝味道 C. 取少量点燃 D. 用硝酸银溶液检验
27.下列变化 , 只有加入酸才能一步实现的是………………………………………( )
A.Zn 一→ZnS04 B.CaC03 一→CO2 C.MgO 一→ +MgC12 D.BaCl2 一→BaS04
28.蚊子、蜂、蚂蚁等昆虫叮咬人后,会向人体注入一种叫蚁酸(甲酸)的物质,使皮肤红肿疼痛,要消除肿痛,可涂抹下列物质中的……………………………………( )
A.稀硫酸 B.氢氧化钠溶液 C.稀氨水或肥皂水 D.食用醋
二、填充题
1.写出下列物质的化学式: 铅笔笔芯不是铅而是 ;纯碱不是碱而是 。
2.下表是硝酸钾在某些温度的溶解度,将60℃时100g24%的硝酸钾溶液变成饱和溶液可以采用的方法是:加入硝酸钾 g;或降低温度到 ℃恰好饱和。
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
3.将铁粉和铜粉的混合物投入到硝酸银和硝酸锌的混合液中,充分反应后,过滤,在滤渣中滴入盐酸有气体产生,则滤渣中一定含有 ,滤液中一定含有 和水。
4.下图是一种显示事物异同点的信息处理方法,两个圆分别代表金刚石和石墨的有关信息,两圆重叠的区域表示金刚石和石墨的共同特征(相同点),重叠区域以外的部分表示它们的独有特征(不同点),请你在图下的空格内填写与B、C中的(1)(2)(3)区域对应的适当内容(每处只要求填一点)。
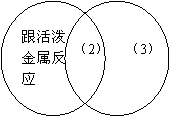


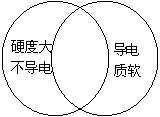
![]() 金刚石 石墨
氢气 一氧化碳
酸
碱
金刚石 石墨
氢气 一氧化碳
酸
碱
A B C
![]() (1)
(1)
![]() (2)
(2)
![]() (3)
(3)
5.在日常生活中我们常使用一些铝制器皿。在清洗表面的污垢时,不能使用热的碱性溶液,因为铝能跟碱性溶液中的氢氧化钠、水作用生成一种叫做偏铝酸钠(NaAlO2)的盐和一种可燃性单质气体。请写出该反应的化学方程式: 。
6.有一辆盛有浓硫酸的槽车,由于翻车而导致大量浓硫酸泼洒在路面上。为了减少硫酸对环境的危害,现有如下方法:①用大量的水冲洗路面;②从路基旁边取土将浓硫酸覆盖;③立即调用大量熟石灰覆盖。你赞成的方法是______,为什么?_______________________________________________
![]() 7.已知:化合物甲+单质乙 化合物丙+单质丁,试写出三个符合此表达式的化学方程式(要求:甲在三个化学方程式中所属类别不同)
7.已知:化合物甲+单质乙 化合物丙+单质丁,试写出三个符合此表达式的化学方程式(要求:甲在三个化学方程式中所属类别不同)
(1)_____________________________________________
(2)_____________________________________________
(3)_____________________________________________
8.一包氧化铜和锌粉组成的混合物,投入到一定量的稀盐酸溶液中,充分反应后,滤出不溶物,再向滤液中加入锌粉,产生气体。则滤出的不溶物是 ,滤液中一定含
有的溶质是 。
9.一氧化氮是一种难溶于水的无色气体,其密度与空气相似。它很容易与空气中的氧气化合,生成红棕色的NO2 。因此,实验室收集一氧化氮气体,除了用排水法之外,还可以用另外一种具体的收集方法:
。
三、简答题
1.2003年10月16日,神州五号载人飞船成功返航,标志着我国已跨入航天领域国际先进行列。(1)在宇宙飞船上要安装盛有Na2O2颗粒的装置,它的作用是与人呼出的二氧化碳反应生成氧气和碳酸钠,写出该反应的化学方程式: 。
(2)请你写出一种实验室制取氧气的化学反应方程式: 。
请在下面的仪器中根据上述反应选择适当的仪器组成一套制取并收集干燥的氧气的装置,各仪器从左到右的接口顺序是![]() 。(填各仪器接口处的字母)。(3)证明集气瓶中的氧气已经收集满的方法是
。
。(填各仪器接口处的字母)。(3)证明集气瓶中的氧气已经收集满的方法是
。
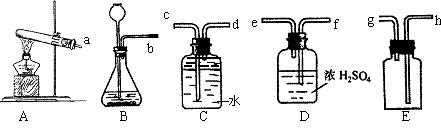
(4)要测定生成的氧气的体积,必须选用除上图以外的仪器是 (填仪器名称)。
2.某校学生对买来的工业固体烧碱的杂质成分进行研究(已知各组分都是钠元素的化合物)
(1)假设:该固体烧碱中可能含有碳酸钠、氯化钠。
(2)查阅资料:
①在化工生产中原料往往不能全部转化成产品
②在工业上用食盐和水配成饱和食盐水通过电解(通电)制得烧碱溶液,同时还得到氢气和氯气,再将溶液浓缩得到固体烧碱
(3)实验:请你帮助该同学完成下列实验报告
| 实验步骤 | 实验现象 | 结论或化学方程式 |
| 1.取样,加足量的水, | 固体完全溶解 | |
| 2.用试管取上述试液,加入过量稀硝酸,塞上带导管的单孔塞;将导管的另一端插入 中。 | 有 生成, 有 。 | 证明原固体烧碱中含有碳酸钠 |
| 3.向试管中再加入 。 | 有 生成。 | 写出该反应的化学方程式为: |
(4)结论:根据实验报告得出:原假设能成立。
(5)试写出工业上用电解饱和食盐水制烧碱的化学方程式 。
3.某校化学兴趣小组承担了某项研究课题的一部分:通过实验探究气体X(已知由两种元素组成)的元素组成。实验装置如下。将0.17gX气体由注射器A缓缓送入B装置(B装置中的空气已预先除去),使之完全反应,生成的气体全部用D装置抽取收集。实验的现象和数据记录如下:
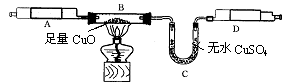
| 现 象 | 反应前质量(g) | 反应后质量(g) | |
| B装置中 | 逐渐变成亮红色 | 21.32 | 21.08 |
| C装置中 | 变蓝色 | 32.16 | 32.43 |
(1)参加反应的氧元素的质量是 g,X中一定有 元素。
| 气 体 | H2 | O2 | CO | CH4 | N2 | CO2 |
| 常温常压时的密度(g/L) | 0.09 | 1.43 | 1.25 | 0.72 | 1.25 | 1.98 |
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25g/L,试推测该气体的化学式是 ,其质量是 g。
(3)写出B装置中发生反应的化学方程式 。
4.小刚和小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究。请填写以下探究过程中的空格:
提出假设: (1)化学反应中,反应物的总质量与生成物的总质量 。
确定研究方法: 分析推理、查阅资料、实验探究。
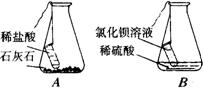 设计并进行实验:小刚设计的实验装置和选用药品如A图所示,小洁设计的实验装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、
准确的称量和细致的观察。
设计并进行实验:小刚设计的实验装置和选用药品如A图所示,小洁设计的实验装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、
准确的称量和细致的观察。
实验结论: 小刚认为:在化学反应中,生成物
的总质量与反应物的总质量不相等。
小洁认为:在化学反应中,生成物的总质量与反
应物的总质量相等.
(2)你认为 的结论正确.请说出导致另一种结论错误的原因 。
结论分析: (3)请从原子的角度,简要分析你认为正确的结论 。
查阅资料:小刚和小洁通过查阅材料了解到:法国伟大的科学家拉瓦锡,早在18世纪就 围绕这个问题进行了准确、缜密的研究,并做出了科学结论。
结论应用: (4)环保部门常用I2O5,测定空气受CO污染的程度,发生反应的化学方程式为I2O5+5CO=I2+5X,根据生成X的多少,可判断CO的含量,X的化学式是 。
5. 化学是一门以实验研究为基础的自然科学。通过对大量实验事实的分析,得出一些规律,并总结规律和物质本身的内在联系,在此基础上对一些物质的性质作出推测。这是化学学习必需的思想方法,你有这方面的体验吗?请仿照示例的思维过程,以学过的酸、碱、盐、金属的化学性质为例,填写下表(所填规律不能重复):
| 实验事实(每空至少举两例) | 规 律 | 推测同类物质具有的相同性质 |
| 示例:NaOH、KOH溶液都能使无色酚酞变红 | 碱溶液能使无色酚酞变红 | Ca(OH)2溶液也能使无色酚酞变红 |
| a. Na2CO3、CaCO3与HCl溶液反应都能生成能使澄清石灰水变浑浊的气体 | ||
| b. |
6.某校研究性学习小组的同学查阅化学史料时发现:
早在300多年前,英国化学家波义耳在一个敞口的容器中加热一种金属,结果发现反应后质量增加了,由此得出反应前后质量不守恒。之后,俄国化学家罗蒙诺索夫在密封玻璃瓶内燃烧金属,发现反应后质量不变,由此得出反应前后质量守恒。这两位科学家的实验相似,为何结论不同?该学习小组的同学沿着科学家的足迹进行实验探究,请你完成以下相关内容:
(1)交流实验:两科学家得出的结论究竟与哪些实验因素有关呢?
(2)提出假设:若用同种金属、同一容器进行实验,两位科学家得出的不同结论主
要是由于 的缘故。
(3)实验验证:
已知钠在空气中受热燃烧生成氧化钠固体。
| 操作步骤与实验现象 | 简 答 |
| ①在底部铺有细沙的锥形瓶中,放入一小块金属钠,塞紧橡皮塞,称量,用砝码使天平平衡。 | 称量前需 。 |
| ②取下锥形瓶,放在垫有石棉网的三脚架上微热、观察到金属钠着火燃烧,冷却后,再称量。 | 称量时观察到 。 |
| ③将锥形瓶塞取出一会儿,盖上瓶塞,再称量。 | 称量时观察到 。 |
(4)得出结论:假设成立。
(5)依据以上实验事实,解释两位科学家的实验结论:
。
 7、利用下列仪器和装置,用排水法收集30ml人呼出的气体。试回答下列问题:
7、利用下列仪器和装置,用排水法收集30ml人呼出的气体。试回答下列问题:
(1)连接的顺序用字母表示为a接 , 接d,导管插入量筒中。
(2)实验结束时,应该在量筒里收集到30ml水,估计从嘴里呼出的气体的体积
(填“大于”、“小于”或“等于”)30ml,并分析其原因
。
(3)在实验中,Ⅱ中的水不一定要先装满(想一想为什么?)。如果利用装置Ⅱ进行排水集气法收集一瓶氧气,Ⅱ中的水一定要先装满吗? 。
(4)说说装置Ⅱ(试剂可以自选)的其他用途(至少写出一种用途) 。
四、计算题
1.含有不溶性杂质的粗盐12.0克,放入适量水中,氯化钠全部溶解。过滤后,恰好得到20℃时的NaCl的饱和溶液44.2克。往上述氯化钠饱和溶液中加入足量的硝酸银溶液,充分反应后生成白色沉淀。将沉淀过滤、烘干、冷却后称量,所得质量为28.7克。求:
(1)粗盐中氯化钠的百分含量; (2)20℃时NaCl的溶解度。
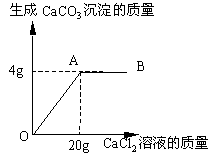 2.碳酸钠和氯化钠的混合物14g,常温溶解在足量水中,向溶液中逐滴加入氯化钙溶液。加入氯化钙溶液的质量与生成的CaCO3沉淀的质量的关系如图
2.碳酸钠和氯化钠的混合物14g,常温溶解在足量水中,向溶液中逐滴加入氯化钙溶液。加入氯化钙溶液的质量与生成的CaCO3沉淀的质量的关系如图
(1)图象中表示恰好完全反应的点是 ;
(2)求原混合物中氯化钠的质量分数。(精确到0.01%)
3.加热氯酸钾和二氧化锰的混合物15克,使其完全反应。在一定温度下,向残留固体中加入4克水,有9.24克固体未溶解,再加入2克水,仍有8.28克固体未溶解,且剩余固体为混合物。
求:(1)生成氧气的质量。
(2)此温度下,氯化钾的溶解度。
(3)原混合物中氯酸钾的质量。(精确到0.1)
4.把4g硫粉在给定质量的氧气中燃烧,有关实验数据如下表所示:
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
请回答下列问题:
(1)第1次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是 。
(2)请你通过计算求出第2次实验生成二氧化硫多少克?
(3)在表中填写第3次实验生成二氧化硫的质量。
5.将20g CaCl2和CaC03 的固体混合物放入到 65.9g 水中充分溶解, 并加入 21.2%5Og 的Na2CO3溶液, 恰好完全反应。
(1) 写出与 Na2C03 溶液发生的化学反应方程式 ;
(2) 求原固体混合物中 CaCl2 的质量 ;
(3) 求生成溶液的质量 ;
(4) 若将生成的溶液蒸发, 得到t℃的饱和溶液 , 此时的溶解度为 36g/100g 水 , 求需蒸发掉多少克水 ?