中考初三化学模拟试题
姓名 班级 得分
[可能用到的相对原子量质量:H-1 O-16 C-12 Na-23 Mg-24 Ca-40 Cl-35.5
S-32 Fe-56 Zn-65 Ag-108]
第Ⅰ卷(选择题 共40分)
一、 选择题:(以下各题,只有一个符合要求的答案)每题1分,共15分
⒈ 下列变化属于物理变化的是
A、煤的干馏 B、树叶杂草发酵制沼气C、石油的分馏D、用煤焦油提炼成分制医药
2.下列物质中,不能由金属与酸反应直接制得的是
A、 ZnCl2 B、 FeCl3 C、 MgSO4 D、 AlCl3
3.分别盛有浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分蒸发),则两瓶溶液
A、质量都变小了 B、溶质的质量分数都变大了
C、体积变小了 D、溶质的质量分数都变小了
4.下列化学方程式正确的是
A、 2Fe+3H2SO4==Fe2(SO4)3+3H2 ↑ B、 AgNO3+HCl==AgCl ↓ +HNO3
C、 Zn+2HNO3==Zn(NO3)2+H2 ↑ D、 Fe2O3+6HCl==2FeCl2+3H2O
5.固体氢氧化钠必须密封保存的原因是
① 氢氧化钠有毒 ②氢氧化钠有腐蚀性 ③氢氧化钠易吸收水分而潮解
④ 氢氧化钠有挥发性 ⑤氢氧化钠能与空气中的二氧化碳反应
A 、 ①② B、 ②③④ C、 ②③⑤ D、 ③⑤
6.判断复分解反应能否发生,可以不必考虑的是
A、 生成物中是否有沉淀 B、 生成物中是否有水
C、 生成物中是否有气体 D、 金属的活动性顺序
7.将铁片投入下列溶液中,反应完毕后溶液的质量减少的是
A、 稀HCl B、 稀H2SO4 C、 CuSO4 D、 FeSO4
8.正常雨水与酸雨的差异是
A、正常雨水显中性,酸雨显酸性
B、正常雨水的PH值约为5.6,酸雨的小于5.6
C、正常雨水不含杂质,酸雨含杂质 D、 正常雨水降在农村,酸雨降在城市
9.下列实验操作后,溶液温度升高的是
① 浓硫酸倒入水中 ② NaOH固体溶于水中 ③ 生石灰放入水中
④ 浓盐酸滴入浓烧碱中 ⑤NaCl晶体溶解于水中 ⑥NH4NO3晶体溶解于水中
A、只有①②③ B、有①②③④
C、 只有①②③④⑤ D、有①②③④⑤⑥
10.下列各组物质中,属于同一种物质的是
A、 食盐、食碱、NaCl B、生石灰、熟石灰、CaO
C、 石灰石、消石灰、Ca(OH)2 D、火碱、烧碱、NaOH
11.下列四种物质中,在一定条件下能与其他三种物质都能发生反应的是
A、 CuSO4 B、 CO2 C、 NaOH D、 HNO3
12.在化学实验中必须注意安全操作:
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌
③浓硫酸不慎滴到皮肤上,应立即用大量水冲洗,再用3-5%的NaHCO3溶液涂上
④给试管中液体加热,液体一般不超过试管容积的1/3
⑤称量任何固体药品时,均要在天平的左右托盘上放等大的相同的纸片
上述说法中错误的是:
A.③④ B.②④ C.①②③④ D.③⑤
13.做镘头的面团发酵过度会变酸,要除去酸味,可在面团中加入
A、 NaOH B、 NaCl C、 CaCO3 D、 Na2CO3
14. 实验表明,用碱性溶液浸泡新鲜的蔬菜,能有效除去蔬菜上的残留农药,从而降低对人体的损害。根据上述原理,对刚买回来的蔬菜,你认为应浸泡在哪种溶液中
A.白酒 B.食醋 C.烧碱溶液 D.碳酸钠溶液
15、下列四种盐溶液中一般不与其他物质发生复分解反应的是
A、KNO3 B、NaOH C、HCl D、CuSO4
二、选择题:以下个体,只有一个符合要求的答案。(每题2分,共10分)
16、1999年报道:爆炸性的高能N5+阳离子(中子数为7)被美国加州爱德华空军基地空军研究室研究的高能材料的化学家Karl O. Christe与他的同事W.W Wilson合成。关于N5+的说法正确的是:
A.该微粒中的质子数为34
B.该微粒的电子数是34
C.该微粒由5个氮分子构成
D.它是一种由5个氮原子构成的单质分子
17我国研制的大型激光器“神光二号”用了磷酸二氢钾(KH2PO4)大晶体。下列说法正确的是
A.磷酸二氢钾也可用作复合肥料 B.磷酸二氢钾是一种氧化物
C.磷酸二氢钾中含有氢气 D.磷酸二氢钾中磷元素为十4价
18、下面是某同学对有关火星探测资料的分析,其中结论错误的是
| 火星探测的有关资料 | 结 论 | |
| A | 火星南、北两极的极冠温度常年在一70~C至一140~C之间 | 那里很难找到液态水 |
| B | 在火星南、北两极发现“干冰” | “干冰”是固态二氧化碳 |
| C | 火星大气中存在甲烷气体 | 甲烷属于有机化合物 |
| D | 在火星上发现了大量盐的晶体 | 盐就是氯化钠 |
19、.在由C02和O2组成的混合气体中,测知碳元素的质量分数为20%,则混合气体中C02和02的质量比为
A.2∶1 B.1∶2 C.11∶4 D.11∶7
20、La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3,难溶于水,而LaCl3、La(NO3)3都易溶于水。下列各组物质中,不能直接反应制得LaCl3的是
A、La+HCl B、La2O3+HCl C、La(OH)3+HCl D、BaCl2+ La(NO3)3
三、 选择题(以下各题,有一个或二个符合要求的答案。选错、多选不给分。有二个答案的,只选一个且正确,给2分)每题3分,本题共20分
21、若将一瓶浓盐酸和一瓶浓硫酸都敞口放置在空气中,则可以肯定他们
A、质量都增大 B、溶质的质量分数都减小
C、溶液的酸性都增强 D、溶液的PH都增大
22、 现有铁、稀盐酸、氧化铁、氯化钡溶液、氢氧化钠溶液、氯化铜溶液等6种物质,在常温下两两相互组合,能发生的化学反应的种类共有
A、4种 B、5种 C、6种 D、7种
23、对于化学反应:A + B → C + D,下列说法中错误的是
A、若生成物C和D分别是盐和水,则反应物一定是酸和碱
B、 若A和C是单质,B和D是化合物,则反应一定是置换反应
C、若是可溶性碱,B是可溶性盐,则C、D可能是两种沉淀
D、 若A、B各取10克混合,使其充分反应,则C、D质量总和一定等于20克
34、下列场所中,宜贴上“严禁烟火”标语的是
A、加油站 B、面粉加工厂 C、石灰窑 D、炼铁厂
35、现有烧杯、试管、量筒、铁架台、铁夹、酒精灯、集气瓶、玻璃片、水槽、玻璃导管、胶皮导管、单孔橡皮管、药匙十三种实验仪器,用这些仪器不能进行下列实验的是
A、配制100克20%的氢氧化钠溶液 B、氢气还原氧化铜
C、制取氧气 D、粗盐的提纯
姓名 得分
选择题答案:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
| 题号 | 11 | 12 | 13 | 14 | 15 |
|
|
|
|
|
| 答案 |
|
|
|
|
|
|
|
|
|
|
| 题号 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(非选择题,共60分)
21.(10分)按要求写出下列反应的化学方程式:
⑴氢氧化钠和稀硫酸反应
⑵双氧水和二氧化锰混合制氧气
⑶铁丝燃烧
⑷铁与硝酸银的反应
上述反应中,属于复分解反应的是 ,属于置换反应的是 (填序号)。
22.(5分)有下列物质:(1)高锰酸钾(2)碳酸钠(3)氯化钠(4)硫酸铜(5)氢氧化钙(6)氢氧化钠,请按下列要求将正确答案的化学式填在空白处:
(1) 在空气中易潮解且可用作干燥剂的是_____________ _______
(2) 在日常生活中可用于调味、防腐的是_______________ ______
(3) 在日常生活中可用于洗涤的是_____________________ ______
(4) 可用来配制农药波尔多液的是______________ ____________
(5) 可用于消毒的是
23、(4分)从硫、氧、氢、钠四种元素中,选择适当的元素组成可能得到的物质,按下列要求填写化学式:
(1) 碱性氧化物____ _______;酸性氧化物_____ _______;
(2) 碱_______ _____________;含氧酸________ _
24、(方程式为2分,共8分)将一枚生锈(主要成分为Fe2O3)的铁钉放入稀盐酸中,可观察到① _______ ② 该反应的化学方程式可表示为_____________ 反应一段时间,又可观察到① _________________ ② ,该反应的化学方程式为_____________ 。
25、(3分)现有三种溶液:A为硝酸盐、 B为碱、C为钠盐。三者之间存在下列关系:
(1)A、B两溶液混合,产生红褐色的沉淀:
(2)B、C两溶液混合,产生难溶于稀硝酸的白色沉淀。根据实验判断三种溶液中溶质的化学式分别为
A、_______ _____B、__________________C、__________________
26.(2分)美国PPG公司生产的“自净玻璃”的神奇之处全在于它穿上40纳米厚的二氧化钛(TiO2)“纳米膜外套”。其“纳米膜外套”可与太阳光线中的紫外线作用,分解落在玻璃上的有机物,使有机物化为乌有;还能使玻璃表面的雨点或雾气变成一个薄层而使玻璃表面湿润,并洗掉表面的脏物。工业上二氧化钛可用下列方法制得: 2FeTiO3+7Cl2+3C=2X+2FeCl3+3CO2 , X+O2=TiO2+2Cl2 ,
则X的化学式为 。
27.(4分)痕检是公安机关提取犯罪嫌疑人指纹的一种重要方法,硝酸银显现法就是其中的一种:人的手上有汗迹,用手动用白纸后,手指纹线就留在纸上。如果将硝酸银溶液小心地涂到纸上,硝酸银溶液就跟汗迹中的氯化钠作用,生成氯化银,其反应的化学方程式是 。氯化银在光照条件下分解生成银粒和另一种单质,其反应的化学方程式是 。银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由灰褐色逐渐变成黑色,从而显现出黑色的指纹线。
28、(9分)某小组的同学在课外进行科学探究,以验证铜片在空气中灼烧后,表面生
成的黑色物质确实是铜与氧化合生成的CuO,他们进行了以下实验:
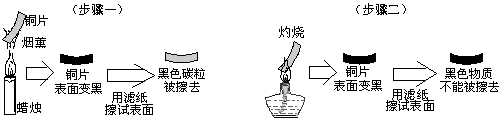 |
(1)由上图两个实验步骤判断:灼烧后铜片表面的黑色物质不是 。
 (2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:
(2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:
A B C
a.甲同学向A装置中通入纯净的H2,为检验反应产物,A的右边应连接上面的装置 (填番号),所选装置中的实验现象为 。
b.乙同学向A装置中通入纯净的CO,为检验反应产物,A的右边应连接上面的装置 (填番号),所选装置中的实验现象为 ;
此方法仅用上述装置进行实验有明显的缺陷,要弥补这个缺陷,应采取的措施是:
。
c.通入的气体如果含有少量水蒸汽,则应在A装置左边连接一个 装置。
(3)结论 :经过甲、乙两同学的实验现象证明,
。
(4)如果甲同学要用数据证明(3)的结论,你认为还应补充的实验操作是:
。
29、(方程式2分,共7分)某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究。
实验一:探究碳酸氢钠的化学性质
(1) 取样品溶于适量的水中,测得溶液的pH大于7。
(2) 向小苏打样品中滴加盐酸,有大量气泡产生,经检验该气体是二氧化碳。该反应的化学方程式为 。
(3) 向小苏打的溶液中加入澄清石灰水,生成了白色沉淀。
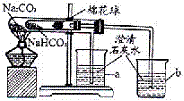 (4)同学们通过查阅资料,在老师的指导下采用了右图所示装置对小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊。(提示:无水硫酸铜遇水变蓝色)试回答:
(4)同学们通过查阅资料,在老师的指导下采用了右图所示装置对小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊。(提示:无水硫酸铜遇水变蓝色)试回答:
① 在实验结束时,操作上要注意的问题是: 。
② 由实验(4)可以得出的结论是 。
请归纳出小苏打的化学性质(至少三点)(1) 。
(2) 。(3) 。
计算题:(30题3分,31题5分,共计8分)
30.25g石灰石跟适量的盐酸混合,充分反应后(杂质不与酸反应),反应后混合物质量
减小了8.8g,求石灰石中碳酸钙的质量分数。
31.将20g不纯的氯化镁样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,得到溶质质量分数为10%的溶液234g。求:
(1)样品中氯化镁的质量;
(2)加入的氢氧化钠溶液中溶质的质量分数。