初中升学化学考试试卷(课改实验区使用)
化学部分
一、选择题(本大题共10分,每小题2分。每小题只有一个正确答案)
1.下列变化在生活中常发生,其中属于化学变化的是
A.酒精挥发 B.瓷器破碎 C.煤气燃烧 D.冰块融化
2.为了防止患甲状腺肿大病,市售食盐中常添加一定量的
A.葡萄糖 B.碘酸钾 C.碳酸钠 D.氯化钾
3.某矿泉水标签上印有的主要矿物质成分及含量如下(单位为mg/L):Ca~20、K~3、Zn~
0.06、F~0.02等。这里的Ca、K、Zn、F是指
A.原子 B.分子
C.单质 D.元素
4.为了增强市民的环保意识,变废为宝,2004年5月初,贵阳市将中山路、神奇路上的垃圾箱全部更换为分类回收垃圾箱。此次摆放的垃圾箱分类标志明显,绿色箱用来装可再利用垃圾,黄色箱用来装不可再利用垃圾。以下物质应扔进黄色垃圾箱的是
A.废旧报纸 B.果皮 C.铝制饮料罐 D.废旧电
5.根据你的生活经验判断,下列做法不正确的是
A.用燃着的火柴检查煤气炉是否漏气
B.做馒头时在发酵的面团中加入少许纯碱
C.切完菜后将菜刀洗净擦干,放在干燥的地方
D.用食盐腌制鱼、肉,以延长鱼、肉食品的保存期
二、填空题(本大题共14分,每空2分)
6.一些食物的近似pH如下表:
| 食物 | 苹果 | 葡萄 | 牛奶 | 玉米粥 |
| pH | 2.9―3.3 | 3.5―4.5 | 6.3―6.6 | 6.8―8.0 |
请回答下列问题:
(1)苹果汁和葡萄汁相比较,酸性较强的是 ,它能使紫色石蕊试液变成 色,
(2)人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用上述食物中的 。在
医疗上,治疗胃酸过多的药物之一是碳酸氢钠,其俗称为 ,请写出它与胃酸中盐酸反应的化学方程式 。
7.某班同学进行“使用塑料的利与弊”的辩论。甲方认为“利大于弊”,理由是:大部分塑料的抗腐蚀能力强,不与酸或碱反应等;乙方认为“弊大于利”,理由是:回收利用废弃塑料时,分类十分困难,而且经济上不合算等。你愿意加入 方(填“甲”或“乙”),并写出另一条理由 。
三、简答题(本大题共10分,每空2分)
8.某化学探究小组的同学从实验废液中回收铜,得到的铜样品中含有少量的铁粉。为测定样品中铜的质量分数,同学们按下述两种方案分别进行实验。
方案一:铜样品![]() 过滤,将得到的固体洗涤、干燥,称量
过滤,将得到的固体洗涤、干燥,称量
方案二:铜样品![]() 过滤,将得到的固体洗涤、干燥,称量
过滤,将得到的固体洗涤、干燥,称量
(1)请写出两个方案中发生反应的化学方程式 。
(2)方案一中反应进行完毕时的现象是 。
(3)用上述两种方案进行实验都 (填“能”或“不能”)测得样品中铜的质量分数,理由是 。
四、实验探究题(本大题共18分,每空2分)
9.据报道,从2005年1月1日起,贵州省各地环保部门将对实验室类污染实施严格的环境监管。
由于学校化学实验室要排放成分复杂的污染物,所以也被列为环境监管范围。某校化学兴趣小
组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体
对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体
与溶液的接触面积,使反应充分进行)。
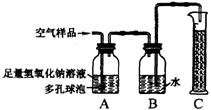 |
请回答下列问题:
(1)实验在没有受污染的乙实验室中进行,取出适量甲实验室中空气样品的方法是
。
(2)将取得的空气样品按上图所示的装置进行实验测定:装置A的作用是,其中发生反应的化学方程式为 。装置B中的现象是 ;装置C的作用是 。
(3)若通入空气样品100mL,实验结束后,量筒中液体的体积为99mL(导管内液体忽略不计),说明装置 中吸收了1mL气体。若这些气体大量排放到空气中,因产生
,会对环境造成不利影响。
(4)请写出你在做化学实验时,减少实验对环境污染的一种做法 。
十一、计算题(本大题共8分,每空2分)
10.实验室配制300g质量分数为10%的氢氧化钠溶液,需氢氧化钠 g,水 g。
11.将一定量的石灰石放人烧杯中,加入100g稀酸恰好完全反应(杂质不溶解,也不参加反应),此时,烧杯中物质的总质量比反应前减少了8.8g,则石灰石中碳酸钙的质量为 g,
所用盐酸的溶质质量分数为 。
参考答案
1.C 2.B 3.D 4.B 5.A
6.(1)苹果汁;红
(2)玉米粥;小苏打;Na2HCO3+HCl=NaCl+CO2↑+H2O
7.甲或乙;甲方理由:塑料的制造成本较低,而且耐用、防水(或容易被塑制成不同形状、良好的绝缘体等);乙方理由;塑料容易燃烧,燃烧时产生有毒气体(或塑料是由石油炼制的产品制成的,石油资源是有限的等)
8.(1)Fe+2HCl=FeCl2+H2↑; Fe+CuSO4=FeSO4+Cu
(2)溶液中无气泡产生 (3)不能;反应前没有对样品进行称量
35.(1)用注射器抽取(或用集气瓶装满水后在室内将水倒出,擦干,瓶口向上,盖上玻璃片、使用气囊收集等)
(2)吸收气体样品中的二氧化碳和二氧化硫;
2NaOH+CO2=Na2CO3+H2O; 2NaOH+SO2=Na2SO3+H2O
水沿着导管进人C中(或水位下降);测量二氧化碳和二氧化硫被吸收后剩余气体的粗略体积
(3)A;酸雨和温室效应
(4)控制实验药品用量(或对污染物进行处理后再排放、不乱倒废液和乱扔废物等)
36.30; 270
37.20;14.6%