化学方程式测试
一、填空题
1.用化学用语表示:
①氮气____________ ②水银____________ ③三个铝离子____________
④硝酸根离子____________ ⑤负二价的硫____________
⑥氯化亚铁____________
2.书写下列方程式,并说明其反应类型:
(1)电解水制取氢气:________________________________________________(
)
(2)氢气还原氧化铜:________________________________________________(
)
(3)细铁丝在氧气中燃烧:____________________________________________(
)
(4)氧化汞受热分解:________________________________________________(
)
3.测定白磷燃烧前后质量的变化情况来验证质量守恒定律的实验,试回答:
(1)白磷燃烧时,观察的现象是________________________________________________。
(2)左盘锥形瓶口在微热前后均要用瓶塞塞紧,为什么?简要回答___________________
_____________________________________________________。
(3)微热时,若不盖上瓶塞,待燃烧完毕后再盖上瓶塞,对测定结果的影响是____________
____________________________________________________________。
4.发射通讯卫星的火箭用联氨(化学式为N2H4)作燃料,用N2O4作氧化剂,燃烧后生成氮气和水,写出联氨和N2O4反应的反应方程式____________________________________。
5.某化合物在纯氧气中燃烧生成CO2和SO2,两者的质量之比为11∶32,该化合物中一定含有____和____________两种元素,若此化合物是一种无色、易挥发的液体,且1个分子中含有3个原子,则此化合物的化学式为________________________。此化合物在纯氧气中燃烧的化学方程式为________________________。
二、选择题
1.在化学反应中,发生改变的是( )
A.元素的种类 B.原子的个数
C.分子的组成 D.反应前后各物质的质量总和
2.现将A、B两种物质各10g混合加热,A完全反应,生成8g C和4g D,则参加反应的A与B的质量比是( )
A.1∶1 B.2∶1 C.4∶1 D.5∶1
3.下列说法中,错误的是( )
A.高锰酸钾受热分解后,剩余固体的质量比原反应物的质量减少3。
B.镁条在空气中燃烧,生成物的质量比原来镁条的质量大。
C.通电分解水的质量等于生成氢气和氧气的质量之和。
D.水结冰后质量没有改变,由此说明化学变化符合质量守恒定律。
4.Cu可以和浓HNO3反应,化学方程式为Cu+4HNO3=Cu(NO3)2 + 2H2O
+2X↑,其中X的化学式为( )
A.N2O3 B.N2
C.NO D.NO2
5.磷在氧气中燃烧后,生成物的质量A与反应物的质量B的关系是( )
A.A=B B.A>B C.A≤B D.A≥B
6.已知反应3A+2B = 2C+D,A、B两物质完全反应时的质量比为3∶4,若生成C和D,共140g则该反应消耗B的质量为( )
A.60g B.80g C.90g D.120g
7.加热高锰酸钾制氧气,生成氧气的质量占高锰酸钾中氧元素的质量分数为( )
A.10% B.25% C.30% D.20%
8.金属单质A跟盐酸反应生成+3价金属氯化物和mg氢气,这时A的质量减少了ng,则A原子的相对原子的质量是( )
A. B. C. D.
9. 将20g H2、O2、N2的混合气体点燃,完全反应后生成18gH2O,则剩余的气体不可能是(
)
A.H2和N2 B.O2和N2 C.H2、O2和N2 D.2g N2
10.4. 6g某有机物完全燃烧时需消耗9. 6g氧气,生成8. 8g二氧化碳和5. 4gH2O,该有机物中( )
A.只含碳、氢两种元素 B.只含碳元素
C.含有碳、氢、氧三种元素 D.可能含氧
三、计算题
用氢气还原12. 4g含有铜粉的氧化铜,充分反应后得到固体11.
6g,求原混和物中铜粉和氧化铜各多少克。
四、研究性学习
石蜡是一种常见的物质,请设计实验方案,证明石蜡中含有氢元素和碳元素。
一、填空题
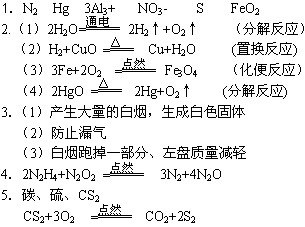
二、选择题
1. C 2. D 3. D 4. D 5. A 6. B 7. B 8. C 9. C 10. C
三、计算题:CuO :4g Cu:8. 4g
四、答:将石蜡点燃,用一干燥小烧杯罩在火焰上,烧杯壁出现水雾,立即将烧杯翻转,倒入澄清石灰水振荡,则变浑浊,即可证明(其它方法证明也可以)