初中化学复习测试题一
说明:1,允许使用CZ1206型计算器。
2,可能使用到的相对原子质量:Ar(H)=1 Ar(C)=12 Ar(O)16 Ar(Fe)=56
Ar(F)=19 Ar(Ca)=40 Ar(Cu)=64 Ar(Cl)﹦35.5
一、选择题(本题有20小题,共40分)
下列各小题只有1个选项符合题意,将它的代号填入括号中。
1.日常生活中发生的变化都属于化学变化的一组是---------------------( )
A.玻璃杯摔碎,米饭变馊 B.酒精挥发,湿衣服晾干
C. 蜡烛燃烧, 乒乓球变瘪 D.菜刀生锈,牛奶变酸
2.常温常压下不适宜用物理性质区别的一组物质是-----------------------( )
A.汞和铝 B.二氧化锰和氧化铜 C.酒精和醋 D.硫和红磷
3.下列仪器,可在酒精灯火焰上直接加热的是----------------------------( )
A.烧杯 B.锥形瓶 C.集气瓶 D.蒸发皿
4.下列关于四种基本反应类型的说法中,正确的是------------------------( )
A.有单质生成的反应一定是置换反应
B.复分解反应中一定有沉淀生成
C.化合反应中可能有元素化合价发生变化
D.由两种物质反应生成盐和水,该反应一定是中和反应
5.下列各组物质中,前者属于混合物,后者属于化合物的是----------------( )
A.食盐,碘酒 B.胆矾,糖水 C.冰水,干冰 D.空气, 氧化镁
6.油炸食物不宜多吃,因为食物长时间煎炸后所产生的微量的丙烯醛(化学式C3H4O )
等有毒物质,会损害人体 健康.下列有关丙烯醛的说法不正确的是--------( )
A. 由碳氢氧三种元素组成
B. 碳,氢,氧三种元素的质量比是9∶1∶2
C. 分子中原子个数比依次为3∶4∶1
D. 在空气中完全燃烧的产物是二氧化碳和水
7.下列说法中,正确的是----------------------------------------------( )
A.在空气中不燃烧的物质,在氧气里也一定不燃烧
B.钢铁生锈,白磷自燃都是缓慢氧化的结果
C.不使用催化剂,双氧水就不能分解
D. 催化剂只能加快化学反应速度
8.下列有关溶液的说法中,正确的是 ------------------------------( )
A.降低饱和溶液的温度都会有晶体析出
B.各种物质的饱和溶液都是浓溶液
C.同温下同种物质的饱和溶液一定比它的不饱和溶液浓
D.溶液中溶质的质量一定小于溶剂的质量
9.对于化学反应xA﹢yB=mC﹢nD下列说法中正确的是---------------------( )
A.x与y之和一定等于m与n之和
B.若反应前A和B各10克,反应后生成C和D的质量和为20克
C.若A和D为单质,B和C为化合物,则该反应为置换反应
D.C和D不可能同时为氧化物。
10.现用CO气体还原1.6克Fe2O3粉,问实际实验过程中需要CO气体多少克-( )
A.小于8.4克 B.等于8.4克 C大于8.4克 D.无法确定
11.下列关于气体收集的实验操作正确的是----------------------------( )
A.把集气瓶正放在实验桌上,用排气法收集氢气
B.把集气瓶倒放在实验桌上,用排气法收集二氧化碳
C.用排水法集满氧气后,先熄灭酒精灯,后撤导气管
D.用排水法收集氢气时,导管不好伸到集气瓶底部
12.分别将盛有浓硫酸和浓盐酸的两个试剂瓶敞口放在空气中一段时间后--( )
A.溶液质量都变小
B.溶质的质量分数都变大
C.溶液的体积都变小
D.溶质的质量都变小
13.只用一种试剂就能鉴别氢氧化钠溶液,石灰水,稀硫酸的是----------( )
A.氯化钠溶液 B。紫色石蕊试液 C.碳酸钠溶液 D.酚酞试液
14.下列物质不属于糖类的是-----------------------------------------( )
A.葡萄糖 B.淀粉 C.油脂 D.纤维素
15.大多数不粘锅的内壁上涂有一层聚四乙烯的涂层,其化学式可以表示为
(CF2CF2)n(n为正整数).下列关于聚四乙烯的说法错误的是------------( )
A. 该物质是一种遇热不稳定的有机物
B. 该物质具有耐高温的性能
C. 该物质含氟的质量分数为76%
D. 该物质是一种化学稳定性很强的物质
16.下列四种金属中,有一种金属的盐溶液能与其它三种金属发生置换反应
则该金属是---------------------------------------------------( )
A.Fe B.Ag C.Zn D.Cu
17.下列材料中,属于合成材料的是-----------------------------------( )
A青铜器 B.陶瓷 C.有机玻璃 D.铜筋混凝土
18.下列关于酸碱盐的说法中,不正确的是-----------------------------( )
A.酸中一定含有氢元素
B.碱中一定含有氧元素
C.盐中一定含有金属元素
D.酸碱盐中一定都含有非金属元素
19.第28届国际地质大会提供的资料显示,海底蕴藏着大量的天然气水合物,俗称
“可燃冰”. “可燃冰”是一种晶体,晶体中平均每46个水分子构建成8个笼,
每个笼内可容纳1个CH4分子或者1个游离的水分子.若晶体中每8个笼有6个容纳了CH4分子,另外2个笼被游离的水分子填充.则“可燃冰”的平均组成可表示成
--------------------------------------------------------------( )
A.3CH4·H2O B. CH4·3 H2O C. CH4·6 H2O D.CH4·8H2O
20.除去下列物质中的杂质(括号内为杂质)所选用的试剂不正确的―――( )
A.FeCl2(CuCl2):Fe 粉
B.NaCL(NaOH) :稀HCL
C.CO(CO2) :NaOH溶液
D.NaOH(Na2CO3):稀H2SO4
第二卷(非选择题 共60分)
二.(本大题共3小题,共19分)
21.物质的性质决定了物质的用途,物质的用途体现了物质的性质,请你据此完成下列
填空:(5分)
(1) 双氧水制氧气过程中,通常加入二氧化锰反应过程中,二氧化锰做
剂
(2) 煤气可做燃料,是因为煤气中的一氧化碳具有 性
(3) 氢氧化钙能用来改良酸性土壤,是因为氢氧化钙具有 性
(4) 在做电解水实验时,通常往水中加入少量的稀硫酸,这是为了增强水的
性
(5) 在使用酸碱时都应十分小心,防止酸碱沾到衣服上或皮肤上,是因为酸碱都有 性.
22.请写出下列反应的化学方程式,并填写反应类型(共10分)
(1)用高锰酸钾制氧气
(2)白磷在空气中自燃
(3)往硫酸铜溶液中滴加氢氧化钠溶液
(4)用稀盐酸来清洗钢材表面的铁锈
其中属于化合反应的是 (填序号下同),其中属于复分解反应的是
23.大棚种植蔬菜在冬季补充二氧化碳.某同学在自家大棚内设计了补充二氧化碳的方法:将工业废硫酸用水稀释后,盛放在塑料桶内,悬于高处,每天向通内加适量的碳酸
氢铵,它和硫酸反应生成硫酸铵和二氧化碳和水.(4分)
(1) 正确写出反应的化学方程式:
(2) 将塑料桶放在高处的原因是:
(3) 反应后生成的硫酸铵在农村还可作:
三.(本大题共3小题,共 17 分)
24.在实验室用15mL氢氧化钠溶液和稀盐酸进行中和反应实验.回答下列问题;
(1)完成该实验必须使用的仪器是__________________________________
(2)要判断氢氧化钠恰好被盐酸中和,需要加入_________________试剂
观察到的现象是_______________________________________
(4) 要从中和后的溶液中获取氯化钠晶体,应进行的操作是:
______________(共4分)
25.阅读下面材料,回答下列问题:(7分)
自从非典型肺炎在我国出现以来,过氧乙酸作为高效消毒剂被广泛使用.过氧乙酸
在常温下是一种无色有刺激性气味的液体,易挥发,易溶于水和醋酸.它对呼吸道粘
膜有刺激性,高含量的过氧乙酸溶液对皮肤有腐蚀性.一般商品过氧乙酸是40%的醋酸溶液,使用前通常用水将其稀释,消毒时可用喷雾法消毒,也可将其配成0.2%
的水溶液来洗手消毒.过氧乙酸不稳定,易分解生成无毒的物质,若用喷雾法消毒,过
氧乙酸在半小时内就可完全分解.
(1) 在过氧乙酸的质量分数为40%的醋酸溶液中,溶质是________,溶剂是_________
(2) 分别指出过氧乙酸的一条物理性质和一条化学性质
物理性质:
化学性质:
(3)100克0.2%的过氧乙酸洗手液中含过氧乙酸_________________克
(4)不慎让高含量的过氧乙酸溶液沾到皮肤上,应该怎么样处理?
(5) 根据过氧乙酸的性质,用过氧乙酸喷雾消毒过的房间,人若要进入,应该注意什么?
26.饲养观赏鱼,可以陶冶人的情操,增加人们对生活的热爱。空运观赏鱼,必须密封。
为了解决鱼的吸氧问题,可在水中加入过氧化钙(化学式为CaO2 ),过氧化钙与水
反应,生成氢氧化钙和氧气。(1)写出过氧化钙与水反应的化学方程式:
.(2)一位养鱼爱好者欲测定所用过氧化钙样品中过氧化钙的质量分数,做了如下实验:称取样品2克,加入到足量的水中,生成了224mL氧气(氧气的密度为1.43g/L).计算所用样品中过氧化钙的质量分数?(共6分)
四.(本题共 3 小题,共 17 分)
27.有机物中有许多物质具有共性如:在有机物里有一大类物质叫烷烃。其中CH4为甲烷,C2H6为乙烷,C3H8为丙烷, C4H10为丁烷………在有机物里有一大类物质叫醇。其中甲醇的化学式为CH3OH, 乙醇的化学式为C2H5OH,丙醇的化学式为C3H7OH,丁醇的化学式为 C4H9OH………已知实验室里用无水醋酸钠(固体)和氢氧化钠(固体)在加热条件下制取甲烷气体,又已知甲烷极难溶于水,且密度比空气小。根据内容回答下列问题:(共5分)
(1)有机物名称中的“甲、乙、丙、丁”与其分子中的什么有关?
(2)根据文中的意思,写出有8个碳原子的烷烃的化学式为 写出n个
碳原子的醇类物质的化学式
(3)从下列图中选出实验室制取甲烷的发生装置(填字母,下同)
收集装置
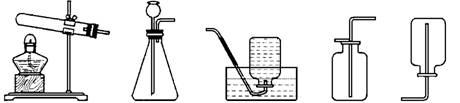
A B C D E
28.钛(Ti)因为有许多神奇的性能而越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时,却可与许多常见非金属单质反应,钛是航空,宇航、军工,电力等方面的必需原料,地壳中含钛矿石之一称金红石(TiO2),目前大规模生产钛的方法是:(共6分)
第一步:金红石,炭粉混合在高温条件下通入氯气制得TiCl4和一氧化碳,写出该反应的
化学方程式:
第二步:在隔绝空气的情况下,用过量的镁在加热条件下与TiCl4反应制得金属钛和氯气。
(1) 写出该反应的化学方程式:
(2) 如何由上述所得产物中分离出纯净的金属钛?写出方法和主要的实验步骤。
29.某样品为铜和氧化铜的混合物,为测定该样品中氧化铜的含量,取用20g此样品分四次向其中加入稀盐酸与之充分反应。每次所用盐酸的体积与反应后剩余固体的质量见下表:
| 第次 | 加入稀盐酸的体积∕mL | 剩余固体的质量∕g |
| 1 | 40 | 16 |
| 2 | 40 | 12 |
| 3 | 40 | 8 |
| 4 | 40 | 8 |
求:(1)样品中铜的质量?(2)样品中氧化铜的质量分数?(3)稀盐酸的质量分数?(共6分)
五、(本大题包括2小题。你只要选做其中的一个小题。若全做以30题计分。方程式2分一个,其它每空1分。共7分)
30.A、B、C、D、E五种物质都是含钙元素的化合物,它们之间存在下列转化关系,图中
H、G、F为另加的试剂。(7分)
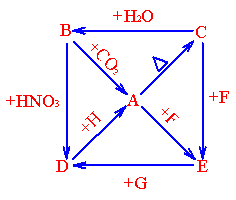
根据上图的关系回答下列问题:
(1)写出有关物质的化学式:
A 、B
C 、D
E 。
(2)写出A→E的化学方程式:
31. 化学物质及其变化与生活密切相关。(7分)
(1)健康人的体液pH必须维持在一定的范围内。如果体液pH超过正常范围,就会导致某些疾病的产生。胃液的pH 7。人体内的二氧化碳气体排出不畅时,会导致血液pH (选填“升高”或“下降”)
(2)自来水中含有少量的Ca(HCO3)2和MgSO4等可溶性盐。烧开水的壶中出现水垢的原因之一就是其中的Ca(HCO3)2发生了分解反应,生成了难溶的碳酸钙和水和二氧化碳,请你写出Ca(HCO3)2受热分解的化学方程式:
实验室若用自来水配制Ba(OH)2溶液,可能出现的现象是
造成这种现象的原因是(请用其中一个反应的化学方程式表示):
。