初三化学质量调研试题
说明:⒈本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
⒉ 试卷满分为100分。考试时间为90分钟。考试时允许使用CZ1206型函数计算器。
⒊可能用到的相对原子量质量:H-1 O-16 C-12 Na-23 Mg-24 Ca-40 Cl-35.5
第Ⅰ卷(选择题 共40分)
一、 选择题(本题包括20小题,共40分。每小题只有一个选项符合题意。请注意将答案按序号统一填写到以下表格中)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
⒈ 下列变化属于物理变化的是
A、煤的干馏 B、树叶杂草发酵制沼气C、石油的分馏D、用煤焦油提炼成分制医药
2.下列物质中,不能由金属与酸反应直接制得的是
A、 ZnCl2 B、 FeCl3 C、 MgSO4 D、 AlCl3
3.分别盛有浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分蒸发),则两瓶溶液
A、质量都变小了 B、溶质的质量分数都变大了
C、体积变小了 D、溶质的质量分数都变小了
4.下列化学方程式正确的是
![]()
![]() A、 2Fe+3H2SO4==Fe2(SO4)3+3H2 B、 AgNO3+HCl==AgCl +HNO3
A、 2Fe+3H2SO4==Fe2(SO4)3+3H2 B、 AgNO3+HCl==AgCl +HNO3
![]() C、 Zn+2HNO3==Zn(NO3)2+H2 D、 Fe2O3+6HCl==2FeCl2+3H2O
C、 Zn+2HNO3==Zn(NO3)2+H2 D、 Fe2O3+6HCl==2FeCl2+3H2O
5.固体氢氧化钠必须密封保存的原因是
① 氢氧化钠有毒 ②氢氧化钠有腐蚀性 ③氢氧化钠易吸收水分而潮解
④ 氢氧化钠有挥发性 ⑤氢氧化钠能与空气中的二氧化碳反应
A 、 ①② B、 ②③④ C、 ②③⑤ D、 ③⑤
6.判断复分解反应能否发生,可以不必考虑的是
A、 生成物中是否有沉淀 B、 生成物中是否有水
C、 生成物中是否有气体 D、 金属的活动性顺序
7.将铁片投入下列溶液中,反应完毕后溶液的质量减少的是
A、 稀HCl B、 稀H2SO4 C、 CuSO4 D、 FeSO4
8.正常雨水与酸雨的差异是
A、正常雨水显中性,酸雨显酸性
B、正常雨水的PH值约为5.6,酸雨的小于5.6
C、正常雨水不含杂质,酸雨含杂质 D、 正常雨水降在农村,酸雨降在城市
9.下列实验操作后,溶液温度升高的是
① 浓硫酸倒入水中 ② NaOH固体溶于水中 ③ 生石灰放入水中
④ 浓盐酸滴入浓烧碱中 ⑤NaCl晶体溶解于水中 ⑥NH4NO3晶体溶解于水中
A、只有①②③ B、有①②③④
C、 只有①②③④⑤ D、有①②③④⑤⑥
10.下列各组物质中,属于同一种物质的是
A、 食盐、食碱、NaCl B、生石灰、熟石灰、CaO
C、 石灰石、消石灰、Ca(OH)2 D、火碱、烧碱、NaOH
11.下列四种物质中,在一定条件下能与其他三种物质都能发生反应的是
A、 CuSO4 B、 CO2 C、 NaOH D、 HNO3
12.某地区进行土壤分析,发现pH值小于7,为了改良土壤,应选择加入的物质是
A、 氢氧化钠 B、 熟石灰 C、 硝酸铵 D、 氯化钠
13.做镘头的面团发酵过度会变酸,要除去酸味,可在面团中加入
A、 NaOH B、 NaCl C、 CaCO3 D、 Na2CO3
14. 实验表明,用碱性溶液浸泡新鲜的蔬菜,能有效除去蔬菜上的残留农药,从而降低对人体的损害。根据上述原理,对刚买回来的蔬菜,你认为应浸泡在哪种溶液中
A.白酒 B.食醋 C.烧碱溶液 D.碳酸钠溶液
15、下列四种盐溶液中一般不与其他物质发生复分解反应的是
A、KNO3 B、NaOH C、HCl D、CuSO4
16、在一定条件下,下列转化不能由一步反应实现的是
A.CO2→CaC03 B.HCl→NaCl C.Fe2O3→Fe(OH)3 D.Ca(OH)2→NaOH
17我国研制的大型激光器“神光二号”用了磷酸二氢钾(KH2PO4)大晶体。下列说法正确的是
A.磷酸二氢钾也可用作复合肥料 B.磷酸二氢钾是一种氧化物
C.磷酸二氢钾中含有氢气 D.磷酸二氢钾中磷元素为十4价
18、下面是某同学对有关火星探测资料的分析,其中结论错误的是
| 火星探测的有关资料 | 结 论 | |
| A | 火星南、北两极的极冠温度常年在一70~C至一140~C之间 | 那里很难找到液态水 |
| B | 在火星南、北两极发现“干冰” | “干冰”是固态二氧化碳 |
| C | 火星大气中存在甲烷气体 | 甲烷属于有机化合物 |
| D | 在火星上发现了大量盐的晶体 | 盐就是氯化钠 |
19、.在由C02和O2组成的混合气体中,测知碳元素的质量分数为20%,则混合气体中C02和02的质量比为
A.2∶1 B.1∶2 C.11∶4 D.11∶7
20、La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3,难溶于水,而LaCl3、La(NO3)3都易溶于水。下列各组物质中,不能直接反应制得LaCl3的是
A、La+HCl B、La2O3+HCl C、La(OH)3+HCl D、BaCl2+ La(NO3)3
第Ⅱ卷(非选择题,共60分)
21.(10分)按要求写出下列反应的化学方程式:
⑴氢氧化钠和稀硫酸反应
⑵双氧水和二氧化锰混合制氧气
⑶铁丝燃烧
⑷铁与硝酸银的反应
上述反应中,属于复分解反应的是 ,属于置换反应的是 (填序号)。
22.(5分)有下列物质:(1)高锰酸钾(2)碳酸钠(3)氯化钠(4)硫酸铜(5)氢氧化钙(6)氢氧化钠,请按下列要求将正确答案的化学式填在空白处:
(1) 在空气中易潮解且可用作干燥剂的是_____________ _______
(2) 在日常生活中可用于调味、防腐的是_______________ ______
(3) 在日常生活中可用于洗涤的是_____________________ ______
(4) 可用来配制农药波尔多液的是______________ ____________
(5) 可用于消毒的是
23、(4分)从硫、氧、氢、钠四种元素中,选择适当的元素组成可能得到的物质,按下列要求填写化学式:
(1) 碱性氧化物____ _______;酸性氧化物_____ _______;
(2) 碱_______ _____________;含氧酸________ _
24、(方程式为2分,共8分)将一枚生锈(主要成分为Fe2O3)的铁钉放入稀盐酸中,可观察到① _______ ② 该反应的化学方程式可表示为_____________ 反应一段时间,又可观察到① _________________ ② ,该反应的化学方程式为_____________ 。
25、(3分)现有三种溶液:A为硝酸盐、 B为碱、C为钠盐。三者之间存在下列关系:
(1)A、B两溶液混合,产生红褐色的沉淀:
(2)B、C两溶液混合,产生难溶于稀硝酸的白色沉淀。根据实验判断三种溶液中溶质的化学式分别为
A、____________B、__________________C、__________________
26.(2分)美国PPG公司生产的“自净玻璃”的神奇之处全在于它穿上40纳米厚的二氧化钛(TiO2)“纳米膜外套”。其“纳米膜外套”可与太阳光线中的紫外线作用,分解落在玻璃上的有机物,使有机物化为乌有;还能使玻璃表面的雨点或雾气变成一个薄层而使玻璃表面湿润,并洗掉表面的脏物。工业上二氧化钛可用下列方法制得: 2FeTiO3+7Cl2+3C=2X+2FeCl3+3CO2 , X+O2=TiO2+2Cl2 ,
则X的化学式为 。
27.(4分)痕检是公安机关提取犯罪嫌疑人指纹的一种重要方法,硝酸银显现法就是其中的一种:人的手上有汗迹,用手动用白纸后,手指纹线就留在纸上。如果将硝酸银溶液小心地涂到纸上,硝酸银溶液就跟汗迹中的氯化钠作用,生成氯化银,其反应的化学方程式是 。氯化银在光照条件下分解生成银粒和另一种单质,其反应的化学方程式是 。银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由灰褐色逐渐变成黑色,从而显现出黑色的指纹线。
28、(9分)为了证明长期暴露在空气中的氢氧化钠溶液已经部分变质,请分别选用三种不同物质类别的试剂完成三种实验方案的设计、并填写实验报告:
| 实验步骤 | 实验现象 | 化学方程式 |
| 1 | ||
| 2 | ||
| 3 |
29、(方程式2分,共7分)某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究。
实验一:探究碳酸氢钠的化学性质
(1) 取样品溶于适量的水中,测得溶液的pH大于7。
(2) 向小苏打样品中滴加盐酸,有大量气泡产生,经检验该气体是二氧化碳。该反应的化学方程式为 。
(3) 向小苏打的溶液中加入澄清石灰水,生成了白色沉淀。
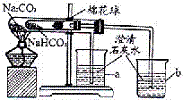 (4)同学们通过查阅资料,在老师的指导下采用了右图所示装置对小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊。(提示:无水硫酸铜遇水变蓝色)试回答:
(4)同学们通过查阅资料,在老师的指导下采用了右图所示装置对小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊。(提示:无水硫酸铜遇水变蓝色)试回答:
① 在实验结束时,操作上要注意的问题是: 。
② 由实验(4)可以得出的结论是 。
请归纳出小苏打的化学性质(至少三点)(1) 。
(2) 。(3) 。
计算题:(30题3分,31题5分,共计8分)
30.25g石灰石跟适量的盐酸混合,充分反应后(杂质不与酸反应),反应后混合物质量
减小了8.8g,求石灰石中碳酸钙的质量分数。
31.将20g不纯的氯化镁样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,得到溶质质量分数为10%的溶液234g。求:
(1)样品中氯化镁的质量;
(2)加入的氢氧化钠溶液中溶质的质量分数。