初三联考 化学试题
化学试题
命题学校:沈阳铁路实验中学 命题人:陈艳 王铁英 校对人:邹海滨
时间:2004.4.3
考试时间65分钟,试题满分65分
相对原子质量;H-1 O-16 N-14 C-12 Ca-40 Na-23 Cl-35.5
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 |
一、 选择题(8分 )
下列各小题的备选答案中,只有一个是正确的。请将正确的答案的标号填在上面的表格内,每小题1分。
1.下列变化,一定不属于化学变化的是
A.石墨转化为金刚石 B.光合作用 C.工业制氧气 D.煤气中毒
2.食品卫生与身体健康密切相关。下列食品导致对人体有害的是
①用石灰水保存鸡蛋②为保持肉制品鲜美,在香肠中添加过量NaNO2③蒸馒头时加入适量纯碱④为了让猪长得瘦,用“瘦肉精”(一种含激素饲料)饲养生猪
A. ①② B. ①③ C. ②③ D. ②④
3.国际冰川专家最近指出:喜马拉雅山冰川按现在的消融速度,至2035年将全部融化,与这种现象相关密切的气体是
A.CO2 B.CO C.N2 D.O2
4.下列有关物质的应用中,具有重大伤害事故隐患的是
A.用活性炭作冰箱除臭剂 B.用CO2灭火
C.用干冰进行人工降雨 D.庆典活动时大量使用氢气球
5.将t℃的某饱和溶液蒸发一定量水后再恢复到t℃时,有晶体析出,下列说法中错误的是
A. 溶液析出晶体后仍为饱和溶液 B.溶液的质量减少
C.溶液中溶质的质量分数减少 D.该溶质在t℃时的溶解度不变
6.将下列物质混合,混合前后烧杯里溶液的质量不变的是
A.浓HCl和浓H2SO4
B. Na2CO3溶液和稀HCl
C.CuSO4溶液和NaOH溶液 D.NaOH溶液和稀HCl
7.下列各组物质混合后,能得到无色透明溶液的是
A. 氢氧化钡溶液、碳酸钾溶液、足量稀硫酸
B. 苛性钠溶液、硫酸铜溶液、足量稀硝酸
C. 澄清石灰水、碳酸钾溶液、足量稀盐酸
D. 氯化镁溶液、硝酸银溶液、足量稀硝酸
8. .科技文献中经常出现下列词汇,其中与物质的颜色无联系的是
A.赤色海潮 B.绿色食品 C.白色污染 D.棕色烟气
二、 选择题( 4分 )
下列各小题的备选答案中,有一个或两个是正确的。请将正确的答案的标号填在上面的表格内,每小题2分。
9.A元素是一种活动性比铝强的金属元素,它的氧化物为A2O3,它所对应的碱
A(OH)3难溶于水,而ACl3、A(NO3)3都易溶于水。下列各组物质中不能直接反应制得ACl3的是
A. A(NO3)3+BaCl2 B.A2O3+HCl
C.A+HCl D. A(OH)3+CuSO4
10.通常条件下,下列转化不能由一步反应实现的是
![]()
![]() A.Cu CuO
B.CuO CuCl2
A.Cu CuO
B.CuO CuCl2
![]()
![]() C.CuCl2 Cu(OH)2
DCu Cu(OH)2
C.CuCl2 Cu(OH)2
DCu Cu(OH)2
三、 填空题(13分)
1.⑴用符号表示:1个亚铁离子 ,二个氮原子 ,
三个二氧化碳分子
⑵以前某些治疗感冒的常用药,因含有PPA(苯丙醇胺),对人体有较大副作用而被禁用。PPA的化学式为C9H13ON,它由 种元素组成,每个PPA分子中共含有 个原子 ,其相对分子质量为 。
2. Na2CO3和CuSO4等物质,在从水溶液中析出时,常会带出一部分水分子。上述两种物质形成的结晶水合物的化学式分别为 、 。
3.有一种物质分别加入KOH溶液、饱和石灰水和稀硫酸中,能出现三种不同现象,该物质是 。
4. .检验NaOH溶液中是否吸收了SO3气体的方法是:取少量该溶液,加入
溶液,若出现 现象,则说明NaOH溶液中吸收了SO3气体。有关反应的化学方程式 ;
四、 简答题(14分)
1.用化学方程式说明下列问题
⑴氢氧化钠溶液要密封保存,否则会变质。
⑵用稀硫酸作电镀、焊接金属制品前的清洁剂
2.分别用一种试剂将下列物质中混入的少量杂质除去。(括号中是混入的杂质)
| 物质 | 需加入试剂 | 有关的化学方程式 |
| HNO3 (H2SO4) | ||
| FeSO4(CuSO4) | ||
| Cu (Al) |
![]()
|
⑴该同学家的庄稼缺两种营养元素,它们是 (填N、P、K或微量元素)
⑵该同学想购买含氮量最高的化肥,下列化肥中他买了
A.NH4NO3 B.NH4HCO3 C.CO(NH2)2 DNH4Cl
4.物质的某些性质可能有利于人类,也可能不利于人类,请仿照示例填表;
|
| 有利的一面 | 不利的一面 |
| 氧气 | 供给呼吸、支持燃烧 | 使金属氧化锈蚀 |
| 一氧化碳 | ||
| 二氧化碳 |
五、 实验题(13分)
1.将碱A和盐B两种溶液,按下图程序进行实验,并假设每次反应都恰好完全反应
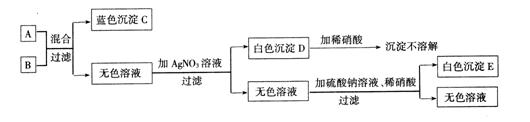
根据上述关系写出下列物质的化学式:
A B C D E
2.19世纪末,科学家瑞利通过如下两种实验方法制取氮气,并测出其密度,从而导致了科学上的某项重大发现,请你参与他的科学发展过程,填写下表:
| 实验步骤 | 解释或结论 |
| ⑴将清新洁净的空气通过氢氧化钠溶液,再通过浓硫酸 | 通过氢氧化钠溶液的目的是为了除去空气中的 。 |
| ⑵将气体通过能与氧气反应的物质(瑞利提示:反应不能生成新气体) | 请写出能用于除尽氧气的物质名称: 。 |
| ⑶收集气体,并测出该气体密度 | 密度为1.2572g/L |
实验一:利用空气分离出氧气
实验二;用亚硝酸钠(NaNO2)和氯化铵(NH4Cl )反应制取氮气,同时还生成了氯化钠和一种常见的溶剂,测得由此法得到的氮气密度为1.250 g/L,该反应的方程式为
试分析两种方法制得氮气密度不同的原因:
3.现有以下6种装置,用它们的序号填空
①证明一氧化碳中含二氧化碳,应将气体经过_________装置;
②除去二氧化碳中含有的少量的一氧化碳,可将气体经过_______装置;
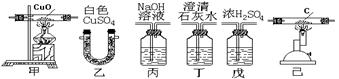 |
③欲将混有少量水蒸气的二氧化碳转化为纯净的一氧化碳气体,按正确连接顺序选用的装置是:戊à_______à_______à戊。
六、 计算题(8分)
1.近年来,乳酸成为人们研究 的热点之一。乳酸在医药、食品等工业中应用前景广阔。乳酸的化学式为C3H6O3,试计算;⑴乳酸中碳、氢、氧元素的质量比等于
⑵乳酸中碳元素的质量分数等于
2.有一纯碱样品中混有一定量的氯化钠,该纯碱样品40g能与168.8g稀盐酸恰好完全反应,共放出8.8g气体,求⑴这种纯碱样品中碳酸钠的质量分数
⑵所得溶液中溶质的质量分数
 七.理化综合(5分)
七.理化综合(5分)
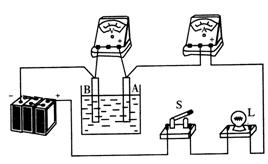
如图所示A、B为两个电极,放在盛有水的玻璃容器里,闭合开关后,向水中逐滴滴入氢氧化钠溶液,电极上将有气泡产生,与电源正极相连的A极上出现的气泡为
B电极上出现的气泡为
在这一过程中,电流表示数变 ,电压表示数变 。
灯泡亮度变 。