初三模拟考试化学试题
沉着、冷静、细心……祝同学们考试成功!
友情提示:1、考试时间70分钟,满分60分
2、请将选择题的答案用2B铅笔涂写到答题卡相应的位置
3、可能用到的相对原子质量:H-1,C-12,O-16,Cl-35.5,Na-23,Ba-137
一、选择题(本题包括10小题,1-5小题每题1分,每小题只有一个选项符合题意,6-10小题每题2分,每小题只有一个或二个选项符合题意,少选得1分,但只要错选就不得分.共15分。)
1.“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝质易拉罐、铜导线等可以归为一类加以回收,它们属于
A.有机物 B.金属或合金 C.氧化物 D.盐
2.A2+结构示意图为, 则它的核电荷数及其氧化物的化学式分别是
A.+12,AO B.+10,A2O
C.+2,AO2 D.+12,A2O
3.令人信服的证明分子在化学变化中可以再分的事实是
A.工业上蒸发分离液态空气制取氧气 B.固态碘受热形成紫红色的烟
C.蔗糖放进水里不见了 D.氧化汞受热分解生成汞和氧气
4.下面关于“2”的解释中,不正确的是
A.Mg2+中的“2”表示镁带有2个单位的正电荷
B.H2SO4 中的“2”表示1个硫酸分子中有2个氢原子
C.H2O中的“2”表示水分子中有2个氢原子
D.Al2(SO4 )3中O上面的“2”表示氧元素的化合价为-2价
5.下列工农业生产、日常生活中化学知识运用错误的是
A.用食醋除去水壶中的水垢 B. 冰箱内放置木炭除异味
C. 用稀盐酸除铁锈 D. 在铁桶内配制农药波尔多液
6.某环保检测站取刚降下的雨水,每隔一定时间测定其pH,数据如下:
| 测定时间/分钟 | 0 | 1 | 2 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
下列有关说法不正确的是
A.雨水酸性逐渐减弱
B.一段时间后雨水酸性渐趋稳定
C.酸雨可腐蚀某些建筑物和金属制品
D.酸雨是由于空气受硫的氧化物或氮的氧化物污染形成的
7.下列括号中的物质是除去杂质所需的药品,其中错误的是
A.NaCl中有杂质Na2SO4(氯化钡)
B.FeS04中有杂质CuSO4(铁粉)
C.CO2中有少量CO(灼热的氧化铜)
D.CO2中有少量HCl气体(氢氧化钠溶液)
8.向含有盐酸和氯化铜的混合溶液中加入氢氧化钠溶液,产生沉淀的质量Q与加入氢氧化钠溶液的质量W的关系,图象正确的是
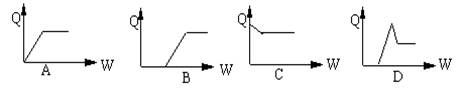
9.关于下列变化过程CO2→CO、H2→H2O、CO→CO2、C→CO2正确的说法是
A.都可以通过化合反应实现 B.都可以通过置换反应实现
C.都可以通过与单质反应实现 D.变化过程中都必须加入氧化剂
10.一包固体物质可能由Na2CO3、K2SO4、NaCl中的一中或几种组成。取试样少许溶于水,加入过量BaCl2溶液,产生白色沉淀,该沉淀不溶于稀HNO3。过滤,在滤液中加入用硝酸酸化的AgNO3溶液,产生白色沉淀。则原固体物质的组成中
A.一定有Na2CO3 B.一定有NaCl
C.一定有K2SO4 D.可能有NaCl
初三模拟考试化学试题
| 题 号 | 二 | 三 | 四 | 总 分 |
| 得 分 |

二.填空题(本题包括6小题,共25分)
11、(1)例举二种熟悉的化学变化现象:(每空0.5分)
①_______________________________。
②_______________________________。
(2)例举二种常见的化学肥料(填写名称):
①_______________________________。
②_______________________________。
(3)例举二种可用排水法收集的气体(填化学式):
①_______________________________。
②_______________________________。
(4)某同学在实验室里过滤一种含固体物质的浑浊液,发现滤液仍很浑浊,其原因可能是:①_______________________________。
②_______________________________。
12.请从铁、高锰酸钾、氧气、氢气、硫酸铜、盐酸、水、氢氧化钙中选择适当的物质(每种物质只能选用一次),按要求写出有关化学方程式。(每空1分)
(1)化合反应(产物常温下呈液态) 。
(2)分解反应(产物有三种) 。
(3)置换反应(产物中无气体生成) 。
(4)复分解反应(产物中有水生成) 。
13.(3分)我国“长征二号”火箭的主要燃料是偏二甲肼(用R表示)在火箭发射进,偏二甲肼和四氧化二氮剧烈反应,产生大量的气体并释放出大量的热,该反应的化学方程式如下:R+2N2O4==== 3N2 + 2CO2 +4H2O,则偏二甲肼的化学式为_______________,推测化学式的依据是 ___________________________________________________________。
14.(每空1分)录相机用的高性能磁粉,主要材料之一是由三种元素组成的化学式为CoXFe3-XO3+X的化合物,已知氧为-2价,钴和铁可能呈现+2或+3价,且上述化合物中,每种元素只有一种化合价,则x值为 __________________,铁的化合价为 ____________ 钴的化合价为______________________ 。
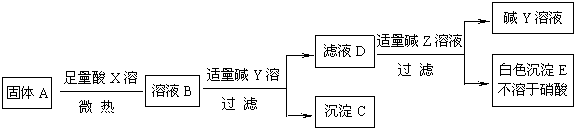 15.(每空1分)物质A、B、C、D、E、X、Y、Z都是初中化学中常见的物质,其中A为氧化物。它们具有如下相互转化关系:
15.(每空1分)物质A、B、C、D、E、X、Y、Z都是初中化学中常见的物质,其中A为氧化物。它们具有如下相互转化关系:
用化学式回答:
(1)若沉淀C呈红褐色,则C是 。
(2)若沉淀C呈蓝色,则A是 。
(3)无论固体C呈红褐色还是呈蓝色,酸X一定是 ,碱Z一定是 。
16.(每空1分)阅读下面材料,回答下列问题。
自从非典型肺炎在我国部分地区出现以来,过氧乙酸作为高效消毒剂被广泛使用。过氧乙酸在常温下是一种无色有刺激性气味的液体,易挥发,易溶于水和醋酸。它对呼吸道黏膜有刺激性,高含量的过氧乙酸溶液对皮肤有腐蚀性。作为一般商品的过氧乙酸是40%的醋酸溶液,使用前通常先用蒸馏水等将其稀释。消毒时可用喷雾法消毒,也可将其配制成0.2%的水溶液洗手消毒。过氧乙酸不稳定,易分解生成无毒的物质。若用喷雾法消毒,过氧乙酸在半小时内就可完全分解。
(1)在过氧乙酸的质量分数为40%的醋酸溶液中,溶质是 ,溶剂是 。
(2)分别指出过氧乙酸的物理性质和化学性质。
物理性质:
化学性质:
(3)1 00 g过氧乙酸的质量分数为0.2%的洗手液中.含过氧乙酸 g。
(4)不慎将高含量的过氧乙酸溶液沾到皮肤上.应怎样处理?
(5)用过氧乙酸消毒过的房间,人若要进入,应注意什么?(根据过氧乙酸的性质回答)
| 得分 | 评卷人 |
三、实验题(本题包括2小题,共12分)
17.(8分)某中学化学兴趣小组的同学在查阅资料时发现金属氧化物A(固体)也能加快氯酸钾的分解速率即起催化作用,且A和二氧化锰的最佳催化温度均在500℃左右。于是对A和二氧化锰的催化性能进行了定量对照实验,实验时均以收满500mL氧气为准(其他可能影响实验的因素均已忽略)。
表1 用MnO2作催化剂
| 实验序号 | KClO3质量/g | MnO2的质量/g | 反应温度/℃ | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
表2用A作催化剂
| 实验序号 | KClO3质量/g | A的质量/g | 反应温度/℃ | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
请回答:
(1)上述实验中的待测数据应是___________________;(1分)
(2)表2内所发生反应的化学方程式:___________________________。(1分)
(3)若选择下列部分装置通过组合来完成该实验,你觉得最佳装置组合是(填序号) _________,各装置的正确连接顺序是(填接口字母,括号内容可以不填满也可以再加)a→( )→( )→( ) (前2分后1分)
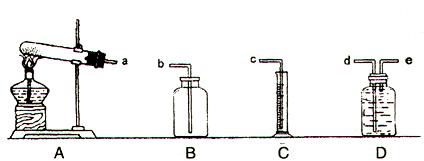
(4)如何判断已收集到500mLO2_________________________________。(2分)
(5)完成此研究后,他们准备发表一篇小论文,请你替他们拟一个论文题目:
_______________________________________________________。
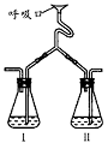 18.为验证人体呼出气体中含有的CO2不是来自空气,而是
18.为验证人体呼出气体中含有的CO2不是来自空气,而是
人体代谢作用产生的。某学校学生课外活动小组设计了
如右图所示装置,你认为该装置应选用的试剂是 。
瓶I 瓶Ⅱ
A. Ca(OH)2 NaOH
B. NaOH Ca(OH)2
C. 稀HCl Ca(OH)2
D. NaOH BaCl2
你选择的理由是:
.

四、计算题(本题包括2小题,共8分)
19.(3分)市售脑黄金化学式为C25H51COOH,其相对分子质量为:___________其中氧元素和氢元素的质量比为:___________。
20.(5分)运用侯氏制碱法制得的纯碱中,可能含有少量的氯化钠。现取某种仅含有氯化钠杂质的纯碱样品23.4g,全部溶解在350g水中。加入氯化钡溶液166g,恰好完全反应生成碳酸钡沉淀。过滤、称量、干燥、沉淀的质量为39.4g。
(1)写出形成沉淀的化学方程式 。(1分)
(2)求23.4g纯碱样品中碳酸钠的质量。(2分)
(3)求滤液中氯化钠的质量分数。(2分)