初中毕业生升学考试理科综合―化学试卷
一、选择题(共16分)
1.物质常发生下列变化:①挥发;②燃烧;③熔化;④发光;⑤锈蚀;⑥腐烂。其中一定属于化学变化的是
A.①②③ B.③④⑥ C.②⑤⑥ D.①⑤⑥
2.小明吃过饼干后忘记密封,几天后他发现剩下的饼干变软了。这说明空气中含有
A.氧气 B.二氧化碳 C.氮气 D.水蒸气
3.下列实验操作正确的是
A.实验室用氯酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯
B.将粗盐加到盛有10mL水的量筒中,用玻璃棒搅拌使其溶解
C.先将pH试纸用蒸馏水润湿后,再测定溶液的pH
D.先用双手紧捂试管,再将导管一端浸入水中检查装置的气密性
4.酸雨、臭氧层破坏和温室效应是全球环境的三大热点问题。下列选项中不会加剧这三大环境问题的是
A.化石燃料的燃烧 B.汽车尾气的排放
C.使用太阳能热水器 D.使用氟里昂作致冷剂
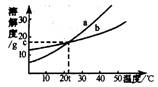 5.如图是a、b两种固体物质的溶解度曲线。下列说法中不正确的是
5.如图是a、b两种固体物质的溶解度曲线。下列说法中不正确的是
A.a的溶解度大于b的溶解度
B.在t℃时,a、b的饱和溶液中溶质的质量分数相同
C.当a中含有少量b时,可以用结晶法提纯a
D.a、b都属于易溶物质
6.氢气、碳、一氧化碳都具有的化学性质是①都能在空气中燃烧 ②常温下都较稳定 ③常温下都能与氧化铜反应 ④都具有还原性⑤都具有氧化性
A.①②③ B.①②④ C.②③④ D.①③⑤
 7.如图所示,在试管和小气球中分别盛有一种液体和一种固体物质,将气球中
7.如图所示,在试管和小气球中分别盛有一种液体和一种固体物质,将气球中
的固体物质小心地倒入试管中,可观察到气球逐渐胀大,下列各组中不能达到上
述要求的是
A.锌粒和稀硫酸 B.纯碱和稀盐酸
C.氯化钠和水 D.鸡蛋壳和醋
8.某同学想用实验证明高锰酸钾溶液的紫红色是MnO4-离子的颜色,而不是K+离子的颜色。他设计的下列实验事实对证明该问题无意义的是
A.将高锰酸钾晶体加热分解,所得固体质量减少
B.观察氯化钾、硝酸钾、硫酸钾溶液都没有颜色,表明溶液中K+离子无色
C.向氯化钾溶液中加入过量锌粉,振荡、静置后未见明显变化,表明锌与K+离子不反应
D.向高锰酸钾溶液中加入适量锌粉,振荡、静置后见紫红色褪去,表明MnO4-离子呈紫红色
二、(本题包括7小题,共27分)
9.生活中很多现象都与化学有着密切的联系。在CO2、CO、SO2、H2O、甲醇、乙醇六种物质中选择正确的物质填人相应空格内。
(1)饮用假酒引起中毒导致眼睛失明,是由于假酒中含有 的原因。
(2)人们在进入干涸深井前必须做灯火实验。这是因为深井中可能积存大量的 。
(3)用煤炉取暖时发生中毒,主要原因是由于煤燃烧时产生的 排放不畅而引起的。
(4)煤中一般都含有硫元素,因此煤燃烧时会产生污染空气的 气体。
10.我国于2003年10月15日用长征二号F型火箭成功发射了“神舟”五号载人飞船,实现了中华民族的千年梦想。长征二号F型火箭所用的燃料是偏二甲肼(化学式为C2H8O2),火箭发射时,该燃料与四氧化二氮(N2O4)剧烈反应,生成二氧化碳、水和组成空气的一种气体单质。则该反应的化学方程式是: 。
11.证明铁、铜两种金属的活动性顺序时,若选用一种酸溶液。则这种酸是 (填一种即可,下同)。若选用一种盐溶液。则这种盐是 。
12.科学实验证明香烟所产生的烟雾中至少有300多种化合物对人体有不同程度的危害。为了检验香烟烟雾中是否含有CO2和CO,在对烟雾进行适当处理后(以排除其它成分的干扰)。依次通过足量的以下试剂:①澄清石灰水;②浓硫酸;③灼热的黑色氧化铜粉末;④澄清石灰水。发现①④变浑浊。
(1)①中变浑浊的现象说明了什么?
(2)烟雾中是否存在CO? ,你做出判断依据的实验现象是什么?
13.向盛有澄清石灰水的试管中加入适量饱和碳酸钠溶液。恰好完全反应。观察到的现象为
,对应化学反应属于反应基本类型中的 反应;接着向试管中滴入几滴酚酞试液。溶液变一色,再逐滴加入盐酸至过量,先观察到的现象是 ,后观察到的现象是 。
14.有一无色溶液A,可能含有H2SO4、HNO3、NaCl、Na2SO4、NaNO3、CuSO4、Na2CO3等物质中的一种或几种,取少量A做如下实验,现象如下图所示,请按下列要求填空:
(1)白色沉淀C是 ,G是 。
(2)无色溶液A中一定不存在的物质为 。
(3)无色溶液A可能的组成有:
① ,② ,③ ,④ 。
15.在探究CO2和NaOH是否发生化学反应时。某同学设计出如下实验装置。
(1)A中反应的化学方程式为 ;
(2)B装置的作用是 ;
(3)A中反应结束后,关闭K,挤压C中胶头滴管的胶头,观察到的现象是 。
(4)为证明CO2和NaOH肯定发生了化学反应,可取出C中溶液,向其中加入 (任填一种),若 (填相应的反应现象)即可判定CO2和NaOH发生了化学反应。
三、(本题共7分)
16.侯德榜是我国著名的化学家。由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠。现取仅含氯化钠杂质的纯碱样品33.2g,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g。
求:(1)该纯碱样品中Na2CO3的质量;
(2)反应后所得溶液中溶质的质量分数。
参考答案
1.C 2.D 3.A 4.C 5.A 6.B 7.C 8.A
9(1)甲醇 (2)CO2 (3)CO (4)SO2
10.C2H8N2+2N2H4=2CO2+4H2O+3N2
11.HCl或H2SO4;CuSO4或其它
12.(1)说明烟雾中含有CO2 (2)存在CO; ④中澄清石灰水变浑浊
13.有白色沉淀生成;复分解;红;红色逐渐褪去至无色,沉淀逐渐溶解,有气泡产生
14.(1)BaSO4 AgCl (2)CuSO4、HNO3、H2SO4
(3)①Na2SO4、Na2CO3
②Na2SO4、Na2CO3、NaCl
③Na2SO4、Na2CO3、NaNO3
④Na2SO4、Na2CO3、NaCl、NaNO3
15.(1)CaCO3+2HCl=CaCl2+CO2↑+H2O (2)吸收HCl气体 (3)D中水沿玻管上升(或倒吸)
(4)稀HCl或稀H2SO4;产生气泡(或CaCl2或BaCl2等溶液;产生白色沉淀)
16.解;设样品中含Na2CO3的质量为x,生成NaCl的质量为y,依题意知产生CO2的质量为33.2g+130g-150g=13.2g。则:
Na2CO3+2HCl=2NaCl+CO2↑=H2O
106 117 44
x y 13.2g
![]() x=31.8g
x=31.8g
![]() y=35.1g
y=35.1g
原样品中含NaCl 33.2g-31.8g=1.4g
![]()
答:该纯碱样品中Na2CO3为31.8g,所得溶液中溶质的质量分数为24.3%。