初三化学中考模拟题(七)
(时间40分钟,满分40分)
一、 选择题(每小题只有一个正确答案,每小题2分,共10分)
1.能证明分子在化学变化中能再分的事实是( )
A.从液态空气中制取氧气 B.水电解生成氢气和氧气
C.干冰升华 D.水变成水蒸气
2.下列叙述中正确的是 ( )
A.生成盐和水的反应不一定是中和反应
B.碱的分子中必定含有氢元素和氧元素
C.生成单质的反应有可能是化合、分解、置换和复分解反应中的任何一类
D.仅由非金属元素不可能组成盐
3.在鉴定某无色溶液的组成时,不同的实验者得出了不同的实验结果如下,其中可能正确的是( )
A.硝酸铜、氯化钠、氯化氢 B.硝酸钡、氢氧化钠、氯化钾
C.氯化钠、硝酸银、硝酸 D.硫酸钾、氢氧化钠、硝酸钡
4.向20℃时的饱和硫酸铜溶液中加入少量的无水硫酸铜粉末,在温度不变的条件下,下列有关叙述正确的组合是( )
①铜溶液的溶质质量分数增大 ②硫酸铜溶液的溶质质量分数减小 ③硫酸铜溶液的溶质质量分数不变 ④析出硫酸铜晶体的质量大于加入的无水硫酸铜的质量 ⑤析出硫酸铜晶体的质量等于加入的无水硫酸铜的质量 ⑥析出硫酸铜晶体的质量小于加入的无水硫酸铜的质量
A.①⑥ B.②④ C.③⑤ D.③④
5.在一个密闭的钢筒内有四种物质,通过电火花点燃后,充分发生反应,测得反应前后各物质的质量如下:
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量(克) | 4 | 10 | 1 | 25 |
| 反应后质量(克) | 未测 | 21 | 10 | 9 |
已知甲的相对分子质量为n,丁的相对分子质量为2n,则该反应的化学方程式中甲与丁的化学计量数之比是( )
A.1:1 B.1:2 C.1:3 D.2:1
二.填空题(本题3个小题,共8分)
6.(2分)空气中含量最多的元素与地壳中含量最多的元素以及地壳中含量最多的金属元素所组成的化合物的化学式是 ,根据初中化学中物质分类的方法它应属于 类。
7.(2分)已知t℃时四种化合物在水中及液氨中的溶解度如下:
| AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
| 水 | 170g | 9.2g | 1.5×10-4g | 33.3g |
| 液氨 | 8.6g | 97.2g | 0.8g | 0 |
写出t℃时上述几种化合物在液氨中能发生复分解反应的化学方程式:
|
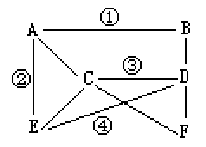
Zn粒、CuCl2溶液、Ca(OH)2溶液、稀H2SO4、
Na2CO3溶液、Ba(NO3)2溶液。图中同一连线两
端的物质可相互发生化学反应,请推断:
(1)A是 ,
F是 (填物质名称)
(2)写出下列符合图中编号的各化学方程式,
① ,
②
三.实验与实践题(本题共2个小题,共12分)
9.(8分)从H2SO4、Na2SO4、Na2CO3、NaCl、NaNO3、Cu(NO3)2、HNO3七种溶液中取出其中的两种,进行混合及有关实验,所观察到的现象已记录在下表中。试根据各步实验及其现象先进行分步推断(即实验进行到该步所能作出的某物质肯定存在、否定存在或可能存在的判断),再综合推断所取两种溶液的可能组合。
| 步骤 | 实验操作 | 实验现象 | 分步推断 |
| (1) | 将取出的2种溶液进行混合 | 混合溶液无色、澄清。 | 混合溶液中肯定不含Cu(NO3)2 |
| 无其它明显现象 | 混合溶液肯定不是下列组合: | ||
| (2) | 用PH试纸测定混合溶液的PH | 测定结果PH=2 | |
| (3) | 向混合溶液中滴入足量的Ba(NO3)2溶液 | 有白色沉淀出现 | |
| (4) | 向上述溶液过滤所得的滤液中滴加AgNO3溶液 | 无明显现象 | |
| 混合溶液的可能组合(写出溶质的化学式,有几组要写几组) | ① 和 ② 和 ③ 和 ④ 和 ○ 和 ○ 和 | ||
10.(4分)根据下面给出的药品和实验装置,设计一个实验,粗略测定由铜和锌两种金属组成的合金―黄铜中锌的质量分数(黄铜已加工成粉末)。
备用药品:稀硫酸、浓硫酸、氧化铜
备用实验装置(另有托盘天平、酒精灯可用):
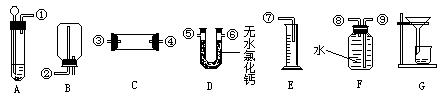
根据你设计的实验方案回答下列问题:
(1) 你选用的药品是
(2) 你选用的实验装置有(填编号) 。若需要组装,则连接的顺序是(用装置接口处的编号表示,若不需要组装,则不填) 。
(3) 称取a克黄铜粉末样品进行实验,实验中你需要测定的其它数据是( )
A、生成氢气的体积 b升 B、反应前仪器和药品的质量c克
C、反应后剩余固体的质量d克 D、反应后仪器和药品的质量e克
(4) 计算合金中锌的质量分数 (用题给字母表示)(可能用到的数据:相对原子质量:Zn―65 Cu―64 O―16 H―1;在实验条件下,2.0克氢气的体积为22.4升)。
三.计算题(5分)(
可能用到的相对原子质量:Ca―40 Na―23 O―16 H―1;C―12)
11.向一定量的由Ca(OH)2和NaOH固体配成的混合溶液中加入足量的纯碱溶液,经充分反应后,将生成的沉淀过滤、洗涤、干燥,冷却称量,所得沉淀的质量与配制混合溶液的固体的总质量相等,则配制混合溶液所用的Ca(OH)2与NaOH的质量比是 。