初三化学全真模拟试卷(一)
相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5
K-39 Ca-40 Ba-137
一、单项选择题(2×22分=44分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 答案 | |||||||||||
| 题号 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| 答案 |
1、你所看到的下列生活现象,属于化学变化的是( )
A、 铁器生锈 B、食物腐败 C、酒精挥发 D、燃放烟花
2、有一种病叫缺铁性贫血症,这里的“缺铁”指的是缺少( )
A、铁单质 B、三氧化二铁 C、铁元素 D、四氧化三铁
3、厄尔尼诺现象产生的原因之一是大气中的二氧化碳剧增,为缓解此现象,最理想的燃料是( )A、优质煤 B、天然气 C、汽油 D、氢气
4、生物细胞中含量最多的元素是( )A、氧 B、碳 C、硅 D、氢
5、2000年10月,世界卫生组织发表报告指出,孟加拉国正处于“人类历史上最严重的集体中毒”,全国一亿二千五百万人口中,最少有八千五百万人长期饮用含剧毒砒霜的地下水。这场环境灾难史无前例,甚至超过了1986年切尔诺贝利核电厂爆炸事件。砒霜的化学式为As2O3,其中As(砷)的化合价为( )A、+6价 B、+5价 C、+4价 D、+3价
6、2001年7月13日,中国北京申办2008年夏季奥林匹克运动会成功。北京申办的主题之一是“绿色奥运”,下列措施与环境保护无关的是( )
A、将一些重污染工厂迁出市内,建立商业区或绿地
B、将燃汽油汽车改造成燃清洁天然气的汽车
C、兴建的大量体育馆可以利用太阳能
D、全北京市民努力学习外语,准备加入志愿者队伍,为奥运服务
7、下列各组中的物质属于同一类别(指酸、碱、盐、氧化物)的是( )
A、氯化钙 氧化钙 硝酸钙 B、烧碱 纯碱 熟石灰
C、纯碱 胆矾 硫酸钠 D、干冰 冰 金刚石
8、下面是几种农作物生长时对土壤PH要求的最佳范围:茶5~5.5 西瓜6 大豆6~7 甜菜7~7.5。如果某地区经常降酸雨,以上农作物最不适宜种植的是( )A、大豆 B、西瓜 C、茶 D、甜菜
9、有液态氢、二氧化碳、盐酸、熟石灰,有关用途为①建筑材料②金属表面除锈③灭火④火箭燃料。请按前面物质的顺序排列出它们的用途( )
A、④③②① B、③④①② C、④③①② D①②③④
10、下列仪器中不能加热的是( )
A、蒸发皿 B、量筒 C、燃烧匙 D、试管
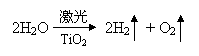 11、氢气是一种绿色能源,科学家最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气的新技术,其中海水分解可用化学方程式表示为 。下列说法正确的是( )
11、氢气是一种绿色能源,科学家最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气的新技术,其中海水分解可用化学方程式表示为 。下列说法正确的是( )
A、TiO2在反应中作氧化剂 B、水分解不产生污染物
C、TiO2在反应中作催化剂 D、该技术可以将太阳能转化为氢能
12、历届奥运会开幕式都要举行隆重的“火炬接力”,火炬中的燃料是丁烷(C4H10)。下列关于丁烷的叙述正确的是( ) ①丁烷是由碳、氢元素组成的 ②丁烷是由丁烷分子构成的 ③丁烷分子由碳、氢元素构成的 ④丁烷由4个碳原子和10个氢原子组成 ⑤丁烷分子是由碳原子和氧原子构成的
A、①②③④⑤ B、①②⑤ C、②③④⑤ D、①②④⑤
13、下列物质的用途跟它的物理性质密切相关的是( )
A、氢气用作高能燃料 B、一氧化碳用来冶炼生铁
C、稀硫酸用来清除铁锈 D、干冰用于人工降雨
14、从基本反应类型看,反应Cu+Hg(NO3)2=Cu(NO3)2+Hg属于( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
15、某学校化学课外活动小组,近期在扬州市区某街道十字路口,测定空气被污染的情况时,发现CO气体的含量超出了国家规定的标准。你认为其主要原因是( ) A、机动车辆排放大量废气 B、商店较集中
C、生活污水的大量排放 D、人流量较大
16、正电子、负质子等都是反粒子。它们跟通常所说的电子、质子相比较,质量相等但电性相反。科学家设想在宇宙中可能存在完全由反粒子构成的物质----反物质;物质与反物质相遇会产生“湮灭”现象,释放出巨大的能量,在能源研究领域中前景广阔。请你推测,反氢原子的结构可能是( )
A、由一个带正电荷的质子与一个带负电荷的电子构成
B、由一个带负电荷的质子与一个带正电荷的电子构成
C、由一个带正电荷的质子与一个带正电荷的电子构成
D、由一个带负电荷的质子与一个带负电荷的电子构成
17、下面金属排列顺序,前者能把后者从其盐溶液里置换出来的是( )
A 、Zn、Al、Mg B 、Al、Zn、Fe C 、Ag、Cu、Hg D 、Zn、Hg、 Cu
18、下列各组的三种溶液,只用酚酞试液(组内物质可互相混合),便能鉴别出来的( )
A、 H2SO4 HCl NaCl B、 HCl Ba(OH)2 KOH
C、 H2SO4 NaOH KOH D、 HCl NaCl NaOH
19、列各组仪器中,均标有零刻度的是( )
A、托盘天平和温度计 B、量筒和集气瓶
C、温度计和集气瓶 D、托盘天平和量筒
20.在调节好平衡的托盘天平的两个托盘上,各放一个等质量的烧杯,然后加入等质量、等质量百分比浓度的盐酸,然后二边各放a克锌和铝,反应结束后,烧杯中剩余的铝比剩余的锌多,那么此时天平( )
( A )仍平衡 ( B )放锌的一边重 ( C )放铝的一边重 ( D )无法判断
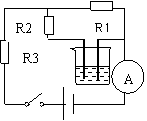 21.如图电源电压为12伏,R1=R2=10欧姆,R3=20欧姆,
21.如图电源电压为12伏,R1=R2=10欧姆,R3=20欧姆,
烧杯中有80克溶质质量分数20%的硫酸铜溶液,若向
烧杯中加入溶质质量分数10%的氢氧化钡溶液171克,
充分反应后,求电流表示数 ( )
(A)0.1A (B)0.2A (C)0.3A (D)0.4A
22.只含C、H或C、H、O的物质充分燃烧后的物质均为H2O和CO2,相同分子数目的①C2H5OH ②CH3OH ③CH4 ④C2H4 分别充分燃烧,所消耗O2的质量相等的是( ) ( A )①③ ( B )②③ ( C )②④ ( D )①④
 二、 填空题:(每空1分,共34分)
二、 填空题:(每空1分,共34分)
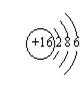
23. 原子是 中的最小粒子。某元素的原子结构示意图为
该元素的原子最外电子层上有 个电子。
24. 用化学符号表示:镁离子 ,+2价的铁元素 ,
 | |||
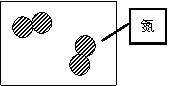 | |||
|
25.TNT是一种烈性炸药,爆炸时发生反应TNT+21O2=====28CO2+10H2O+6N2,则TNT的组成元素分别是 ,其原子个数比 ,相对分子质量 。
26.硒元素具有抗衰老,抑制癌细胞的功能,它的化学性质与硫相似,元素符号为Se,对应的含氧酸的化学式为H2SeO4,这种酸应读作 ,其与氢氧化钠溶液反应的化学方程式为 。
 27.用排水法收集一瓶氢气,如图所示倒置于铁架台上,将一根点燃的蜡烛缓慢的插入集气瓶中,集气瓶口有一团火焰,插入瓶中的蜡烛熄灭了,说明氢气具有
性,不具有
性,该实验操作过程还能说明氢气
,
。
27.用排水法收集一瓶氢气,如图所示倒置于铁架台上,将一根点燃的蜡烛缓慢的插入集气瓶中,集气瓶口有一团火焰,插入瓶中的蜡烛熄灭了,说明氢气具有
性,不具有
性,该实验操作过程还能说明氢气
,
。
28. 写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)煅烧石灰石制生石灰
___________________________________________〔 〕
(2)酒精燃烧的反应
______________________________________________
29. (1)水(H2O)中氢元素与氧元素的质量比是 ;
(2)甲醛(HCHO)中碳元素的质量分数是 ;
(3)某甲醛溶液中氢元素的质量分数为10%,碳元素的质量分数为 。
30.现有白纸、溶质质量分数分别为:(A)10%的NaOH溶液,(B)5%的H2SO4溶液,(C)5%紫色石蕊试液。试设计《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸 画上花,再蘸 画上叶,将白纸挂在墙上,把 向纸上喷即可。实验的化学原理是 。
| (Ⅰ)实验结论 | (Ⅱ)实验方法 | (Ⅲ)实验现象 |
| (1)CaO溶于水后溶液显碱性 | ||
| (2)用消石灰和硫酸铜溶液配制波尔多液时,硫酸铜溶液过量 | ||
| (3)某可燃性气体是CO不是H2 |
31.为了证实(Ⅰ)项 中的结论,请填写(Ⅱ)项中的实验方法和(Ⅲ)项中实验现象。
32.根据下图的溶解度曲线回答:
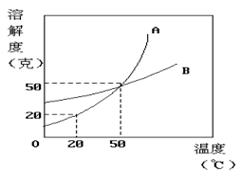 (1)20℃时,A物质的溶解度(填大于、小于、等于)_______B物质的溶解度。
(1)20℃时,A物质的溶解度(填大于、小于、等于)_______B物质的溶解度。
(2)_______ ℃时,两种物质的溶解度相等。
(3)20℃时,将20克A放入50克水中,
可以得到A的饱和溶液_______克。
三、实验题(共16分)
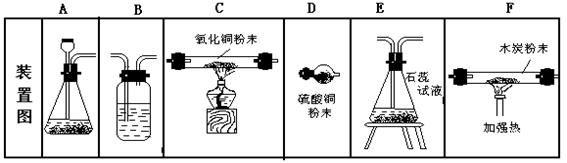 翰林汇3533 . 看图回答下列问题:
翰林汇3533 . 看图回答下列问题:
(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色。判断:①A中产生的气体是__________。C中的氧化铜由_________色,反应前后(用符号填充)______________元素的化合价发生了变化。
②B中用于干燥气体的液体是_________________(填物质名称)。
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编
号(本题2分)。
| 实验 要求 | 制CO | 证明CO | CO | CO还原性 | 除去混和气体 |
| 装置 编号 |
①写出实验室制CO2的化学方程式 。
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液____________。
③除去混合气体中的CO2,应通入(填物质的化学式)___________溶液。
34、现有NaNO3、AgNO3、HCl、Na2CO3、NaCl、Ca(NO3)2六种溶液,仅Ca(NO3)2溶液瓶上贴有标签。为确定其它五种溶液各是什么,将它们随意编号为A、B、C、D、E后,两两混和进行实验,根据实验现象(如下表所示)回答:
| A | B | C | D | E | |
|
| ↓ | ↓ | ↓ | ━ | |
| B | ↓ | ↑ | ━ | ━ | |
| C | ↓ | ↑ | ━ | ━ | |
| D | ↓ | ━ | ━ | ━ | |
| E | ━ | ━ | ━ | ━ |
(1)把由实验现象能确定的A、D、E的化学式填在下表相应的空格中。
A D E
(2)为了确定B、C物质各是什么,还要进行如下实验。填空回答有关问题:
①从已确定的试剂中选用____________作为鉴别试剂最简单。
②向未确定的B、C溶液中分别加入①中选用的鉴别试剂,有白色沉淀生成的原溶液化学式是__________无反应现象的原溶液化学式是__________。
③A+D反应的化学方程式 。
四、计算题(6分)(相对分子质量:NaCl―58.5 Na2CO3―106 HCl―36.5)
35、将氯化钠和碳酸钠的混合物10克,放入盛有100克某稀盐酸的烧杯中,恰好完全反应后,测得溶液的总质量为107.8克。求:
①原混合物中氯化钠的质量分数?
②原稀盐酸中溶质的质量分数?
③所得溶液的溶质质量分数?
扬州中学教育集团 赵铭
模拟1答案
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 答案 | B | C | D | A | A | D | C | D | A | B | A |
| 题号 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| 答案 | B | D | C | A | B | B | D | A | A | D | B |
二、填空题
23.化学变化 6 24.Mg2+ +2 Fe 3Pb 2N2
25. C H N O 7:5:3:6 908
26. 硒酸 H2SeO4 +2NaOH ==Na2SeO4 +2H2O
|
|
28. CaCO3 ====== CaO+H2O 分解反应 C2H5OH +3O2======2CO2 +3H2O
29.1:8 40% 10%
30. B A C 紫色石蕊试液遇酸溶液变红色遇碱溶液变蓝色
31.
| (Ⅰ)实验结论 | (Ⅱ)实验方法 | (Ⅲ)实验现象 |
| (1)CaO溶于水后溶 液显碱性 | 取少量CaO放入试管中,加入适量水溶解,再滴入酚酞试液 | 溶液变红 |
| (2)用消石灰和硫酸铜溶液配制波尔多液时,硫酸铜溶液过量 | 取少量配制的液体,向其中插入一根铁丝 | 铁丝表面覆盖一层红色固体 |
| (4)某可燃性气体是 CO不是H2 | 点燃,将产物通入澄清石灰水中 | 石灰水变白色浑浊 |
32.小于 50℃ 60克
三、实验题
33. (1)①氢气(或H2)、黑色逐渐变成红、Cu,H ②浓硫酸。
(2)AEFCB (3) ①CaCO3+2HCl=CaCl2+CO2↑+H2O
②红色逐渐褪去(或红色逐渐变为紫色)。
③Ca(OH)2
34. (1) AgNO3 NaCl NaNO3 (2) ①Ca(NO3)2 ② Na2CO3 HCl
③AgNO3 +NaCl====AgCl↓+NaNO3
35. 47% 3.65% 9.8%
 A
A