���б�ҵ�ῼ��ѧģ���Ծ���һ��
����
| �⡡�� | һ | �� | �� | �� | �� | �ܡ��� | �Ϸ��� | ������ | |
| ��� |
����ע�⣺���Ծ���������⣬����100�֣�ʱ��90������
�����õ������ԭ��������H��1����O��16����C��12����S��32����Fe��56��Cl��35.5����Cu��64����Na��23
һ. ѡ���⣨ÿС��ֻ��һ����ȷ�𰸣�ÿС��2�֣���50�֡���
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| �� | |||||||||||||
| ��� | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| �� |
1��6000����ǰ�����¾��������µ�������У�������ѧ�仯���ǡ��������� ��������
A���������ݡ�����B. ���ƴ���������C. ĥ��ʯ����������D. ����֯��
2�����и����ʼ����������ʵ������������������仯ѧ���ʵ��ǡ��������������� ��������
A����H2�������B����̿ұ���� C��CO2�������� D��ʯ������
3�������������ڴ�������ǡ����������������������������������������������� ��������
������A������ˮ�������� B��Һ���������������� C���״ס������������� D������
4��ͬ��Ԫ�ص�ԭ�Ӻ����ӣ�һ��������ͬ�ġ��������������������������������� �� �� ��
������A�����Ӳ���������������B�������������� C��������������������D��������
5�������ֲ��Ӫ�����������ص����ʽ���ˮ����ˮ�ʣ����¡�ˮ���������������ڣ�������
��A���ʡ�����B�����ʡ�����C���طʡ����� D�����Ϸ���
6�����;�ˮ�������ƣ�Na2FeO4���У���Ԫ�صĻ��ϼ�Ϊ�������������������� ��������
A��+2�ۡ����� B��+3�ۡ����� C��+5�ۡ��� D�� +6��
7��ũ���о�������귢ׯ�ڡ������������ڷŵ������£������е������͵������������˵�������������������پ������ָ��ӵĻ�ѧ�仯������������ױ�ũ�������յ������Ρ������ׯ��ʩ���ˡ����������� ����������������������������������������������������
A���طʡ����� B���ʡ����� C�����ʡ�������D�����Ϸ�
 |
8����ѧ��Ӧ������Ҫ��һ���������½��С�ͨ�����ƻ�ı䷴Ӧ�������Լӿ졢����������ֹ��Ӧ�Ľ��С����и�ͼ����ӳ�Ĵ�ʩ�У��ܼӿ��仯ѧ��Ӧ���ʵ��ǡ���������������
9��24.5g����غ�5.5g������ػ�ϼ���һ��ʱ���,�Ƶ�ʣ����������Ϊ22.5g�����Ƶ�����������Ϊ���������������������� ��������������������������������������������
A��7.5g������ B��2.0 g��������C��14.1 g������ D��9.6 g��
10�������й���Һ����������ȷ���ǡ������������������������������������� ��������
A����ij���ʵı�����Һ�������ܼ�����ʹ���ʵ��ܽ������
B��������Һ���¶�����������
C��������Һ���������ʣ����Һ�����ʵ���������һ����С
D����һ���¶��£�ͬһ���ʵı�����Һһ���Ȳ�������Һ���ʵ�����������
11��ʵ��������H2��ԭCuO��ʵ��ʱ����ԭ8gCuOʵ��������H2��������������������
A������0.25g���� B����0.25g��������C������0.25g������D������8g
12�������ᴿ��ʵ���У���Ҫ����˳����ȷ���ǡ��������������������������� ��������
������ ��A�����ˡ��ܽ⡢�������� ��B���ܽ⡢����������
������ ��C�������� �ܽ⡢���ˡ� ��D���ܽ⡢���ˡ�����
13��ʳ�Ͱ��Ǽ�ͥ���õ�ζƷ����ȻҲ�������������;��������������Ϊ����ȷ����
���������������������������������������������������������������������� ��������
A������ɴ��պȡʳ�ײ���ͭ���ϵ�ͭ�� �� B����ʳ�׳�ȥ��ˮƿ�е�ˮ��
C���ðƲ�ȥ�����ϵ���ā�� �� ��������D���ðƲ����в˵��ϵ����⡡����
14������һ������Ũ����IJ۹���·����������Ũ�������й©��Ϊ�˲���Ⱦ�Աߵ�ˮԴ�����в�ȡ�Ĵ�ʩ���˵��ǡ��������������������������� �������������� ��������
������A����ˮ��ϴй©��Ũ���ᡡ�������� B������ʯ������й©����Ũ������
C�����Ȼ�������й©����Ũ�����ϡ� D��������й©����Ũ��������
15��̼�����������еĻ�ѧ�����ǣ��ٳ����¶����ȶ����ڳ����¶��ܺ�����ͭ��Ӧ���۸����¶��ܶ�ȡijЩ�����������е��������ڷ�Ӧ�г���Ϊ���������ݶ���һ����Դ��������
������A���٢ڢۡ������� B���٢ۡ�������������C���٢ڢۢݡ������� D���٢ܢ�
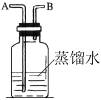 16����ͼ��ʾװ�ã���ϴ������������;��ҽԺ������������ʱ��Ҳ���������Ƶ�װ�á�����˵������ȷ���ǡ�����������������������
����������������������������������������������������������������������������������������������������������������������������
16����ͼ��ʾװ�ã���ϴ������������;��ҽԺ������������ʱ��Ҳ���������Ƶ�װ�á�����˵������ȷ���ǡ�����������������������
����������������������������������������������������������������������������������������������������������������������������
������ ��A��B�������ӹ�����ƿ����������
������ ��B��B�������Ӳ�������������
������ ��C����װ�ÿ������۲��Ƿ����������
������ ��D����װ�ÿ������۲�����������ٶ�
17����һС�����еIJ�������״�Ľ�����Ͷ����з�̪��Һ��ˮ�У��۲쵽�����������п�˵���ƺ�ˮ��Ӧ�ų�����������ǡ������������������������������������� ��������
������A�������Ƹ���ˮ���ϡ�������B���������γ�С��״
������C����������ˮ����Ѹ���ζ���D����Ӧ�����Һ���ֺ�ɫ
18����������������ͭ�����ۣ����뵽ʢ��ϡ������ձ��У���ַ�Ӧ���в�����ʣ�࣬���˺���Һ�к��е������ǡ��������������������������������� ���������� ��������
A��H2SO4�� �� B��FeSO4�� C��FeSO4��CuSO4������ D��H2SO4��FeSO4��
19���������⣨H2O2����MnO2�������·ֽ⣬����ˮ�����������ѹ�������ˮ��Һ���������̡������ơ��Ȼ�þ��Ϻ����ķ�Ӧ�����������л�����Ӧ�����еġ�����������
������A�����Ϸ�Ӧ������������B���ֽⷴӦ�������� C���û���Ӧ��������D�����ֽⷴӦ
20�������������ʱ仯Ҫ��ļ������ǡ����������������������������������� �� �� ��
����![]()
������A��Cu��������B��Na2O��������C��![]() �������� D��CuO ��
�������� D��CuO ��
21��ij��Һ�к� n ��K+��n ��SO![]() ��n��Cl���������ڲ�������H+ ��OH���⣬�����������Ӵ��ڣ������Ʋ����Һ��������������������������������������������
��������
��n��Cl���������ڲ�������H+ ��OH���⣬�����������Ӵ��ڣ������Ʋ����Һ��������������������������������������������
��������
������ ��A��pH > 7������ B��pH = 7�� ����C��pH < 7��������D��pH �� 7����
22��2003��10��15������9ʱ���������������ţ������ػ���о��š����ۡ�������˷ɴ�ֱ�̲���һ�Žۺ�ɫ���������������յĴ�Į���ա��й���һ������̫�մ��������˳�����գ����ͷɴ��ij�������F����ʽ���������ػ���ķ�����������ʡij�о������Ƶġ������Ҫȼ����ƫ�����£���ѧʽΪC2H8N2���������й�ƫ��������ɵ���������ȷ����
��������
������A����2��̼ԭ�ӡ�4���������ӡ�һ������������ɡ���
������B����̼���⡢������Ԫ�����
������C����2��̼ԭ�ӡ�8����ԭ�ӡ�2����ԭ�ӹ���
D�����Ԫ��̼���⡢����������Ϊ1: 4:1
23��19������20����֮��������ѧ�еķ�������͵��ӵ��Ⱥ��֣����������ǵ�����������ԭ�ӵ��ڲ������Ҹ���һ������ʹ�������̽��ԭ�Ӻ˵��ڲ���ɡ�ijѧϰС���ͬѧ�ڹ���ԭ�Ӻ�ԭ�Ӻ˵������У�����������˵����
��ԭ������λ�����ĵ�ԭ�Ӻ˺ͺ��������ɣ�
�ڴ�����ĵ�����ԭ�Ӻ���ռ����ƺ��˶���
��ԭ�ӵ�ȫ������ɺ�ȫ��������������ԭ�Ӻ��
��ԭ�Ӻ��������Ӻ�������ɣ����ӵĸ���һ�����������ӵĸ�����
������������У�����ȷ���ǡ������������������������������������������� ��������
A���٢ڡ���������B���ڢܡ������� C���٢ۡ�������D���ۢܡ�
24��ij�������վȡ�ս��µ���ˮ��ÿ��һ��ʱ��ⶨ��pH���������£�
| �ⶨʱ����� | 0 | 1 | 2 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
�����й�˵������ȷ���ǡ����������������������������������������� ��������
A����ˮ����������B�����������ڿ�����������������������Ⱦ�γɵ�
C��һ��ʱ�����ˮ���Խ����ȶ�����D������ɸ�ʴijЩ������ͽ�����Ʒ
25����֪��Ҳ�ܺ�����������Һ��Ӧ��2Al +2NaOH +2H2O===2NaAlO2+3H2����������������һ�������������������Һ��Ӧ����һ������������ᷴӦ����Ҫ��ȡ������������������������������Ϊ���������������������������������������������������������� ��������
A��1��1�� �� B��1��2�� �� C��2��3������ D��3��2��
��������⣨���21�֣�ÿ��1�֣�
26�������³´�л�����к������������������������������������������ ����������
�������� �����ܻ��ܣ�ʹ����ʯ��ˮ����ǡ�
27������ʯ�ҡ�������̼��ʳ�ηֱ�����ˮ�����εõ�A��B��C������Һ�����ǵ�pH�ɴ�С��˳���ǣ���A��B��C��ʾ����ͬ��___________���ֱ�����������Һ�еμӷ�̪��Һ���Ժ�ɫ����___________��Һ��
28��Ũ�������������ΪA�����ڷ���һ��ʱ������������ΪB����A___________B���>������<����=������ͬ����Ũ���������ΪA�����ڷ���һ��ʱ����������ΪB����A___________B��V1mLˮ��V2mL�ƾ���Ϻ���Һ�����___________��V1+V2��mL��
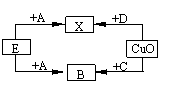 29��A��B��C��D��E�dz�����������ɫ���壬����֮��ת����ϵ��ͼ��ʾ��ͼ�з�Ӧ��������ȥ��X�ڳ�����ΪҺ�壩���������ƶ���ȷ����
29��A��B��C��D��E�dz�����������ɫ���壬����֮��ת����ϵ��ͼ��ʾ��ͼ�з�Ӧ��������ȥ��X�ڳ�����ΪҺ�壩���������ƶ���ȷ����
A�������� ��B�������� ��C����������D�������� ��
30����ͼΪA��B��C���������ʵ��ܽ������ͼ���Իش���������
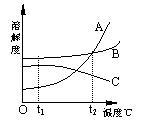 ��1���¶�Ϊt1��ʱ��A��B��C ���������ܽ���ɴ�С
��1���¶�Ϊt1��ʱ��A��B��C ���������ܽ���ɴ�С
��˳��Ϊ������������ ��
��2��t2��ʱA ��B �����ʵ��������� ��� ��
��3����A�л���������B�����Ӵ˻�����з����A�ɲ�ȡ�ķ����� �������������������� ��
31����һ����ĩ�������� NaCl��Na2SO4��Na2CO3��FeCl3��MgCl2 �е�һ�ֻ�����ɡ���������ʵ�飺��ȡ������ĩ����ˮ�ܽ⣬����ɫ����Һ����ȡ����������Һ������������������Һ��������������ȡ������ĩ���μ�ϡ���ᣬҲ�������������ʣ�
������ ��1����ʵ��ٿ�֪��ԭ��ĩ��û��__________�� ʵ��ڿ�˵��ԭ��ĩ��û��_________��
ʵ���֤��ԭ��ĩ��û��____________��
��2����������ʵ�飬�ɵó�ԭ��ĩ�п����е�������________________________��
��3��Ϊ��һ��ȷ��ԭ��ĩ�ijɷ֣�����ͼ��ʾ����ʵ�飺
����[ ��AgNO3��Ba (NO3)2��BaCl2��ѡ�������ΪA��B�Լ�����A��B�������Ӳ�ͬ ]
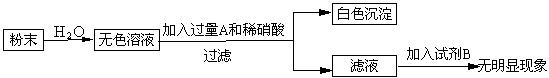
�û�ѧʽ��д����ĩ�ijɷ�__________���Լ�A__________���Լ�B__________��
��������⣨���9��, ÿ��1�֣�
32��Ǧ��Ϊʲô������Ӳ�IJ����?��������ʯī̫��������ʯī����о����������ĥ����ˣ������ϳ���ʯī��ĩ�в���һЩճ����ĩ������Ӳ�ȡ�ճ������Խ�࣬Ǧ�ʾ�ԽӲ���±�Ϊ������ͨǦ�ʵı�ż���оԭ�ϵ���ȣ�
| ��� ԭ����� | 2H | H | HB | 2B |
| ʯī(��������)% | 74.0�� | 75.2�� | 81.3�� | 85.5�� |
| ճ��(��������)% | 26��0�� | 24��8�� | 18��7�� | 14��5�� |
�Իش��������⣺
(1)�ϱ���Ӳ������Ǧ����(����)���� ��������������������
(2)���о�ʯī����һ����;������������������������ ��
 33����1��ú��һ�ֳ��õĻ�ʯȼ�ϣ���ͥ��ú�����˴ӡ�ú��������ú���ı仯����ǰ���ǰ�ú�ۼӹ����Դ���ƹ��������壬�������ǰ�ú�ۼӹ���Բ���壬����Բ�����ڴ���һЩ��(����ͼ)������������ֱ仯���ŵ��ǣ���������������������������������
��ú��ȼ��ʱ�����������Ⱦ�Ϊ�˼���úȼ��ʱ�Ի�������Ⱦ�����跨��úת��������ȼ�ϡ���ˮ����ͨ�����ȵ�ú����ƵýϽྻ��ˮú��(��Ҫ�ɷ���CO��H��)������д���÷�Ӧ�Ļ�ѧ����ʽ������������
����
33����1��ú��һ�ֳ��õĻ�ʯȼ�ϣ���ͥ��ú�����˴ӡ�ú��������ú���ı仯����ǰ���ǰ�ú�ۼӹ����Դ���ƹ��������壬�������ǰ�ú�ۼӹ���Բ���壬����Բ�����ڴ���һЩ��(����ͼ)������������ֱ仯���ŵ��ǣ���������������������������������
��ú��ȼ��ʱ�����������Ⱦ�Ϊ�˼���úȼ��ʱ�Ի�������Ⱦ�����跨��úת��������ȼ�ϡ���ˮ����ͨ�����ȵ�ú����ƵýϽྻ��ˮú��(��Ҫ�ɷ���CO��H��)������д���÷�Ӧ�Ļ�ѧ����ʽ������������
����
���������������������������������� ��ú�������ڼ���ˮú�����������������������ζ�����壬��Ŀ�������������������������������������� ��
��2��ijͬѧ��ʵ������з����������ƹ���¶���ڿ�����һ��ʱ������˳��⣬���ڼ���Ҳ�����ֹ������ܳ����������Щ����˵���˿����к������������� ��������������ѧ֪ʶ��������˵�������к����������ʣ����������������������������� ��
���������������������������� ��
�ġ�ʵ���⣨���11�֣�
34����4�֣�����ƿ��ɫ���壬���Ƿֱ��Ƕ�����̼���������ж��ַ����ɽ�����������������ģ��ʾ��Ҫ���о����ּ�����
������ ʾ�����ô����ǵ�ľ���ֱ����ƿ���£���ȼ����������Ϩ����Ƕ�����̼��
����1��______________________________________________________________________
����2��______________________________________________________________________
35���±��ǿ����е�����ɷֺ��������������ɷֺ������ձ���
| ����ɷ� | ���� | ���� | ������̼ | ˮ | �������� |
| �����е����壨%�� | 78 | 21 | 0.03 | 0.07 | 0.9 |
| ���������壨%�� | 78 | 16 | 4 | 1.1 | 0.9 |
����ijУ�о���ѧϰС���ͬѧ����˼�ʵ�鷽������֤��������������������ɷֵĺ�����ʲô��ͬ������Ҫ������������ͼ��ʾ��
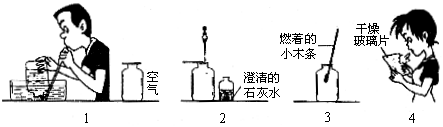
����������ͼʾ����Ҫʵ��������輰��֤���������±��У�
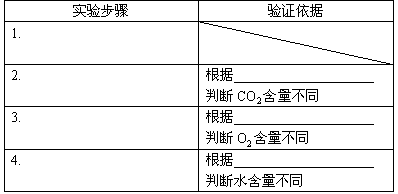
�塢�����⣨���9�֣�
36��3�֣����á�������=��������������д���пհס�
��1������������ag����ͭ��Һ�У���Ӧһ���ȡ������Һ������Ϊbg����a���� b��
��2��mg KclO3������ȫ�ֽ��agO2��mgKMnO4������ȫ�ֽ��bgO2����a������b��
��3��ȡ���������ֱ�Ϊag��bg��пƬ��һ�������������ᷴӦ����һ�����������ᷴӦ�������ɵ�������H2����a���� b��
37��6�֣�����ͬѧΪ�˲ⶨ��������̼��Ƶ���������, ��ȡ 5.55g ����ĺ������ĩ�������Ĵθ��¼��ȣ����ʲ��μӷ�Ӧ������ȴ������ʣ�������ظ���������¼�������£�
| �������� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ʣ�����������g�� | 4.25 | 3.95 | 3.35 | 3.35 |
����㣺
��1����ȫ��Ӧ�����ɶ�����̼________________________g��
��2��������̼��Ƶ�����������
�����
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| �� | B | C | B | C | B | D | C | C | A | D | A | D | D |
| ��� | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| �� | B | B | A | C | B | C | D | C | B | A | A | A |
26��N2 �����ܡ� 27��![]() �� 28��
�� 28��![]()
29��A��O2��B��CO2�� C��CO�� D��H2
30��1��B>C>A������2�� �ܽ�ȡ��� ��3�����½ᾧ����ᾧ��
31����1��FeCl3��MgCl2��Na2CO3 ���� ��2��NaCl��Na2SO4
������ ��3��Na2SO4��Ba(NO3)2��AgNO3��NaCl�� AgNO3��Ba(NO3)2
32��(1)2H��(2)�������缫
33����1��ʹú������ĽӴ��������ȼ�ո�Ϊ��֡� C+H2O![]() CO+H2
CO+H2
���ڼ��緢��ú���Ƿ�й©
��2��ˮ����ˮ����ͭ¶���ڿ�����һ��ʱ���������� ���糿��Ҷ�ϳ���¶��
34��(ÿ��2�֣���
����1���ֱ������������ʯ��ˮ�����л��Dz�������CO2���������������O2��
����2���ֱ����������ɫʯ����Һ������Һ������CO2���������������O2��
����3����ϸ��ϵС����Ͷ��ƿ�У���Ϣ��������CO2����Ȼ��������O2��
35��7�֣�
������1������ˮ�������ռ���ƿ���������壬���ռ���ƿ������1�֣�
������2���������ʯ��ˮ�ֱ����ʢ�к���������Ϳ����ļ���ƿ�У�����ʯ��ˮ���dz̶ȵIJ�ͬ�ж�![]() ������ͬ��2�֣�
������ͬ��2�֣�
������3����ȼ�ŵ�ľ���ֱ����ʢ�к���������Ϳ����ļ���ƿ�У�����ľ��ȼ������IJ�ͬ�ж�![]() ������ͬ��2�֣�
������ͬ��2�֣�
������4��ȡ�������IJ���Ƭ���������е�һ����������ݲ���Ƭ��ˮ���IJ�ͬ�ж�ˮ������ͬ��2�֣�
36����1������ ��2�������� ��3��=
37����6�֣��⣺��1��2.2���������������������������������������������������� 2��
|
CaCO3====CaO+CO2��
100������������ 44
x���������������� 2.2g
![]()
�� x=5g���� �������������������������������������������������� 2��
��������̼��Ƶ�����������![]() ��100%��90.1% �������� 2��
��100%��90.1% �������� 2��