初三化学第一学期期中考试
试卷
可能用到的相对原子质量:H:1、C:12、N:14、O:16、Na:23、Mg:24、Al:27、P:31、S:32、Cl:35.5、K:39、Fe:56、Cu:64、Zn:65
第Ⅰ卷(选择题 共40分)
注意:1~20小题每题只有1个选项符合题意,21~25小题每题有1~2个选项符合题意。请将其序号填入下表答案栏内:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 | C | A | C | C | B | D | A | C | B | A | C | D | A | B | A |
| 题号 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| 答案 | B | D | D | C | B | BD | AB | D | A | CD |
一、选择题(本题共20小题,每小题只有1个选项符合题意,请将其序号填入卷首相应答案栏内。每小题1.5分,共30分。)
1.通过化学的学习,我们知道化学在人类社会发展中起着重要的作用。请你分析下列四个选项中不属于化学学科研究的是
A.开发新型能源 B.合成新的物质
C.空间形式和数量关系 D.防治环境污染
2.下列说法中正确的是
A.含有氧元素的化合物可能不是氧化物 B.在化学反应中原子不可分,离子也不可分
C.具有相同质子数的粒子一定是同种元素 D.分子保持一切物质化学性质的最小粒子
3.下列词语可用来概括描述物质的某些性质,其中均属于物理性质的是
A.还原性 氧化性 B.可燃性 稳定性
C.溶解性 挥发性 D.活动性 吸水性
4.下列各组物质中,前一种为混合物后一种为单质的是
A.冰水混合物 水 B.水银 氮气
C.新鲜的空气 硫磺 D.氧化镁 液态氧
5.NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条件下极易与氧气反应。实验室收集NO的装置是
 |
A B C D
6.人类生活需要能量,下列能量主要由化学变化产生的是
A.电灯通电发出的光 B.电熨斗通电发出的热量
C.水电站利用水力产生的电能 D.液化石油气燃烧放出的热量
7.下列粒子中,不能保持物质化学性质的是
A.H B.O2 C.Fe D.CO2
8.在O2、CO2、KClO3三种物质中,下列说法正确的是
A.都含有氧分子 B.都含有氧原子 C.都含有氧元素 D.都含有氧离子
9.在化学反应“2H2+O2![]() 2H2O ”中,肯定发生了变化的是
2H2O ”中,肯定发生了变化的是
A.元素的种类 B.元素的化合价 C.物质的总质量 D.原子的数目
10.下列物质在氧气中燃烧,火星四射,生成黑色固体的是
A.铁 B.硫 C.磷 D.镁
11.为了进一步优化城市环境,某同学提出了如下建议:①使用无磷洗衣粉;②使用无铅汽油;③禁止焚烧秸杆;④禁止燃放烟花爆竹;⑤分类回收垃圾;⑥提倡使用一次性发泡塑料餐具和塑料袋。上述建议中不可采纳的是
A.③ B.② C.⑥ D.⑤
12.天然气的主要成分是甲烷,其化学式为CH4,下列四位同学在讨论化学式CH4的意义,其中错误的是
 | |||||||
 | |||||||
 | |||||||
 | |||||||




A B C D
13.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示:
| 物质 | A | B | C | D |
| 反应前的质量/g | 35 | 2 | 24 | 15 |
| 反应后的质量/g | 待测 | 64 | 0 | 10 |
试判断该密闭容器中发生反应的化学反应基本类型为
A.化合反应 B.分解反应
C.置换反应 D.无法判断
14.在饮用水中常添加含钙、镁、锌、硒的矿物质,可以改善人体营养增强体质。其中“钙、镁、锌、硒”是指
A.单质 B.元素 C.原子 D.离子
15.在原子结构中,决定元素种类的是
A.质子数 B.相对原子质量 C.中子数 D.最外层电子数
16.在下列物质中,硫元素的化合价最低的
A.S B.Na2S C.SO2 D.K2SO4
17.运载飞船的火箭常用液态肼(N2H4)和液态双氧水(H2O2)作推进剂,若它们充分混合反应的化学方程式为:N2H4+2H2O2==X+4H2O,则X的化学式为
A.H2 B.O2 C.NH3 D.N2
18.化学实验应遵循一定的操作顺序,这对实验结果、实验的顺利完成乃至师生安全等都具有十分重要的意义。下列对有关化学实验中先后操作顺序的叙述错误的是
A.实验室制取氢气时,应先检查装置的气密性后装药品
B.进行氢气的性质实验时,应先验纯后进行点燃或还原氧化铜的实验
C.实验室制取氧气用排水法收集氧气完毕时,应先将导管从水槽中取出后熄灭酒精灯
D.氢气还原氧化铜实验结束时,应先停止通氢气后停止加热
19.现有一不纯的锌样品6.5g,加入足量的稀盐酸充分反应后生成了氢气0.21g。则该样品中含有的杂质不可能是
A.铁 B.镁
C.铜 D.铝
20.现有Zn、Mg、Al的混合物若干克,与196g稀硫酸(其中硫酸的质量分数为10%)恰好完全反应,则反应中生成氢气的质量是
A.0.2g B.0.4g
C.4g D.无法计算
二、选择题(本题共5小题,每小题有1~2个选项符合题意,请将其序号填入卷首相应答案栏内。每小题2分,共10分。)
21.某物质经分析只含有一种元素,则下列对该物质的说法中正确的是
A.一定是纯净物 B.一定不是化合物
C.一定是单质 D.可能是混合物
22.化学知识中有很多的“相等”,下列有关“相等”的说法中正确的是
A.参加化学反应的物质的质量总和等于反应后生成的物质的质量总和
B.化合物中元素化合价的正价总数等于负价总数
C.在原子中原子核内的质子数等于中子数
D.在置换反应中,两种反应物的质量比等于两种生成物的质量比
23.氢能源是一种极其理想的新能源,是因为氢气燃烧放出的热量大,且生成物不污染环境。但氢气作为能源目前还不能被广泛使用,分析其原因,下列说法中错误的是
A.虽然制氢气的资源丰富,但制取成本高
B.高效、经济的制取氢气的方法还在研究之中
C.高效、价廉的贮氢材料还在研究之中
D.氢气的化学性质很活泼,常温下就会发生爆炸
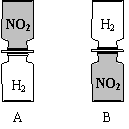 24.把分别充满红棕色二氧化氮(NO2)气体和氢气的集气瓶按下图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需要很长时间才能达到同样的效果。由此现象不能得出的结论是
24.把分别充满红棕色二氧化氮(NO2)气体和氢气的集气瓶按下图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需要很长时间才能达到同样的效果。由此现象不能得出的结论是
A.分子由原子构成
B.分子间有间隔
C.二氧化氮的密度比氢气大
D.分子是不断运动的
25.将H2和O2 组成的混合气体4g置于密闭的容器中,经电火花引燃,使之充分反应得到1.8g水蒸气,则反应前混合气体中,H2和O2的质量比可能为
A.1∶1 B.1∶3
C.1∶19 D.3∶2
第Ⅱ卷(非选择题 共60分)
三、填空题(本题共7小题,共27分。)
|
|
27.(4分)物质的性质决定物质的用途,物质的用途反映物质的性质。下列图示形象地表示了氢气的部分用途,请在下表中对应填写氢气用途的代号和与用途对应的具体性质。
 氢气的用途:a.充氢气球;b.作高能燃料;c.制备金属材料;d.合成氨。
氢气的用途:a.充氢气球;b.作高能燃料;c.制备金属材料;d.合成氨。
| 图示 | 用途 | 性质 |
| ⑴ | c | 还原性 |
| ⑵ | a | 密度小 |
| ⑶ | b | 可燃性 |
上述图示中还能表示氧气用途的是 ⑶ (填图示编号)。
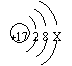 |
28.(2分)某原子的结构示意图为 ,则该原子的核电荷数为 17 ,核内质
子数为 17 ,核外电子分 三 层排布,它的最外层电子数X= 7 。
29.(2分)碳酸氢铵(俗称碳铵,化学式为NH4HCO3)是一种常用化肥,生产厂家有下面使用说明:“本品宜存贮于干燥阴冷处,防止受潮,施用后盖土或立即灌溉,避免曝晒或与碱性物质(如熟石灰)混合使用,以免变质,造成肥效损失。”请回答:
⑴碳铵中含有的氮元素是农作物生长所需要的营养元素,它能促使作物的茎、叶生长茂盛,叶色浓绿。碳铵中氮元素的化合价为 -3 价。
⑵根据碳酸氢铵的使用说明,你能得出碳酸氢铵具有的性质是(至少写出物理、化学性质各一点) 易溶于水,不稳定(或受热、见光易分解,能跟碱性物质发生反应等) 。
30.(4分)2003年12月23日,重庆市某天然气井发生井喷事故,喷出的天然气中H2S气体的含量很高,H2S气体有臭蛋气味,密度比空气大,有剧毒。井喷发生不久,附近的村民就闻到了臭蛋气味,这体现了分子 不断运动 的性质;当村民们得知这种臭气有剧毒时,迅速撤离村庄,远离井喷地点。为了减少中毒机会,村民在撤离井喷地点时应发行量往高处走的原因是 H2S 的密度比空气大 ;技术人员通过原有的H2S放喷管线,成功点燃了地下喷出的H2S气体,使气体不再扩散,此时H2S燃烧生成了一种淡黄色的固体和水,试写出该反应的化学方程式 2H2S+O2== 2S+2H2O 。
31.(8分)下面图示中表示的是我们已经学过的某些物质之间,在一定的条件下可实现的转化。
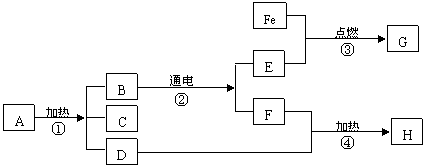 |
若A为绿色粉末、D为黑色粉末、H为红色固体,试回答下列问题:
⑴写出有关物质的名称:A 碱式碳酸铜 、C 二氧化碳 、
F 氢气 、G 四氧化三铁 ;
⑵写出有关反应的化学方程式,并指出所属反应的基本类型:
① ( 分解反应 )、
② ( 分解反应 )、
③ ( 化合反应 )、
④ ( 置换反应 )。
32.(3分)现有一混合气体,只由碳和氧两种元素组成,若其中碳和氧两种元素的质量比为3∶5,则该混合气体的可能组成有:① 、 ;② ;③ 。
四、简答题(本题共2小题,每小题3分,共6分。)
33.在加油站和一些公共场所常有如下图所示的警告标志,请你指出这是一个什么标志并说出它在这些地方的不同意义。
 答:这一个“禁止吸烟”的标志。
答:这一个“禁止吸烟”的标志。
在加油站:是从安全角度考虑的,防止发生火灾或爆炸。
在公共场所:是从环境保护角度考虑的,防止香烟燃烧产生有害气体污染空气,损害人们的健康。
34.将四种金属Mg、Zn、Fe、Cu各一小块分别投入盛有等质量等浓度的稀硫酸的试管中,试管依次标号为①、②、③、④。实验中有关现象如下表:
| 试管编号 | ① | ② | ③ | ④ |
| 现 象 | 反应快 有气体产生 | 反应较快 有气体产生 | 反应较慢 有气体产生 | 不反应 无气体产生 |
分析上述实验,可以得出许多结论。请写出你能归纳出的两个结论:
⑴ 并不是所有的金属都能跟稀硫酸反应 ;
⑵ 不同的金属与稀硫酸反应的速度不同 。
五、实验题(本题共3小题,每个空格1分,共15分。)
35.下列实验操作错误的是 A 。
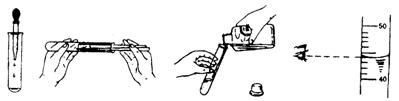
A B C D
36.实验室制取气体的实验中,较为重要的一项内容就是需要研究和设计制取气体的发生装置。研究和设计制取气体的发生装置时常需考虑 反应物状态 和 反应条件 两方面的因素。比较实验室制取氢气和制取氧气在这两方面的不同,若将实验室制取氧气的发生装置变为制取氢气的装置,至少应进行的两点改进是:⑴ 去掉酒精灯 ;⑵ 将试管口竖直向上 。为了方便地加入酸液,还应使用的仪器是 长颈漏斗 。
37.在一次化学兴趣小组活动中,老师拿出两瓶无标签的试剂,分别是固体和液体,他取了少量的的两种试剂在试管中混合,立即产生一种无色气体。请你一起参加他们的探究:
⑴①此气体是什么物质?验证它们的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是 氢气 | 用拇指堵住试管口一会儿,然后点燃该气体。 | 产生淡蓝色火焰或听到爆鸣声,证明是氢气。 |
产生此气体的化学方程式可能是 Zn+H ↑ 。
②制取该气体,采用的发生装置可选取下图中的 B (填序号),收集装置是 D或E 。
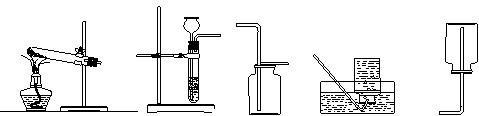 |
A B C D E
 ③如用右图所示装置收集该气体,气体由
b 端(填“a”或“b”)通入。(注:以上答案应与猜想的气体相对应)
③如用右图所示装置收集该气体,气体由
b 端(填“a”或“b”)通入。(注:以上答案应与猜想的气体相对应)
⑵你还猜想此气体可能是 氧气 ,生成这种气体的化学方程式可能是 2H 。
六、计算题(本题共3小题,第38、39小题各3分,第40小题6分,共12分。)
38.磷酸二氢钾(KH2PO4)应用于我国研制的巨型激光器“神光二号”中。试计算:
⑴磷酸二氢钾的相对分子质量为 136 ;
⑵磷酸二氢钾中磷和氧的质量比为 31∶64 ;
⑶磷酸二氢钾中钾元素的质量分数。(28.7%)
39.某同学为了研究实验室中用某氯酸钾样品制氧气的有关问题,他将5g该样品与1g二氧化锰混合,加热该混合物(假设杂质不参加反应),在不同时间测得有关数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 5.04 | / | 4.08 | / |
| 生成氧气的质量/g | / | 1.84 | / | 1.92 |
⑴加热t3时间后氯酸钾是否已经完全反应?____是____(填“是”或“否”),此时二氧化锰的质量为 1 g。
⑵该样品中氯酸钾的质量分数为 98% 。
40.某学生用一种不纯的锌粒和稀硫酸反应,共做了五组对比实验,实验结果记录如下表:
| 实验序号 | 加入锌粒的质量/g | 稀硫酸的体积/mL | 生成硫酸锌的质量/g |
| 1 | 1.5 | 40.0 | 3.22 |
| 2 | 3.0 | 40.0 | m |
| 3 | 4.5 | 40.0 | 9.66 |
| 4 | 6.0 | 40.0 | 10.80 |
| 5 | 7.5 | 40.0 | n |
⑴上表中,m= 6.44 g,n= 10.80 g;
⑵上述五组对比实验中,反应后硫酸有剩余的是 1、2、3 (填实验序号);
⑶计算所用锌粒的纯度。(86.7%)
初三化学参考答案
第Ⅰ卷(选择题 共40分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 | C | A | C | C | B | D | A | C | B | A | C | D | A | B | A |
| 题号 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| 答案 | B | D | D | C | B | BD | AB | D | A | CD |
第Ⅱ卷(非选择题 共60分)
三、填空题(本题共7小题,共27分。)
26.(4分)⑴2Cl2 ⑵2Mg2+ ⑶NH4+ ⑷FeCl2
27.(4分)c 还原性 a 密度小 b 可燃性 ⑶
28.(2分)17 17 三 7
29.(2分)-3 易溶于水,不稳定(或受热、见光易分解,能跟碱性物质发生反应等)
30.(4分)不断运动 H2S
的密度比空气大 2H2S+O2![]() 2S+2H2O
2S+2H2O
31.(8分)⑴A、碱式碳酸铜 C、二氧化碳 F、氢气 G、四氧化三铁
⑵①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O 分解反应 ②2H2O
2CuO+CO2↑+H2O 分解反应 ②2H2O![]() 2H2↑+O2↑ 分解反应 ③3Fe+2O2
2H2↑+O2↑ 分解反应 ③3Fe+2O2![]() Fe3O4 化合反应 ④H2+CuO
Fe3O4 化合反应 ④H2+CuO![]() Cu+H2O 置换反应
Cu+H2O 置换反应
32.(3分)①CO、CO2 ②CO、O2 ③CO、CO2、O2
四、简答题(本题共2小题,每小题3分,共6分。)
33.这一个“禁止吸烟”的标志。在加油站:是从安全角度考虑的,防止发生火灾或爆炸。
在公共场所:是从环境保护角度考虑的,防止香烟燃烧产生有害气体污染空气,损害人们的健康。
34.⑴并不是所有的金属都能跟稀硫酸反应;⑵不同的金属与稀硫酸反应的速度不同。(或其他合理答案)
五、实验题(本题共3小题,每个空格1分,共15分。)
35.A
36.反应物状态 反应条件 去掉酒精灯 将试管口竖直向上 长颈漏斗
37.⑴①氢气 用拇指堵住试管口一会儿,然后点燃该气体。 产生淡蓝色火焰或听到爆鸣声,证明是氢气。 Zn+H2SO4==ZnSO4+H2↑ ②B D或E ③b(注:以上答案应与猜想的气体相对应)
⑵氧气 2H2O2
![]() 2H2O+
O2↑(或其他合理答案)
2H2O+
O2↑(或其他合理答案)
六、计算题(本题共3小题,第38、39小题各3分,第40小题6分,共12分。)
38.⑴136 ⑵31∶64 ⑶28.7%
39.⑴是 1 ⑵98%
40.⑴6.44 10.80 ⑵1、2、3 ⑶86.7%