![]()
|
|
学科:化学 |
| 教学内容:二氧化碳的实验室制法 |
【基础知识精讲】
1.反应原理:常用大理石(或石灰石)与稀盐酸起反应制得.
CaCO3+ 2HCl= CaCl2+ CO2↑十 H2O
注意:(1)不能用浓盐酸,因为浓盐酸易挥发出HCl气体,使制得的CO2不纯.
(2)不能用硫酸代替稀盐酸,因为反应生成的CaSO4微溶于水,覆盖在大理石(或石灰石)表面,使反应难以进行.
(3)不能直接用CaCO3粉末,因为反应速度太快,不适宜实验室制取气体.
2.反应装置:前面已学过了氧气、氢气的实验室制法,有了一定的实验设计思路,由于实验室制CO2为“固十液”不加热型,因此,其发生装置与制H2相同.
3.收集方法:因为CO2能溶于水,且密度比空气大,所以一般采用向上排空气法收集.
4.验满:用燃着的木条放在集气瓶口,如果火焰熄灭,证明已收集满.
5.二氧化碳的灭火原理:CO2既不能燃烧,也不能支持燃烧,而且密度又比空气大,能使物体跟空气隔绝而停止燃烧.
常用灭火器种类:泡沫灭火器、干粉灭火器和液态CO2灭火器.
【重点难点解析】
例1 实验室制备CO2,可选择的试剂组是( )
A.石灰石和稀盐酸 B.碳和氧化铜
C.大理石和稀硫酸 D.碳酸钠和稀盐酸
分析 实验室制气体选择试剂的原则:(1)原理正确;(2)原料易得,物美价廉;(3)操作简便,易于收集,(B)的反应要在高温进行,操作不便,(C)反应后有微溶物CaSO4生成,它覆盖在大理石表面,阻碍反应进行,(D)反应过于剧烈,不便收集。
解答 选(A)
例2 下列气体中,既能用排水法收集,又能用向下排空气法收集的是( )
A. 氧气 B.氢气 C.二氧化碳 D. 氯气
分析 既能用排水法收集,又能用向下排空气法收集的气体,必须具备难溶于水且密度比空气小的性质,同时满足这一性质的气体只有氢气.
解答 选(B)
例3 如图5-8是某同学设计的制取纯净、干燥二氧化碳气体的装置.回答:
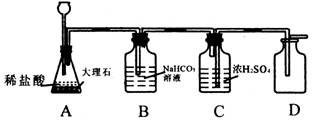
图 5-8
(1)指出图中的错误,并说明可能造成的不良后果?
(2)写出A中发生反应的化学方程式
(3)B中NaHCO3溶液的作用是 ,能否换成NaOH溶液 (填能或不能);C中浓H2SO4的作用是 .
( 4 )B、C顺序能否交换 .
分析 B、C均为洗气装置,气体顺利流动,导管要“长进短出”,显然C有错误.排空气法收集气体,其导管均应插入集气瓶底部,这样有利于空气的排出,D有错误.除杂质时,主要物质不能与洗气瓶中的物质发生反应,故不能用 NaOH(2NaOH+CO2=NaCO2+ H2O). B、C顺序不能变,否则除去水蒸气的气体通过B时又会带来水蒸气。
解答 (1)C中导管没按“长进短出”装配,气体无法流动,D中导管末插入集气瓶底部,不便空气排出,难以收集满纯净的CO2.
(2)CaCO3+ 2HCl= CaCl2十CO2 + H2O
(3)除少量HCl气体;不能.除水蒸气
(4)不能
例4 为测定某石灰石样品中碳酸钙的质量分数,取22.2g石灰石样品,放入盛有146g稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸均恰好反应(杂质不反应),放出气体,燃杯内物质质量变为159.4g.求(1)石灰石中碳酸钙的质量分数;(2)盐酸的质量分数.
分析 22.2g石灰石中除CaCO3外,还会有杂质; 146g稀盐酸中溶质 HCl
的质量未知;159.4g是 CaCl2溶液与未及应的杂质的质量和,均不能直接作为计算的依据.但从题意分析可知,原石灰石与盐酸的质量和减去最后烧杯内物
质的质量为反应中产生CO2的质量.
解 “设石灰石中CaCO3的质量为x,盐酸中含HCl的质量为y
CO2的质量为:146g+ 22. 2g- 159. 4g=8.8g
CaCO3+ 2HCl= CaCl2+CO2↑十 H2O
100 73 44
x y 8.8g
![]() =
=![]()
![]() =
=![]()
解得 x= 20g y=14.6g
所以 CaCO3的质量分数=![]() ×100%=90.1%
×100%=90.1%
盐酸的质量分数 = ![]() ×100% = 10%
×100% = 10%
答:略
【典型热点考题】
例1 硫化亚铁是一种黑色块状固体,把稀硫酸滴在硫化亚铁的表面,会产生硫化氢气体,实验室常用这个反应来制取硫化氢气体.硫化氢是无色有臭鸡蛋气味的气体,它的密度比空气大,能溶于水,水溶液叫氢硫酸.
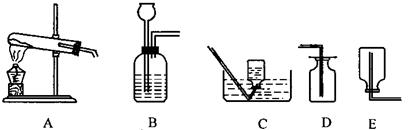
图5-9
(1)制取硫化氢。应选用图5-9所示的 装置(填代号,下同);收集硫化氢时应选用图5-9所示的 装置.
(2)硫化氢气体可以燃烧,当氧气不充分时,燃烧产物是单质硫和水,其化学方程式为 .
分析 实验室选择制备气体的装置,应根据反应物的状态和反应条件等因素确定,该实验属“固 + 液”不加热型,其发生装置与制H2、CO2相同;气体的收集方式取决于气体的密度和水溶性.
解答 (1)B;D (2) 2H2S +
O2![]() 2S↓+ 2H2O
2S↓+ 2H2O
例2 怎样用最简单的方法检验某固体物质中有含碳酸根的化合物?
分析 仅通过加稀盐酸观察有无气体产生来判断碳酸根的存在是不严密的,因为一些较活泼的金属(如Zn)也可与盐酸及应产生气体,所以还要用澄清的石灰水来证明产生的气体为二氧化碳.
解答 取少量固体物质于试管中,加入适量稀盐酸,并将产生的气体通入足量的澄清石灰水中,如果澄清石灰水变浑浊,则说明固体物质中含有碳酸根的化合物.

【同步达纲练习】
一、选择题
1.为了证明鸡蛋壳的主要成份含有碳酸根离子,向鸡蛋壳上滴加的药品是( )
A. 稀盐酸 B.氯化钠溶液 C.石蕊试液 D.硫酸溶液
2.实验室制取二氧化碳一般有五个步骤:①检查装置的气密性;②按要求装配好仪器;③向漏斗中注入酸液;④向广口瓶中放入小块的大理石;⑤收集气体.下列操作顺序正确
的是( )
A.①②③④⑤ B.②①④③⑤. C.①④②③⑤ D.②③④①⑤
3.各取一定质量的碳酸钙和碳酸镁,分别与足量的盐酸反应,若要使两个反应生成的二氧化碳的质量相等,则所取碳酸钙与碳酸镁的质量比是( )
A.1∶1 B.50∶21 C.25∶21 D.21∶25
4.检验集气瓶中的二氧化碳是否收集满的方法是( )
A. 将燃着的木条伸入集气瓶内 B.将带火星的木条伸入集气瓶内
C.将少量石蕊试液注入集气瓶内 D.将燃着的木条放在集气瓶口
5.欲证明生石灰中含有石灰石,最简单的方法是( )
A. 加热 B.加水,通入CO2 C.加碳酸钠溶液 D.滴加稀盐酸
6.质量相同的CaCO3、Na2CO3 、K2CO3分别与足量的盐酸反应,放出的气体( )
A.一样多 B.CaCO3最多 C.Na2CO3最多 D.K2CO3 最多
7.实验室制取CO2时,应选用的一组仪器是( )
A.锥形瓶、集气瓶、导管、水槽
B.长颈漏斗、锥形瓶、导管、集气瓶、酒精灯
C.分液漏斗、导管、锥形瓶、集气瓶
D.广口瓶、集气瓶、导管、酒精灯
8.欲除去热水瓶胆内壁附着的水垢(主要成份是碳酸钙),可采用的办法是( )
A. 加热 B. 用砂子擦洗 C.加稀盐酸浸洗 D.加碳酸浸洗
9.植物的光合作用可以表示为:CO2 + H2O→淀粉 + O2由此判断生成的淀粉中一定含有的元素是( )
A.碳、氢、氧元素 B.碳、氧元素 C.碳、氢元素 D.氢、氧元素
二、填空题
10.在通常情况下,一氧化氮是一种难溶于水的无色气体,它的密度跟空气相近.一氧化氮很容易限空气中的氧气化合,生成红棕色的二氧化氮气体.
(1)实验室里,一氧化氮气体可用 法收集.
(2)一氧化氮跟氧气反应的化学方程式是 .
(3)二氧化氮是红棕色的气体,这是二氧化氮的 性质.
11.某学生利用一支底部有破洞的试管和一个广口瓶组装成制取二氧化碳的发生装置(如图5-10所示),在铜网上应盛放 ,广口瓶中应盛有 .若将铜网换成铁网,那么产生的后果是 ,其原因是(用化学方程式表示) .
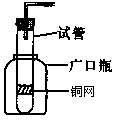
图5-10
三、计算题
12.含杂质(杂质不参加反应)10%的大理石250克与足量盐酸反应,可生成CO2多少g?在标准状况下这些CO2的体积是多少升?(CO2的密度为1.977克/升)
【素质优化训练】
13.做如下实验,步骤为:①用食醋将鸡蛋泡至蛋壳变软;②向一个瓶口比鸡蛋略小的广口瓶中投入燃着的酒精棉球;③迅速将鸡蛋小头对准广口瓶的瓶口,可观察到什么现象?解释发生此现象的原因.
14.实验室制取CO2气体时,若反应物之一是浓盐酸,那么把制得的CO2气体通入澄清石灰水中,可能会出现什么现象?为什么?
15.盛满石灰水的瓶子敞开放久了,瓶内壁就会出现一层白色固体物质,该物质(化学式)是 ,其形成的化学反应方程式为 .可用 。除去,其化学方程式为 。
【生活实际运用】
16.钙是人体必需的元素,缺钙会造成骨骼和牙齿脆弱.当从食物中不足以得到人体所需的钙时,就要用含钙的药品来“补钙”.下列物质中,可以作为补钙药品的是( )
A.CaCO3 B.CaO C. Ca( OH)2 D. Ca
17.家庭中洗涤热水瓶内少量的水垢,实际可行的方法是( )
A.用稀盐酸洗涤 B.用食用白醋洗涤
C.用热碱水洗涤 D.用食盐水洗涤
【知识验证实验】
鸡蛋壳的主要成份是 ,某同学用鸡蛋、稀盐酸和大玻璃筒做了如下实验:将一个鸡蛋放入盛有稀盐酸的大玻璃筒中,鸡蛋沉到筒底,其表面产生气泡并有部分气泡附着在鸡蛋表面,过了一会儿,鸡蛋徐徐上升.这个实验用白醋代替稀盐酸也能完成,你也不妨试一试.
(1)清简述鸡蛋徐徐上升的原因.
(2)请写出碳酸钙跟盐酸反应的化学方程式.
(3)请举出两个例子,说明类似(2)中反应原理在实际生活中的应用.( 2001年北京市中考题)
【知识探究学习】
化学与生活:化学与生活紧密相连,生活的方方面面都离不开化学,学习化学知识,可以有效地解决一些生活中的难题.
例如,阅读下列短文:
近几年来,很多科学家在研究和讨论直接威胁人类生存的地球逐渐变暖的问题,这个问题已引起了越来越多的人们的注意.随着工业生产的发展和人类生活水平的提高,煤、石油、天然气等矿物燃料的需求量不断增大,它们燃烧后放出大量的二氧化碳气体.而由于一些天灾和人为地乱砍滥伐,能吸收二氧化碳的大片森林却在不断消失.因此每年都有大量的二氧化碳进入大气.在地球的大气层中,二氧化碳气体能像温室中的玻璃那样起保温作用.于是就使地球的气温持续上升,这就是所谓的“温室效应”,科学家们认为,温室效应将对人类产生很大影响.
试根据以上叙述回答:防止温室效应进一步发展的有效措施有哪些?

参考答案:
【同步达纲练习】
一、1.A 2.B 3.C 4.D 5.D 6.B 7.C 8.C 9.C
二、10.(1)排水;(2)2NO+O2=2NO2;(3)物理 11.石灰石(或大理石) 稀盐酸 制得的二氧化碳的气体中混有氢气 Fe+2HCl=FeCl2+H2↑
三、12.99g,约50.2升
【素质优化训练】
13.鸡蛋被吸入广口瓶中,食醋是一种酸与蛋壳中的碳酸钙反应后使鸡蛋变软;酒精棉球在广口瓶中燃烧温度上升使广口瓶中的气体质量减小,当酒精棉球熄灭后温度降低,广口瓶中压强减小,故鸡蛋被吸入 14.可能看不到石灰水变浑浊的现象.因为浓盐酸挥发出来的氯化氢气体溶于水生成盐酸,盐酸与石灰水反应生成氯化钙和水,另外在盐酸存在时,碳酸钙不能生成.当然还要看混合气体中氯化氢占多大比例,石灰水中氢氧化钙含量的多少等因素 15.CaCO3 Ca(OH)2+CO2=CaCO3↓+H2O 稀盐酸 2HCl+CaCO3=CaCl2+H2O+CO2↑ 16.A 17.B
【知识验证实验】
(1)鸡蛋壳中的碳酸钙与稀盐酸反应产生大量气泡附在蛋壳表面,使鸡蛋受到浮力大于重力而使鸡蛋上浮.
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)①用稀盐酸或白醋去水垢.②做馒头时,加入适量的纯碱使馒头松软而无酸味③用柠檬酸和小苏打制汽水④泡沫灭火器灭火
答案:CaCO3
【知识探究学习】
解答:(1)大量植树造林,禁止乱砍伐;
(2)减少煤、石油、天然气等矿物燃料的使用;
(3)更多开发利用核能、太阳能、风能等能源.
