高中阶段招生考试化学卷
化 学 试 卷
| 题号 | 一 | 二 | 三 | 四 | 五 | 总分 |
| 得分 |
|
|
|
|
|
|
说明:1.全卷共6页。考试时间90分钟,满分100分。
2.请将选择题的答案填在括号内,其它试题的答案写在试卷相应的位置上。
3.可能用到的相对原子质量:H―1 C―12 O―16 Na―23 S―32
Ca―40 Cl―35.5 Ba―137
一、选择题(本题包括14小题,每小题2分,共28分。每小题只有一个选项符合题意,请将正确选项的编号填写在题目右边的括号内)
1. 地壳里元素的质量分数含量最大的是.....................................................…......( )
A.N B.Fe C.H D.O
2.下列变化属于物理变化的是...........................................................................…...( )
A.铁生锈 B. 玉米酿酒 C.干冰汽化 D.白磷自燃
3. 化学变化的最小粒子是...........................…........................……….....................( )
A.分子 B.原子 C.离子 D.质子
4. 实验室要收集一试管CO2,最好选用的装置是.....................................................( )
 |
A B C D
5. 次氯酸钠(化学式是NaClO)有强氧化性,可作消毒剂。则次氯酸钠中,氯元素的
化合价是 ............................................................................................….................( )
A.0 B.+1 C.+2 D.+3
6.下列实验操作正确的是..............................................................................................( )
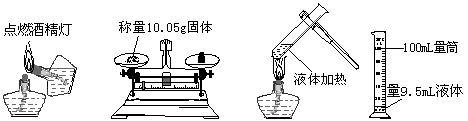 |
A B C D
7.下列说法错误的是.....................................................................................................( )
A. 矿泉水是混合物 B.CuSO4 是盐
C.纯碱(Na2CO3)是碱 D.Na2O是氧化物
8. 在H2、H2O、H2SO4 三种物质中,都含有..........................................................( )
A.氢元素 B.氢原子 C.氢分子 D.氢气
9. 测定生活中一些物质的pH,结果如下:

参照以上图示判断,下列说法正确的是...................................................................( )
A.牙膏是中性物质 B.草木灰可改良碱性土壤
C.胃酸过多的人不宜多吃橘子 D.食醋能使无色酚酞变红
10. 下列各组物质,在溶液中能共存的一组是...........................................................( )
A. HCl、NaCl、NaOH B. NaCl、CuSO4、Ba(OH)2
C. Na2CO3、NaOH、 CaCl2 D. NaNO3、HCl、CaCl2
11. 七星岩的岩石主要成分是碳酸钙,取一块岩石样品测其含碳酸钙75%,则该岩石
样品含钙(设其它成份不含钙)的质量分数为 ............................…....................( )
A.25% B.30% C.40% D.75%
12. 在含有H2SO4的CuSO4 溶液中加入一定量的铁粉,充分反应后,发现有固体剩余。
则下面的叙述正确的是....................................................…................…..........…....( )
A.溶液中一定含有FeSO4 B.溶液中一定没有CuSO4
C. 固体物质中一定不含有Cu D.固体物质中一定没有Fe
13. 向HCl和FeCl3的混合溶液中,不断加入NaOH溶液,下图曲线正确的是...( )
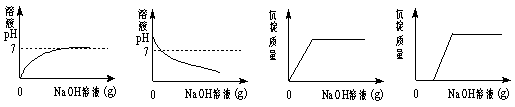 |
A B C D
14. 甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱
和溶液(试管底部均有未溶解的固体),
 再放进盛有冰水的烧杯里, 则下列说
再放进盛有冰水的烧杯里, 则下列说
法正确的是.................................( )
A.甲溶液中溶质的质量分数增大
B.乙溶液中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.试管里甲、乙两溶液中的溶质都减少
二、填空(本题有5小题,共22分)
15.(3分)写出下列化学符号或符号的意义:
(1)两个铁原子 ;(2)甲烷分子 ;(3)5H2O 。
 16.(2分)用肇庆特产之一桂皮蒸馏可以得到桂油,其主要成份是肉桂醛,化学式为C9H8O,它可作为饮料和食品的增香剂。则肉桂醛中含有 种元素,一个肉桂醛分子中有 个原子。
16.(2分)用肇庆特产之一桂皮蒸馏可以得到桂油,其主要成份是肉桂醛,化学式为C9H8O,它可作为饮料和食品的增香剂。则肉桂醛中含有 种元素,一个肉桂醛分子中有 个原子。
17.(3分)氯原子结构示意图 还可以画为: 。据此回答:
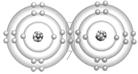 (1)氯原子有 层电子,原子核内有 个质子。
(1)氯原子有 层电子,原子核内有 个质子。
(2)图为: 的分子所表示的物质类别是 (填“单质”
![]() 或“化合物”)。
或“化合物”)。
|
 18.(2分)空气不流通时,使用燃气热水器会产生有毒气体,石油气中的一种气体X在氧气不足时燃烧,发生反应:X +5O2=====3CO+
CO2 + 5H2O,则X的化学式是
。
18.(2分)空气不流通时,使用燃气热水器会产生有毒气体,石油气中的一种气体X在氧气不足时燃烧,发生反应:X +5O2=====3CO+
CO2 + 5H2O,则X的化学式是
。
19.(12分)按要求写出化学反应方程式:
(1)(5分)安全火柴梗头及火柴盒侧面的物质如右
图所示,当两者摩擦时,生热点燃红磷而使火柴梗着火。
按要求填空:
①氯酸钾分解的化学方程式为: 。
②红磷反应的化学方程式为: ,反应类型是 反应。
(2)(5分)电镀前,把铁制品放入稀盐酸中浸泡,以除去表面的铁锈。其除锈的化学方程式为: ,反应类型是 反应;
如果浸泡时间太长会有气泡产生,该化学方程式为:
。
(3)(2分)某课外活动小组去鼎湖山宝鼎园,在铜鼎的表面取了一些铜绿[ 化学式为:
Cu2(OH)2CO3 ],将其放入装有稀H2SO4 的小烧杯中,样品溶解、溶液变蓝,并有气泡产生。由此现象写出该反应的化学方程式: 。
三、(本题有2小题,共18分)
20.(6分)将100mL酒精(CH3CH2OH)与l00mLH2O 充分混合后,其体积 200mL
(填<、 =、 >),原因是 ;
如果用这种酒精水溶液浸湿一块手帕,表演者将手帕放在布伞上点燃,一阵熊熊火焰燃烧后,手帕和布伞完好无损(如右图)。这一过程中,燃烧的物质是 ;燃烧后手帕和布伞完好无损的原因是
。
21.(12分)实验时,有同学不小心放错了胶头滴管,使得NaNO3溶液的试剂瓶中可能
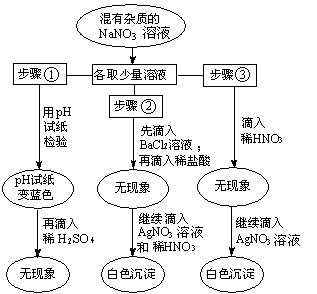 混入NaCl、NaOH、Na2CO3和Na2SO4
混入NaCl、NaOH、Na2CO3和Na2SO4
中的一种或几种。为了验证,他们进
行了如右图所示的实验。请回答:
(1)由步骤①得知:此溶液中含有
(写化学式)。
(2)由步骤②可知:此溶液不存在
(写化学式)。
(3)由步骤③可知:此溶液中含有
(写化学式)。
(4)某同学由步骤②判断这瓶NaNO3
溶液中含有NaCl,你认是否正确
(填“正确”或“错误”),原因是: 。
四、(本题有2小题,共18分)
 22.(6分)现有如右图三种实验装置:
22.(6分)现有如右图三种实验装置:
(1)写出标有番号的仪器名称:
① ,② 。
(2)装置A可用于制取的气体是:
。 A B C
(3)装置B可用于制取的气体是 。
(4)如果用C装置制取H2,在反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止,其原因是 .。
23.(12分)某小组的同学在课外进行科学探究,以验证铜片在空气中灼烧后,表面生
成的黑色物质确实是铜与氧化合生成的CuO,他们进行了以下实验:
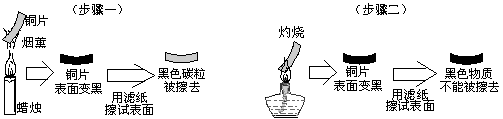 |
(1)由上图两个实验步骤判断:灼烧后铜片表面的黑色物质不是 。
 (2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:
(2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:
A B C
a.甲同学向A装置中通入纯净的H2,为检验反应产物,A的右边应连接上面的 装置(填番号),所选装置中的实验现象为 。
b.乙同学向A装置中通入纯净的CO,为检验反应产物,A的右边应连接上面的 装置(填番号),所选装置中的实验现象为 ;此方法仅用上述装置进行实验有明显的缺陷,要弥补这个缺陷,应采取的措施是:
。
c.通入的气体如果含有少量水蒸汽,则应在A装置左边连接一个 装置。
d.对A装置加热前,通入纯净气体应先 后 。
(3)结论 :经过甲、乙两同学的实验现象证明,
。
(4)如果甲同学要用数据证明(3)的结论,你认为还应补充的实验操作是:
。
五、(本题有2小题,共14分)
|
(1)从标签上的文字说明可以推知:
过氧乙酸受热时容易发生
。
(2)一瓶这种溶液中含过氧乙酸溶质 g。
(3) 0.5%的过氧乙酸溶液可以杀死细菌和SARS
病毒。 某医院需配制0.5%的过氧乙酸, 一瓶这种
过氧乙酸需加多少克水?
25.(8分)将7.33gNaCl和Na2SO4的固体混合物溶于85g水中,滴入10g BaCl2溶液恰好沉淀完全。过滤,将固体沉淀物干燥称得质量为2.33g。请计算:
(1)原混合物含有Na2SO4多少克?(2)所得滤液中溶质的质量分数为多少?
高中阶段招生考试
化学参考答案及评分标准
一、选择题(本题包括14小题,每小题2分,共28分)
1. D 2.C 3.B 4.A 5.B 6.C 7.C 8.A 9.C 10.D 11.B
12.A 13.D 14.B
(以下各题的化学方程式,未配平扣0.5分,未写条件扣0.5分)
二、填空(本题有5小题,共22分)
15.(3分)(1)2Fe (2)CH4 (3)五个水分子(每空1分)
16.(2分)三(1分),18(1分)
17.(3分) (1) 3(1分),17(1分) (2)单质(1分)
|
|
|
(2)Fe2O3 +6HCl ====2FeCl3 +3H2O(2分),复分解(1分);
Fe +2HCl====FeCl2 + H2↑(2分)
(3) Cu2(OH)2CO3 + 2H2SO4=====2CuSO4 + CO2↑ + 3H2O(2分)
三、(本题有2小题,共18分)
20.(6分)<(1分),酒精和水分子间都有空隙,它们混合后,部分分子挤占了分子间的空隙,故混合后的总体积小于混合前各自体积之和(或答“分子间都有空隙”同样给分,2分)。乙醇(或酒精,或C2H5OH,1分);水蒸发带走了酒精燃烧产生的热量(或水有降温作用,1分),使手帕和布伞的温度达不到着火点(1分)
21.(12分)(1) (2分)NaOH 。(2) (4分)Na2CO3 、Na2SO4(每空2分)
(3) (2分)NaCl (以上化学式写成物质名称,每错1个扣1分)
(4) (4分)错误(2分);加入HCl和BaCl2引入了Cl―,无法证明原溶液是否含有Cl―(或引入了Cl―,2分)
四、(本题有2小题,共18分)
22. (6分)(1)(2分)①锥形瓶,②试管 (2)(2分)H2、CO2
(3)(1分)O2 。[第(2)、(3)两问的答案写名称同样给分]
(4)(1分)反应不断产生气体形成的压力,使干燥管内液面下降脱离固体,从而使反应停止
23.(12分) (1)(1分)碳粒(或吸附的碳,或活性碳)
(2)(8分)a.C(1分),无水硫酸铜由白色变为蓝色(或无水CuSO4变蓝,或变蓝色,1分)。 b. B(1分),澄清石灰水变浑浊(或变浑浊、或有白色沉淀,1分)对尾气进
行处理(或在导管出口处点燃,或在导管口套接一个气球或塑料袋,1分)。c.C装置(或干燥装置、或装有浓硫酸的洗气瓶、或装有碱石灰的干燥管。1分) 。d.通气体、加热(2分)
(3) (1分)铜在空气中加热确实是与氧化合,并生成了氧化铜( 或黑色物质中含有氧元素。其它合理叙述均给分)
(4)(2分)对铜片灼烧前后,以及用气体还原以后都进行称量(或“对铜片灼烧前后,C装置反应前后都称量”。答“对铜片称量”给1分;答“称量”不给分)
五、(本题有2小题,共14分)
24.(6分)(1)分解(或燃烧、或爆炸).................................................................(1分)
(2) 200 ......................................................................................................................(2分)
(3) 解:设需加入水的质量为x。................................….....................................(0.5分)
则:(x+500)×0.5%=500×40%....................................................................…....(1分)
解得:x=39500(g) ...................................................................……......................(1分)
答:一瓶这种过氧乙酸需加水39500g。.............................................................(0.5分)
25.(8分)解:设混合物中含Na2SO4 的质量为 x,生成NaCl 的质量为y。
则:Na2SO4+BaCl2===BaSO4↓+2NaCl........................................................…..….....(1分)
142 233 117 ............................................................…....(1分)
x 2.33g y.............................................……........................(1分)
![]() (1) 142 :
x=233 : 2.33g
解得: .............................(1分)
(1) 142 :
x=233 : 2.33g
解得: .............................(1分)
![]() (2) 117:
y=233 : 2.33g ..................................(1分)
(2) 117:
y=233 : 2.33g ..................................(1分)
∴滤液的总质量为:10+7.33+85-2.33=100(g) .....................................……....................(1分)
滤液中溶质的质量为:1.17+(7.33-1.42)=7.08(g) ..................…………............................(1分)
![]()
故:滤液中溶质的质量分数为: …………………….................(1分)
解法二:(1)同上。
(2)根据质量守恒定律:Na+ 反应前后质量不变。
由2.33g BaSO4→BaCl2 引入Cl― 0.71g ; 2.33g BaSO4→Na2SO4 用去SO42― 0.96g
阴离子减少的质量: 0.96g- 0.71g = 0.25g ..........................................................…….....(1分)
滤液中溶质的质量为:7.33g- 0.25g=7.08g .......................................................….......(1分)
滤液的总质量为:10+7.33+85 - 2.33=100(g) ...................................................…........(1分)
滤液中溶质的质量分数为: ………….. .........................….......(1分)
答:(1)原混合物含Na2SO41.42g;(2)滤液中溶质的质量分数为7.08%。
(如有其它正确解法,参考相应标准给分)