初三年(上)化学期中试卷
相对原子质量 H―1 O―16 S―32 C―12 Mn―55
Fe―56 Na―23 K―19 N―14 Cl―35.5
一、选择题:(每小题只有一个正确答案,1-15题每小题1分,16-25题每小题2分,共35分)
1. 下列变化属于化学变化的是:()
A. 家庭自制冰块 B.矿石粉碎 C.铁钉生锈 D.氧气液化
2. 在空气中分别点燃下列物质,发生反应最剧烈的是:()
A. 镁带 B.木炭 C.硫粉 D.蜡烛
3. 下列各组元素中,元素符号大写字母不相同的是:()
A. 铝、银 B.氯、钙 C.汞、银 D.硫、磷
4. 下列物质属于纯净物的是:()
A. 净化的空气 B.冰和水的混合物
C.高锰酸钾受热分解后的固体产物 D.海水
5. 在粗盐提纯的各个操作中都必须用到的仪器是:()
A. 烧杯 B.量筒 C.玻璃棒 D.酒精灯
6. 取三份相同质量的氯酸钾,将第一份直接加热,第二份加入二氧化锰后加热,第二份加入高锰钾后加热,产生氧气最多的是:()
A. 无法判断 B.第一份 C.第二份 D.第三份
7.下列关于分子、原子、离子的叙述正确的是:()
A. 原子是构成物质的最小粒子 B.离子是带电的原子或原子团
B. 分子是化学变化中的最小粒子 D.构成物质的粒子只有分子和原子
8.会严重污染大气的气体是:()
A.氢气 B.氮气 C.二氧化硫 D.二氧化碳
9.碳的相对原子质量是:()
A. 12 B.12 C.1.993×10-26 D.1/12
10.美国和日本的三位科学家以导电有机高分子材料的研究成果容获2000年若贝尔化学奖,在其相关技术中用碘来掺杂聚合物,使其导电能力增强有力107,具有金属般的导电能力。碘(I2)属于:()
A.非金属单质 B.金属单质 C.化合物 D.混合物
11.下列仪器使用不正确的是: ()
A. 镊子夹取块状药品 B.药匙取出少量的二氧化锰
C.酒精灯引燃另一只酒精灯 D.天平称量固体药品
12.A、B两种元素的化合价分别为+1、+4价,由于这两种元素和氧元素组成的化合物的化学式是:()
A.ABO3 B.A2BO3 C.ABO4 D.A2BO4
13.下列结构示意图中,表示阳离子的是:()
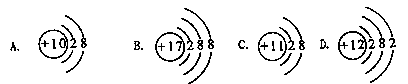
14.下列符号中,能表示一种单质的化学式,还有表示一种元素和该元素的一个原子的是:()
A.O B.H2 C.2N D.C
15.同质量的SO2和SO3中氧元素的质量比为:()
A.5:4 B.6:5 C.5:6 D2:3
16.X元素原子最外层有6个电子,Y元素原子最外有3个电子,这两种元素形成的化合物的化学式为:()
A.Y2X3 B.X2Y3 C.X3Y2 D.YX2
17.H2还原CO的操作内容有:①加热②通氢气③停止通氢气④停止加热,正确的操作顺序是:()
A.①②③④ B.②①③④ C.①③②④ D.②①④③
18.最近科学家研制一种新的分子,起化学式是C60,下列说法正确的是:()
A.由分子C60构成的纯净物是一种化合物
B.纯净物C60的相对分子质量为12×60=720
C.由分子C60构成的纯净物是一种金属单质
D.纯净的物质(C60)是由60个碳原子构成
19.某气体既能用排水法收集,又能用向上排空气法收集。该气体具备的性质是:()
A.易溶于水,比空气轻 B.难溶于水,比空气轻
C.易溶于水,比空气重 D.不易溶于水,比空气重
20.下列化学式所表示的各物质中,氧元素的质量分数最小的是()
A.CO2 B.MnO2 C.FeO D.Na2O
21.下列化合物中,硫元素的化合价最低的是:()
A.SO2 B.H2SO4 C.SO3 D.H2S
22.下列说法正确的是:()
A.呼吸和食物腐败都包含有缓慢氧化
B.可燃物的急剧燃烧一定会发生爆炸
C.缓慢氧化一定会引起自燃
D.浸在70-80℃热水里的白磷不会自燃,是因为温度低于着火点
23.冶金工业上,用氢气从三氧化钨冶炼出金属钨,这是利用氢气的()
A.氧化性 B.还原性 C.助燃性 D.以上都不是
24.地壳中含量最多的金属元素和非金属元素,以及大气中含量最多的元素,可以组成的化合物是:()
A.Fe(NO3)3 B.Al2(SO4)3 C.Al2O3 D.Al(NO3)3
25.下列关于物质燃烧现象的叙述,错误的是:()
A.木炭在氧气中燃烧发出红光 B.氢气在空气里燃烧发出淡蓝色火焰
C.硫在空气里燃烧发出蓝色火焰 D.磷在空气里燃烧产生浓厚白烟
二、填空题:(共40分)
26.构成物质的粒子有______、_______、_______等。如二氧化碳是由________构成的。铁是由_____构成的。氯化钠是由_______和_______构成的。
27.实验室取固体药品一般用______,取用一定量的液体应用_______,吸取和滴加少量液体时,可用__________。
28.铁丝在氧气中______________________________________。做此实验时,为了防止集气瓶爆炸,集气瓶里应先放入_______或___________。
29.水通电后,正极上生成_____,负极上生成_______,说明水由____和_____组成。化学反应文字表达式为________________________________。
30.有①磷②铁③氧化铜④氧气⑤氢气⑥稀盐酸⑦高锰酸钾七种物质(填各物质的序号)
(1) 属于混合物的有________,属于化合物的有___________,
属于单质的有_______,属于氧化物的有___________。
(2) 从上述的七种物质中选择合适的物质作为反应物,写出符合下列要求的文字表达式,并在各物质名称下写出相应的化学式。
① 生成氧气的分解反应____________________;
② 生成氢气的置换反应_______________________;
③ 生成白色固体的化合反应___________________;
④ 有水生成的置换反应______________________。-
31.写出下列符号中2所表示的意义
+2
(1) O2___________(2)CO_______
32.某化合物的化学式为KnR2O3n+1,则元素R的化合价为___________。若已知化合物的相对分子质量为A,则R元素的相对原子质量为_________。
 33.某种氮元素的氧化物A中,氮元素的化合价为+5价,则A的化学式为__________,相对分子质量为__________,此氧化物中,氮元素的质量分数为(精确到0.1%)______;另一种氮的氧化物B中,氮氧两种元素的质量比为7:4,相对分子质量为44,则B的化学式_________。
33.某种氮元素的氧化物A中,氮元素的化合价为+5价,则A的化学式为__________,相对分子质量为__________,此氧化物中,氮元素的质量分数为(精确到0.1%)______;另一种氮的氧化物B中,氮氧两种元素的质量比为7:4,相对分子质量为44,则B的化学式_________。
三、实验题:(本题共15分)。
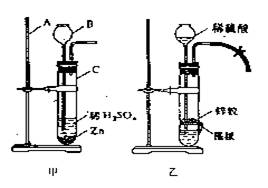
34.右图甲、乙表示氢气的简易发生装置。
试回答:(1) 甲图中仪器名称:A_____、
B_______、C_______。
a) 这两种装置中,_____装置(填“甲”或“乙”)能控制反应的发生和停止。
b) 甲装置的仪器B,如未插入稀硫酸中,则出现的问题将是
c) (用A、B、C回答)先将锌粒从____口加入,后将稀硫酸从______口倒入。
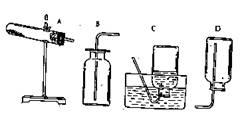 35.见右图所示的四种装置,试回答:
35.见右图所示的四种装置,试回答:
(1)若用装置A制备氧气,则所缺少的一种仪器的名称是__________。
(2)(用图中字母回答)收集氧气的装置
是____或_____。
(3)装置A中,若试管内的固体药品是高锰酸钾,则需要一团_____________放在靠近试管口的地方,以防止加热时______________________________________。
(4)A装置中,试管口应略向下倾斜是为了____________________________,(B)(D)装置中的导管要伸到接近集气瓶的底部,是有利于___________________________。
(5)实验完毕时应先_____________后_____________________,以防__________________。
四、计算题(共10分)
36.根据碳酸氢铵(NH4HCO3)的化学式计算(写出计算过程)
(1)碳酸氢铵的相对分子质量为:_________________________________。
(2)碳酸氢铵中氮、氢、氧、碳的原子个数比为________________,碳酸氢铵里氮、氢、氧、碳元素的质量比为________________________________________。
(3)碳酸氢铵中氮元素的质量分数为________________________(精确至0.1%)。
(4)50碳酸氢铵与多少硝酸铵(NH4NO3)含有相同质量的氮元素? (精确至0.1)。
37.实验室用氯酸钾为原料制氧气,现有6.125g氯酸钾,问:
(1)这6.125g氯酸钾中含氧元素多少克?(第(1)、(3)小题要写出过程)
(2)若将这6.125g氯酸钾和少量的二氧化锰混合加热,最多可制得氧气_________克?
(3)制得的氧气,在标准状下,占体积约为多少升?( 在标准状下,氧气的密度为1.43g /L) (精确至0.1)
参 考 答 案
一、选择题:(每小题只有一个正确答案,1-15题每小题1分,16-25题每小题2分,共35分)
1.C 2.A 3.D 4.B 5.C 6.D 7.B 8.C 9.B 10.A 11.C 12.B 13.C 14.D 15.C
16.A 17.D 18.B 19.D 20.C 21.D 22.A 23.B 24.D 25.A
二、填空题:(共40分)
26.分子、原子、离子。二氧化碳分子、铁原子。钠离子和氯离子。
27.药匙、量筒、滴管。
|
29.氧气,氢气,氧元素和氢元素。水 → 氢气 + 氧气
|
(2)①高锰酸钾 → 锰酸钾+二氧化锰+氧气 ②铁 + 稀盐酸 → 氯化亚铁 + 氢气
|
|
③磷 + 氧气 → 五氧化二磷 ④氧化铜 + 氢气 → 铜 + 水
P O2 P2O5 CuO H2 Cu H2O
31.(1)一个氧分子中含有两个氧原子(2)在氧化铜中,铜为+2价
32.![]()
33.N2O5,108,25.9%,N2O
三、实验题:(本题共15分)。
34.铁架台,长颈漏斗,试管。(2)乙(3)氢气将会从长颈漏斗口逸出。(4)C,B.
35.(1)酒精灯(2)B或C(3)棉花,防止高锰酸钾粉末进入导管。
(4)防止冷凝的水滴倒流回试管底部,使灼热的试管破裂;将集气瓶里的空气排出。
(5)把导管移出水面,熄灭酒精灯,水槽里的水倒吸入试管,使灼热的试管破裂。
四、计算题(共10分)
36.(1)79 (2)1:5:3:1;14:5:48:2(3)17.7%(4)25.3kg
37. (1)2.4g(2)2.4(3)1.7L