初三特训班化学测试题(西城)1
(测试时间30分钟)
班级 姓名 学号 分数
可能用到的相对原子质量:H―1 O―16 C―12 N―14 Na―64 Cu―64 Ca―40
Zn―65 Fe―56 Mg―24
一、 选择题(每题有1~2个选项)(请将答案填写在下面答案表里)
1.日常生活中的下列变化,前者是化学变化,后者是物理变化的是
(A)钢铁生锈 灯泡发光 (B)煤气爆炸 煤燃烧
(C)酒精挥发 食物腐败 (D)石蜡熔化 干冰升华
2.下列物质中,含有氧分子的是
(A)KClO3 (B)CO2 (C)SO2 (D)液态氧
3.下列物质中,硫元素的化合价由高到低排列的一组是
(A)K2SO4、K2SO3、K2S (B)H2S、SO2、SO3
(C)H2S、H2SO4、H2SO3 (D)Na2SO4、Na2S、Na2SO3
4.下列物质中,属于金属单质的是
(A)金刚石 (B)水
(C)镁
(D)氧气
5.下列物质中,属于氧化物的是
(A)Fe2O3 (B)KClO3 (C)O2
(D)Ca(OH)2
6.根据质量守恒定律,在反应2AB2 + B2 = 2C中,C的化学式可能是
(A)A2B4 (B)AB3 (C)A2B3 (D)A3B2
7.下列哪种过程不产生二氧化碳
(A)呼吸 (B)木材燃烧 (C)植物光合作用 (D)煅烧石灰石
8.制取氧气的方法有:①加热氯酸钾;②加热高锰酸钾;③加热氯酸钾和二氧化锰的混合物;④加热氧化汞;⑤加热氯酸钾和高锰酸钾的混合物;⑥水中通入直流电。下列用于实验室制取氧气方法的选择中,都正确的是
(A)①②③⑤ (B)②③④ (C)②③⑤ (D) ②③⑥
9.将CO、CO2、H2、O2和N2的混合气体依次通过石灰水、热铜网、灼热的氧化铜,若每次都完全反应,冷却至室温,最后剩余的气体是
(A)N2和CO (B)O2和N2 (C)CO2和N2 (D)只有N2
10.欲证明生石灰中含有石灰石,最简单的方法是
 (A)加热
(B)加水,通入CO2
(A)加热
(B)加水,通入CO2
(C)高温煅烧 (D)滴加稀盐酸
11.吸烟危害健康,其原因是吸烟时会吸入多种有害气体。其中有一种是氧化物,它的组成中氧元素与另一种元素的最简质量比为4:3。它是下列气体中的
(A)NO (B)CO2 (C)CO (D)SO2
12.一定量的NaNO3饱和溶液由30℃升温至50℃(忽略水的蒸发),肯定改变的是
(A) 溶质的质量 (B)溶液的质量
(C) 溶液的溶质质量分数 (D)NaNO3的溶解度
13.要配制0.5%的过氧乙酸溶液1000g,下述方法中正确的是
(A)称取0.5过氧乙酸,溶于100g水中 (B)称取0.5过氧乙酸,溶于1000g水中
(C)称取50g过氧乙酸,溶于950g水中 (D)称取5g过氧乙酸,溶于995g水中
14.在一定温度下某固态溶质(不含结晶水)的水溶液,经历如下变化:
 |
溶液甲 溶液乙 溶液丙 ,下列结论正确的是
(A)溶液甲可能是饱和溶液 (B)溶液乙一定是不饱和溶液
(C)溶液乙和溶液丙中的溶质质量分数可能相等
(D)溶液丙若再蒸发5g水,析出的晶体可能大于2g
15.某无色气体可能由CH4、H2、CO、CO2中的某两种气体组成,在恒温、恒压条件下,通过过量的澄清石灰水,未见变浑浊,混合气体在O2中能够点燃,充分燃烧后气体中二氧化碳和水蒸气分子个数比为1:1。则原混合气体的成分可能是
(A)CH4 、H2 (B) CH4 、CO (C)CO、 H2 (D) CH4 、CO2
答案表
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
二、填空题
16.用符号表示:两个氮原子_______两个水分子 钠离子
三个硝酸根离子 +3价铝元素
17.现有如下化学实验方法:(A)用燃着的木条 (B)通入足量澄清石灰水 (C)检验燃烧后的产物 (D)在空气中充分灼烧。请从中选择适当方法的序号,写在各题题后的横线上
①鉴别氢气和一氧化碳 ;②除去一氧化碳中少量的二氧化碳 ;
③鉴别氧气和二氧化碳 ;④除去氧化铜中少量的铜 。
18.在一个通风良好、燃烧正旺的煤炉的煤层上方常会观察到有蓝色火焰产生,这是因为在煤层上方有 燃烧。此时煤炉中发生了三个不同的化学反应,其化学方程式:
①
②
③
19.在粗盐提纯的实验中,玻璃棒共用了________次,它在下列操作中的作用是:(1)在过滤操作中____________ ;(2)在蒸发操作中 _________ _____。
20.葡萄糖(C6H12O6)、蔗糖(C12H22O11)等糖类化合物是人的生命活动不可缺少的重要物质。已知核糖的相对分子质量为150,其中含碳40%,含氢6.7%,其余是氧。则核糖的化学式是 。
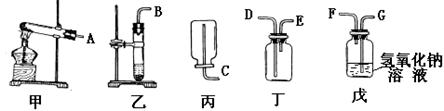 21.硫化氢(H2S)是一种无色、具有臭鸡蛋气味的有毒气体,其密度比空气大,且能溶于水形成氢硫酸,溶液显酸性。实验室通常用块状固体硫化亚铁(FeS)跟稀硫酸反应,在常温下通过复分解反应制得硫化氢气体和硫酸亚铁。试根据下图回答:
21.硫化氢(H2S)是一种无色、具有臭鸡蛋气味的有毒气体,其密度比空气大,且能溶于水形成氢硫酸,溶液显酸性。实验室通常用块状固体硫化亚铁(FeS)跟稀硫酸反应,在常温下通过复分解反应制得硫化氢气体和硫酸亚铁。试根据下图回答:
(1)具有臭鸡蛋气味,这属于硫化氢的 (物理、化学)性质。
(2)实验室制取硫化氢应选用的发生装置是 收集装置是
 (3)实验室制硫化氢气体的化学方程式
(3)实验室制硫化氢气体的化学方程式
(4)为了验证硫化氢的水溶液呈酸性,可将该气体通过装置戊,戊中所盛放的试剂应该是 ;现象是 ,进气口应为 。
(5)因为硫化氢有毒,所以不能在空气中随意排放。请从上图中选择装置,完成硫化氢的制气、收集、尾气处理实验操作,将装置的接口顺序填在横线上
(注明:氢氧化钠溶液显碱性,可与酸发生反应)
三、计算题(最后结果保留一位小数)
22.15g不纯锌粒与100g稀硫酸充分反应得到0.4g氢气, (无晶体析出)求:
(1)锌粒的纯度?
(2)稀硫酸溶液的溶质质量分数?
(3)生成硫酸锌溶液的溶质质量分数?
23.现有200g溶质质量分数为10%的NaOH 溶液,求:
(1) 需加多少克49%的稀硫酸与之完全反应?
(2NaOH +H2SO4== Na2SO4 +2H2O )
(2) 取出20g溶液后剩余溶液的质量分数为__________________
(3) 在剩余溶液中加入20g水后, 溶液的质量分数为___________
初三特训班化学测试题答案(西城)1
一、选择题
1、A 2、D 3、A 4、C 5、A 6、B 7、C 8、C
9、C 10、D 11、C 12、D 13、D 14、CD 15、BC
二、填空题
16.2N 2H2O Na+ 2NO3- ![]()
![]() 17.①C、②B、③A、④D
17.①C、②B、③A、④D
18.CO C+O2 CO2
![]()
C+CO2 2CO
2CO+O2 2CO2
19.3 引流 搅拌,防止受热不均,液滴外溅
20.C5H10O5
21.(1)物理 (2)乙 丁 (3)FeS+H2SO4=FeSO4+H2S↑
(4)紫色石蕊试液 变红 G
(5)B D E G F
22.(1)86.7% (2)19.6% (3)28.6%
23.(1)50g (2)10% (3)9%