初三化学模拟试卷2
(总分100分,答卷时间100分钟)
说明:1、本试卷分第I卷和第II卷,第I卷为选择题,第II卷为非选择题;答题时,将第I卷的答案填在答题卡上,考试结束时,只需交答题卡和第II卷
2、本试卷可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23
Mg-24 Al-27 S-32 Cl-35.5 Cu-64 Ag-108
第I卷选择题 (共40分)
一、选择题(每小题只有1个选项符合题意。每小题1.5分,本题共30分。)
1、我国宇航员杨利伟从神州五号飞船上观察到的地球是一个美丽的、蔚蓝色的星球,下列有关说法正确的是
A.地球上的水是无色无味的 B.蔚蓝色主要是海洋的体现
C.大气层中有淡蓝色的液氧 D.蔚蓝色主要是森林的体现
2、下列没有元素化合价变化的是
A.田径比赛的发令枪打过后有白烟 B.撒布干冰产生云雾
C.KClO3与MnO2混合加热 D.水通直流电
3、吸烟有害健康,原因之一是烟气中含有使血红蛋白不能很好地跟氧气结合的有毒气体,该气体是
A.CO2 B.N2 C.CO D.O2
4、下列饮料中,不属于溶液的是
A.可口可乐 B.啤酒 C.雪碧 D.酸奶
5、2005年,南通市将结束西气东输工程,届时市区居民将可望用上天然气,下列有关天然气的说法不正确的是
A.天然气较人工煤气纯度高,燃烧形成的污染小
B.天然气较人工煤气热值高(即反应放出的热量大)
C.天然气燃烧后没有污染
D.天然气的主要成份是甲烷,早在明朝宋应星所著的《天工开物》一书中就有记载
6、根据下列粒子结构示意图,判断下列说法正确的是
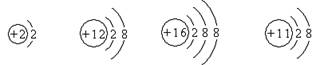
A.它们都是原子 B.它们都是离子
C.它们表示三种元素 D.它们都是稳定结构
7、20℃时,往50g水中加入20gNaCl晶体,充分搅拌后,过滤,得到2g固体,则滤液中的溶质质量分数为
A.26.5% B.40% C.28.6% D.36%
8、下列各项活动的后果,对环境都没有危害的是

工业废气 人、动物、植物的呼吸 喷洒农药 植物的光合作用
① ② ③ ④
A.②③④ B.②④ C.①③④ D.①②④
9、下列物质沾在试管内壁上,用盐酸不能洗去的是
A.做氢气还原氧化铜实验留下的红色固体
B.氢氧化钠溶液与硫酸铜溶液反应后留下的蓝色固体
C.碱式碳酸铜受热分解后残留的黑色粉末
D.铁钉锈蚀形成的锈斑
10、下列物质中既能与稀盐酸反应又可以和石灰水反应的是
A.硫酸铜 B.稀硝酸 C.碳酸钠 D.氧化铁
11、某有机物完全燃烧生成CO2和H2O, 已知参加反应的该有机物和O2的分子个数之比为1∶3,则该有机物的化学式可能是
A. C2H6O B.CH4 C. C2H2 D.CH2O
12、下列各组物质混合后,不能发生化学反应的是
A.碳酸钠溶液与盐酸 B.氯化钡溶液与硫酸
C.氢氧化钾溶液与硝酸 D.硝酸钾溶液与氯化钠溶液
13、据《中国消费者报》消息:现在宾馆、饭店中配备的小牙膏大多数是假冒伪劣产品,不法分子用工业滑石粉(3MgO・4SiO2・H2O)作为填充剂,长期使用可导致口腔溃疡和牙龈出血。下列说法中正确的是
A.滑石粉分子是由3个MgO分子、4个SiO2分子和一个H2O分子构成
B.滑石粉是由Mg、Si、O、H四种元素组成
C.滑石粉属于氧化物 D.滑石粉属于混合物
14、下列化学方程式中,正确的是
|
C.CO2+2NaOH==Na2CO3+H2O D.P+O2==PO2
15、在配制溶质质量分数为10%的氯化钠溶液时,导致溶液中氯化钠质量分数小于10%的可能原因是①用量筒量取水时俯视读数,②配制溶液的烧杯用少量蒸馏水润洗,③在托盘天平的左盘称取氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数 ,④盛装溶液的试剂瓶用蒸馏水润洗,⑤氯化钠晶体不纯净
A.①②③④⑤ B.①②④⑤ C.①②③ D.②③④⑤
16、在托盘天平两盘上各放一个烧杯,两烧杯盛有等质量的等质量分数的足量盐酸,天平保持平衡。此时向左盘烧杯中加入10gMgO,若要使天平再次平衡,应向天平右边的烧杯中加入
A.10gCu B.10.9g镁条 C.10gNa2CO3 D. 12g铝片
17、某无色溶液中,含有KNO3、BaCl2、Na2CO3、HCl中的两种溶质。向混合溶液中加入稀硫酸,只产生无色、无味气体的现象,则此溶液中所含的物质是
A.Na2CO3、BaCl2 B.HCl、KNO3
C.HCl、Na2CO3 D.Na2CO3、KNO3
18、下列有关实验叙述正确的是
A.氢气还原氧化铜实验时,可以不需要检验氢气的纯度
B.托盘天平可以准确称得4.55g 氯化钠固体
C.无论是对试管内固体还是液体加热,加热时,都先要预热,然后将酒精灯火焰集中对准装有药品的部分加热
D.通常胶头滴管用完后立即洗干净,而药匙用完后只需用干净的纸擦拭干净
19、若浓硫酸的组成用SO3・x H2O来表示,则98%的浓硫酸可表示为
A.SO3・![]() H2O B.SO3・
H2O B.SO3・![]() H2O C.SO3・46H2O D.SO3・2H2O
H2O C.SO3・46H2O D.SO3・2H2O
20、向含有盐酸和氯化铜的混合溶液中加入氢氧化钠溶液,产生沉淀的质量Q与加入氢氧化钠溶液的质量W的关系,图象正确的是
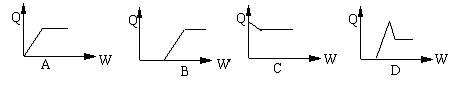
二、选择题(每小题有1~2个正确答案,全都选对得2分,若有两个正确答案的选对一个得1分,多选或选错不得分。每小题2分,共10分)
21、下列说法不正确的是
A.档案等资料的书写要用碳素墨水是因为常温下碳单质的化学性质稳定
B.从环境保护角度,未来的理想燃料是氢气
C.农作物的茎、叶生成茂盛,叶色浓绿是因为土壤中氮肥充足的原因
D.除去KNO3中含有少量NaCl杂质,可用蒸发、结晶的方法
22、有一包铜和碳组成的固体混合物,在一定条件下与氧气完全反应,生成固体氧化铜和二氧化碳气体,并测得反应前后固体质量不变,则原固体混合物中碳的质量分数是
A.15% B.20% C.32% D.无法确定
23、不用其他试剂就可以鉴别的一组溶液是
A.Na2CO3、NaOH、HCl、Ca(OH)2
B.KOH、NaCl、H2SO4、HCl
C.NaCl、CuSO4、NaOH、H2SO4
D.NaOH、KNO3、Na2SO4、HCl
24、向AgNO3、Cu(NO3)2、Mg(NO3)2的混合物溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Ag+、、Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
D.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+、Mg2+
25、在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
下列说法正确的是
A.该闭容器中发生的化学属于分解反应
B.密闭容器中发生的化学属于化合反应
C.反应后密闭容器中A的质量为22g
D.该反应中A、B、C、D四种物质的质量比为22∶9∶111∶80
第II卷非选择题(共60分)
三、填空题(本题共有4小题,共21分)
26、人体内含过多的尿酸(C5H4N4O3)会引起痛风和肾结石,治疗时可以服用嘌呤醇(C5H3N4OH),两者组成的元素种类 (填“相同”或“不同”),每个分子中所含 原子个数不同。
27、调味用的食醋中含有醋酸,醋酸可与氢氧化钠反应生成醋酸钠(CH3COONa),同时醋酸可用来浸泡水壶以除去水壶中的水垢(主要成分是碳酸钙和氢氧化镁)。写出有关反应的化学方程式
①
② 。
28、用化学方程式表示除去下列各组物质中的杂质(括号内的物质为杂质)
(1)FeSO4(CuSO4)_______________________________________________________
(2)CuO(C)_____________________________________________________________
(3)NaOH(Na2CO3)_______________________________________________________
(4)CO2(CO)____________________________________________________________
29、A、B、C是三种常见的氧化物,常温下,A是无色无味的气体,B是无色无味的液体,C、D、F是白色固体,自然界中含有F的矿石是重要的建筑材料之一,向E、D中滴加紫色的石蕊试液,E中石蕊呈红色,D中石蕊呈蓝色。B和C化合生成D时,放出大量的热,下图是相关物质的转化关系:
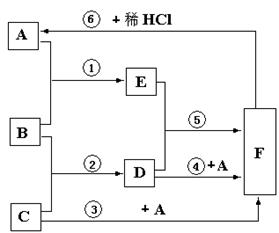
试回答:
(1)用化学式表示下列物质:
B___________ C _________ E___________
(2)书写下列变化的化学方程式
④____________________________________________________________
⑥____________________________________________________________
四、简答题(本题共有2小题,共9分)
30、日常生活中我们要科学地节约用水。现有一件刚用洗涤剂洗过的衣服,“拧干”后湿衣服残留的溶液为100g ,其中含洗涤剂的质量分数为1%,则湿衣服上残留的洗涤剂质量为______g 。现用5700g 清水对这件衣服进行漂洗,有以下两种漂洗方法(假设每次“拧干”后湿衣服仍残留100g 溶液)。
方法一:用5700g 清水一次漂洗,“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示)________g;
方法二、将5700g清水均分成质量相等的三份(每份1900g),分三次漂洗。
第1次漂洗“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示)_______g;
第3次漂洗“拧干”后残留在衣服上的洗涤剂的质量为(用分数表示)_______g;
由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水分成多份,多次漂洗效果好?_______________________________________________________
31、某同学在学习了酸、碱、盐知识后,该同学进行了如下微型实验:分别滴加盐酸、醋酸、硫酸铝、氯化铵四种无色溶液各3滴于井穴板的井穴中(每个井穴相当于一支小型试管),再加入1滴石蕊试液(所有试剂用量共0.4mL),观察到四种溶液均变红。
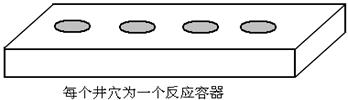
(1)本实验说明这四种溶液都显____________性,pH_________7(填“<”“>”或“=”)
(2)由此实验的过程和现象你还能得出哪些结论? (只要答两点)_____________________
_____________________________________________________________________________。
五、实验题(本题共有3小题,共17分)
32、有些化学实验必须严格遵循一定的实验操作顺序,否则可能造成实验失败,甚至发生事故,例如:点燃氢气前必须先检验氢气的纯度,然后再点燃,请再举两个严格遵循实验操作顺序的实例:
(1)______________________________________________________________
(2)______________________________________________________________
33、用下图所示实验装置作测定水组成的实验,回答有关问题:(9分)
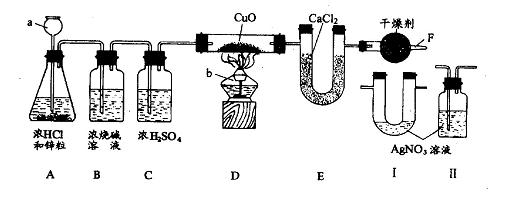
⑴ 图中仪器 a的名称是_____________________,仪器b的名称是__________________。
⑵ 根据精确实验测知,水中氢氧元素的质量比为1∶8,试用“<”、“>” 或“==”符号回答:
① 如果没有C装置,则测得的水中氢氧两种元素的质量比___________1∶8;
② 如果没有F装置,则测得的水中氢氧两种元素的质量比___________1∶8;
⑶ 为了证明进入D装置玻璃管的H2中不含有HCl,常在________装置之间增加装置__________(选填I或II);为了证明进入D装置玻璃管的H2中不含有水蒸气,常在____________装置之间增加一个装有无水硫酸铜的干燥管,则新增的两个装置在达到实验目的的前提下实验现象是:_______________________________________________。
34、某科学家在科学实验时,不慎将稀盐酸溶液洒到身旁盆花的花瓣上,他惊奇地发现花瓣的颜色发生了改变。于是他想到植物的叶子是否可以用来指示溶液的酸碱性呢?他作了一系列的实验来验证自己的设想,结果发明了用花瓣做酸碱指示剂的方法。
请问:如果是你,你将会设计出一些什么试验方案来验证自己的设想呢?请将实验过程、现象及结论填入下表:
| 设想 | 实验内容 | 观察到的现象 | 解释或结论 |
| (1)是否酸溶液都可以使该花瓣变色呢 | (1)将其他酸溶液也分别滴到该花瓣上 | 花瓣的颜色也发生同样的变色 | 该花瓣可以用来检验某溶液是否是 溶液 |
| (2)NaOH溶液是否也可以使花瓣变色呢? | (2) | 花瓣的颜色果然发生了不同于酸的变色 | |
| (3)是否所有碱溶液都可以使该花瓣变色呢? | (3) |
六、计算题(本题共有2小题,共13分)
35、为了对海水中的氯化钠(假设以NaCl计算)进行成分分析,甲、乙、丙、丁四位同学分别进行实验,他们的实验数据如下表,请仔细观察分析,回答下列问题:
| 甲 | 乙 | 丙 | 丁 | |
| 所取海水样品的质量/g | 100 | 100 | 100 | 300 |
| 加入AgNO3溶液的质量/g | 50 | 100 | 150 | 200 |
| 反应后所得的沉淀物的质量/g | 1.435 | 2.87 | 2.87 | 5.74 |
(1)两溶液恰好完全反应的是________________(填甲、乙、丙或丁)的实验。
(2)请计算海水中的氯化物(以氯化钠计算)的质量分数是多少。
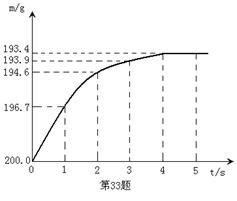 36、向盛有12.60g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应。反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示。烧杯连同药品的起始质量为200.0g。反应的化学方程式为:
36、向盛有12.60g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应。反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示。烧杯连同药品的起始质量为200.0g。反应的化学方程式为:
2NaHCO3+H2SO4 = Na2SO4 + 2H2O + 2CO2↑
回答下列问题:
(1)当碳酸氢钠与硫酸溶液恰好完全反应时,所需的时间约为 。
(2)当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为 。
(3)反应后,所得硫酸钠溶液的溶质质量分数为多少?
参考答案
一、选择题(每小题只有1个选项符合题意。每小题1.5分,本题共30分)
BBCDC DABAC ADBCD ADDAB
二、选择题(每小题有1~2个正确答案,全都选对得2分,若有两个正确答案的选对一个得1分,多选或选错不得分。每小题2分,共10分)
D B AC BD AD
三、填空题(本题共有4小题,共21分)
(2分)26. 相同 氧
(4分)27. CaCO3+2CH3COOH=(CH3COO)2Ca +H2O+CO2↑
Mg(OH)2+2 CH3COOH =(CH3COO)2Mg + 2H2O
|
(2) C+O2====CO2
(3)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
![]() 或者Na2CO3 +Ba(OH)2=BaCO3↓+2NaOH
或者Na2CO3 +Ba(OH)2=BaCO3↓+2NaOH
(4)CO +CuO====Cu +CO2
(7分)29(1)用化学式表示下列物质:
B: H2O C :CaO E:H2CO3
(2)书写下列变化的化学方程式
④Ca(OH)2+CO2 =CaCO3↓+H2O
⑥CaCO3+2HCl=CaCl2+H2O+CO2↑
四、简答题(本题共有2小题,共9分)
(5分)30.1g 1/58 1/20 1/8000 多次漂洗好
(4分)31.(1)酸 <
(2)酸溶液显酸性;酸性溶液不一定是酸溶液;有些盐溶液显酸性
(其他合理答案也可)
五、实验题(本题共有3小题,共17分)
(2分)32.(1)氢气还原氧化铜时,应先通入氢气,再点燃酒精灯加热氧化铜
(2)排水法收集氧气结束时,应先把导管移出水面,再熄灭酒精灯
(其他合理答案也可)
(9分)33.(1)长颈漏斗 酒精灯 (2)①> ②>
(3)BC Ⅱ CD Ⅱ中无白色↓产生 ; 无水CuSO4固体不变色
(6分) 34.
| 设想 | 实验内容 | 观察到的现象 | 解释或结论 |
| (1)是否酸溶液都可以使该花瓣变色呢 | (1)将其他酸溶液也分别滴到该花瓣上 | 花瓣的颜色也发生同样的改变 | 该花瓣可以用来检验某溶液是否是 酸 溶液 |
| (2)NaOH溶液是否也可以使花瓣变色呢? | (2)将NaOH溶液滴到该花瓣上 | 花瓣的颜色果然发生了不同于酸的改变 | NaOH溶液也可以使花瓣变色 |
| (3)是否所有碱溶液都可以使该花瓣变色呢? | (3)将其他碱溶液也分别滴到该花瓣上 | 花瓣的颜色也发生同样的改变 | 该花瓣可以用来检验某溶液是否是 碱 溶液 |
六、计算题(本题共有2小题,35题6分,36题7分,共13分)
35.(1)乙(2分)
(2)设NaCl的质量为X
NaCl+AgNO3=AgCl↓+NaNO3 (1分)
![]() 58.5
143.5
58.5
143.5
X 2.87g
58.5/143.5=X/2.87g (1分)
X =1.17g (1分)
(1.17g/100g)x100%=1.17% (1分)
答:海水中的氯化物(以氯化钠计算)的质量分数是1.17%
34. (1)4S (1分)
(2)CO2:200g-193.4g=6.6g (1分)
设反应生成的Na2SO4的质量为X
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑ (1分)
142
![]() 88
88
X 6.6g (1分)
142/88=X/6.6g
X=10.65g (1分)
10.65g/(12.6g+100.5g-6.6g)X100%=10.65g/106.5g X 100%=10% (2分)
答:反应后,所得硫酸钠溶液的溶质质量分数为10%