初三化学期中试卷
注意:(1)本卷分Ⅰ、Ⅱ两卷,考试时间为100分钟
(2) 请把所有答案写在答题卷中,做在试题卷中无效
(3)本卷可能用到的相对原子质量:H 1;C 12 ;N 14;O 16;S 32;Fe 56;Cl 35.5;K 39;Mn 55
Na 23;F 19;P 31;Al 27;Cu 64;Mg 24;Zn 65
Ⅰ卷选择题(本卷60分)
一、 单项选择题(本大题共30小题,每小题有且仅有一个答案,每题2分,共60分)
1.下列变化:1铜器在潮湿的空气中表面有铜绿生成;2水受热变成水蒸气;3静置使浑浊的河水变澄清;4火药爆炸;5充满氢气的气球升空后不久爆炸;6蜡烛燃烧,属于化学变化的是( )
A.1356 B.146 C.1456 D.2345
2.下列物质中属于纯净物的是( )
A.氮的质量分数为34%的尿素[CO(NH2)2] B.冰水 C.净化的空气 D.澄清石灰水
3.下列实验现象描述正确的是( )
A.铁在空气中燃烧火星四射
B.硫磺在氧气中燃烧产生无色无味的气体
C.红磷在空气中燃烧产生大量白雾
D.氢气在空气中燃烧,发出淡蓝色火焰
4.能使带火星的木条复燃的气体是( )
A.H2 B.N2 C.O2 D.CO2
5.下列仪器中,不能在酒精灯火焰上直接加热的是( )
A.蒸发皿 B.试管 C.燃烧匙 D.烧杯
6.在以下物质中:HNO3 N2O5 N2O3 NO2 NO N2 N2O NH3,氮元素化合价的种类为( )
A.五种 B.六种 C.七种 D.八种
7.在粗盐提纯实验中,不会用到下列仪器中的( )
A.漏斗 B.酒精灯 C.铁架台 D.试管
8.下列实验操作: 1充满氢气的集气瓶应用玻璃片盖住瓶口,正放在水平桌上;2加热时试管底部触及灯芯3实验室两个失去标签的试剂瓶中均装有白色固体,为了分清哪瓶是白砂糖,哪瓶是食盐,可取少量的固体品尝味道。4从试剂瓶中取出的药品,实验完后药品有剩余,为了节约,应放回原试剂瓶中。其中( )
A. 1正确 B. 13正确 C. 全部错误 D. 134正确
9.下列物质由原子直接构成的是( )
A.H2 B.NaCl C.Hg D.H2O
10.1998年中国十大科技成果之一是合成纳米氮化镓。已知镓(Ga)原子结构示意图为
![]()
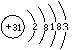 |
,氮原子结构示意图为则氮化镓的化学式是( )
A.Ga3N2 B.GaN C. NGa D.N3Ga2
11. 粗盐提纯实验中,四次用到玻璃棒,其作用依次是( )
A.搅拌、引流、搅拌、转移固体
B.引流、搅拌、转移固体、搅拌
C.搅拌、转移固体、搅拌、引流
D.引流、搅拌、搅拌、转移固体
12.我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量的新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的核外电子数为( )
A.115 B.49 C.66 D.164
13.用适量的H2还原CuO,实验完成后,经称量固体的质量减少了0.8克,则生成的铜的质量为( )
A.64克 B.6.4克 C.3.2克 D.32克
14.继通过食盐补碘在全国范围内基本实现消除碘缺乏病目标后,我国又将启动一项涉及千家万户营养健康问题的“补铁工程”。卫生部已批准以酱油为食物载体,逐步开展补铁工程。这里的碘、铁指的是( )
A.分子 B.原子 C.元素 D.单质
15.绿色燃料物质X,其燃烧反应的化学方程式为X+3O2 点燃2CO2+3H2O ,根据质量守恒定律判断:X化学式为 ( )
A.H2 B.CH4 C.CH3OH D.C2H5OH
16.下列化学方程式正确的是 ( )
A.H2O通电H2↑+O↑ B.S+O2SO2
C.2KClO3 MnO2△ 2KCl + 3O2↑ D.2Fe+3H2SO4=Fe2(SO4)3+3H2↑
17.30克由两种金属组成的混合物与足量的稀硫酸充分反应时可生成2克H2 ,则两种金属的可能组合是( )
A. Mg和Fe B.Zn和Cu C.Al和Mg D.Fe和Zn
18.某气体既能用排水法收集,又能用向下排空气法收集,该气体具有的性质是( )
A.易溶于水,比空气轻 B.难溶于水,比空气轻
C.易溶于水,比空气重 D.难溶于水,比空气重
19.X元素的核电荷数为b ,它的阳离子Xm +与Y元素的阴离子Yn –电子层结构相同,则Y元素的核电荷数为( )
A.b+m+n B.m+n-b C.b-m-n D.m-n-b
20.吸入“笑气”会使人发笑。该气体是由氮、氧两种元素组成的化合物,氮、氧元素的质量比为7 : 4,则它的化学式为( )
A.NO B.NO2 C.N2O D.N2O3
21.实验室用氢气还原氧化铜的主要实验步骤是①停止加热 ②停止通入氢气 ③给氧化铜加热④向试管里通氢气 ⑤氢气验纯。其操作顺序正确的是( )
A. ⑤④③①② B. ③⑤④②① C. ⑤④③②① D. ③⑤④①②
22.在下列化合物中,具有-1价原子团的是( )
A.Ca(OH)2 B.Fe2(SO4)3 C.K2MnO4 D.NH4Cl
23.氢气是一种绿色能源,科学家们最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气的新技术,其中海水分解可以用文字表达式表示为:水![]() 氢气+氧气。下列说法不正确的是( )
氢气+氧气。下列说法不正确的是( )
A.二氧化钛在反应中作氧化剂 B.水分解不产生污染物
C.二氧化钛在反应中作催化剂 D.该技术可以将太阳能转化为氢能
24.已知反应3A+2B=2C+D,A、B两物质完全反应时,质量比为3:4。若生成C和D共140g,则该反应消耗B的质量为 ( )
A.60g B.80g C.90g D.120g
25.在下列各组化合物中,前者是离子化合物,后者是共价化合物的一组是( )
A.KClO3 H2O B.NaCl O2 C.HCl K2SO4 D.ZnSO4 KCl
26.某+3价的金属元素M,在与氧形成的化合物中其质量分数为70%,则M的相对原子质量为( )
A.112 B.27 C.56 D.11
27.某学生用量筒量取液体,将量筒放平且面对刻度平视测量。初次视线与量筒内凹液面的最低处保持水平,读数为18 mL。倒出部分液体后,俯视凹液面的最低处,读数为5 mL,则该学生实际倒出液体的体积为( )
A.大于13mL B.小于13mL C.等于13 mL D.无法确定
28.已知一个CO2分子质量为n kg ,一个CO分子质量m kg ,则CO2的相对分子质量为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
29. “神舟五号”宇宙飞船飞行试验成功,表明我国载人航天技术有了重大突破。运送“神舟五号”飞船的火箭所使用的燃料是偏二甲肼(用R表示),在火箭发射时,偏二甲肼与四氧化二氮剧烈反应,产生大量气体并释放出大量的热,该反应的化学方程式如下:R+2N2O4![]() 3N2+2CO2+4H2O,下列说法正确的是( )
3N2+2CO2+4H2O,下列说法正确的是( )
A.偏二甲肼是由碳、氢两种元素组成的
B.偏二甲肼中含有氧
C.该反应是分解反应
D.偏二甲肼中碳、氢、氮三种元素的原子个数比为1︰4︰1
30.氧化银钮扣电池常用于手表和计算机,电池内的总反应可以表示为:Zn+Ag2O=ZnO+2Ag。下列说法错误的是( )
A.该反应属于置换反应
B.锌发生了氧化反应
C.氧化银发生了还原反应
D.锌元素的化合价降低,银元素的化合价升高
第Ⅱ卷非选择题
二.填空题(本大题共5小题,共20分)
31.用化学符号表示
⑴2个氢原子 ▲ ⑵2个氢分子 ▲ ⑶碳酸根离子 ▲ ⑷硫酸铝 ▲
⑸钙离子 ▲ ⑹氧化铁中铁元素的化合价 ▲ ⑺构成氯化钠晶体的阴离子是 ▲ ⑻保持水的化学性质的最小粒子 ▲
32.地壳中含量最多的非金属元素是 ▲ ,含量最多的金属元素是 ▲ ,(填元素符号)这两种元素形成的化合物化学式为 ▲ 。(填化学式)
33.现有A、B、C三种元素,A元素的原子核内只有一个质子;B原子核外有 2个电子层,第一层有2个电子、第二层有6个电子;C元素的原子失去2个电子后,形成离子的电子层排布与氖原子相同。
(1)写出A、B、C的元素符号:A ▲ B ▲ C ▲
(2)由A元素组成单质的化学式 ▲
(3)B与C形成化合物的化学式 ▲
34.配平下列反应方程式(反应条件已省略):
(1) ▲ NH3 + ▲ O2 →▲ NO + ▲ H2O
(2) ▲ C2H6O + ▲ O2 →▲ CO2 + ▲ H2O
35.某种牙膏中含有抗牙腐蚀的药物,化学式为Na2FPO3,已知F为-1价,其核电荷数为9,则该药物中磷的化合价为 ▲ ,该药物的相对分子质量为 ▲ 。
三.实验题(本大题共2小题,共10分)
36.实验室制取氧气的实验过程,大致可分为以下六步操作,正确的操作顺序是 ▲ 。
①点燃酒精灯,给试管加热;②熄灭酒精灯;③检查装置的气密性;④将氯酸钾和二氧化锰的混合物装入试管里,用带有导管的塞子塞紧,并将它固定在铁架台上;⑤用排水法收集氧气;⑥将导管 从水槽里取出。
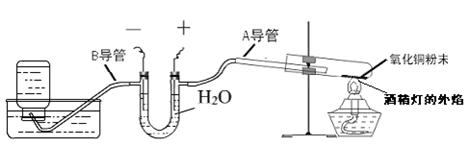 37.某同学设计了一套用电解水产生氢气还原氧化铜,并收集氧气的装置(见下图)
37.某同学设计了一套用电解水产生氢气还原氧化铜,并收集氧气的装置(见下图)
根据装置图回答:图中装置中的三处错误的是 ▲ ; ▲ ; ▲ 。电解水中正极与负极产生的气体的质量比为 ▲ ;氢气还原氧化铜的化学方程式为 ▲ ;实验现象为 ▲ 。
四.计算题:(本大题共2小题,共10分)
38.2001年诺贝尔化学奖授予美国化学家诺尔斯博士与日本化学家野依良治教授和美国化学家沙普利斯教授,以表彰他们催化不对称合成的重大成就。环氧化(R)——丙烯醇(化学式为:C3H6O2)是沙普利斯应用不对称合成技术合成的一种重要物质。该物质用于生产一种治疗心脏病的药物。试计算(计算结果保留一位小数):
(1)C3H6O2中碳、氢、氧三种元素的质量比。
(2)该物质中氧元素的质量分数。
39.在10克氯酸钾和二氧化锰的混合物中,含二氧化锰10%,加热后冷却,试管内的剩余固体中含二氧化锰为12.5%,求分解的氯酸钾占总氯酸钾的质量分数?