初三化学全真试题二
一、选择题(下列每小题只有1个正确选项)
1.日常生活中发生的下列变化,都属于化学变化的一组是( )
A.汽油燃烧,轮胎爆炸 B.湿衣服晾干,酒精挥发
C.菜刀生锈,牛奶变酸 D.铁制成铁锅,植物光合作用
2.市场销售的食盐种类有加钙盐、加锌盐、加碘盐等,这里的钙、锌、碘是指( )
A.分子 B.元素 C.单质 D.阴离子
3.蔬菜在生长的过程中,常喷洒农药防治病虫害,据有关专家介绍,用碱性溶液或清水浸泡,可使残留在蔬菜上的农药毒性降低。因此,买来的蔬菜在食用前最好用水浸泡一段时间,浸泡时可加入适量( )
A.纯碱 B.白糖 C.食醋 D.白酒
4.为适应火车提速,我国铁路主干线上原有的铁轨已全部连接为超长轨,工程技术人员常用如下反应来焊接钢轨间的缝隙:2Al+Fe2O3===Al2O3+2Fe,其中还原剂是( )
A.Fe B.Al2O3 C.Fe2O3 D.Al
5.A2+结构示意图为![]() ,则它的核电荷数及其氧化物的化学式分别是( )
,则它的核电荷数及其氧化物的化学式分别是( )
A.+12,AO B.+10,A2O C.+2,AO2 D.+12,A2O
6.下列说法中,正确的是( )
A.一种单质和一种化合物发生的反应一定是置换反应
B.由一种物质生成多种其它物质的反应一定是分解反应
C.物质跟氧气发生的反应不一定是氧化反应
D.生成盐和水的反应一定是中和反应
7.下列有关实验操作先后顺序错误的是( )
A.先检查装置的气密性,再装药品
B.制取O2结束时,先将导管移出水面,再熄灭酒精灯
C.点燃H2前,必须先检验H2的纯度
D.H2还原CuO完毕,先停止通H2,再熄灭酒精灯
8.依据反应:X+C===2Y和Fe2O3+3Y===2Fe+3X,推断X和Y各表示( )
A.CO和CO2 B.H2O和CO C.CO2和CO D.CO2和H2
9.现有a、b两种物质在室温下的饱和溶液,升高温度后,a溶液中有晶体析出,而b溶液还可以再溶解b晶体,则能正确表示a、b两种物质溶解度曲线的是( )
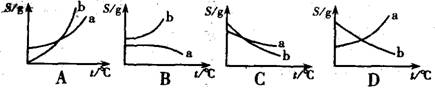
l0.用H2O作反应物或反应物之一,经过一步反应无法制得的物质是( )
A.H2 B.Ca(OH)2 C.P2O5 D.H2CO3
11.下列叙述不符合实验事实的是( )
A.未密封保存的苛性钠遇盐酸有气体生成
B.纯净的氢气在空气里燃烧,产生淡蓝色火焰
C.将Fe(OH)3加入滴有酚酞试液的蒸馏水中显红色
D.在Na2CO3、K2SO4、AgNO3三种溶液中滴入BaCl2溶液,都有白色沉淀生成
12.重铬酸钠(Na2Cr2O7)是一种常用的氧化剂,下列有关它的说法中正确的是( )
A.铬元素的化合价为+7 B.Na+电子数等于质子数
C.它是一种氧化物 D.它是一种正盐
13.某工厂排出含有少量氧化铜和锌粉的废渣和废盐酸混合形成污水,若向污水中加入足量铁粉,则处理后水中一定含有的金属离子是( )
A.Zn2+、Cu2+ B.Zn2+、Fe2+
C.Fe2+、Cu2+ D.只有Fe2+
14.下列括号中的物质是除去杂质所需的药品,其中错误的是( )
A.NaCl中有杂质Na2SO4(氯化钡)
B.FeSO4中有杂质CuSO4(铁粉)
C.CO2中有少量CO(灼热的氧化铜)
D.CO2中有少量HCl气体(氢氧化钠溶液)
15.在反应X+2Y=R+2M中,已知R和M的相对分子质量比为22:9,当1.6gx与Y完全反应后生成4.4gR,则此反应中Y和M的质量比为( )。
A.16:9 B.23:9 C.32:9 D.46:9
二、选择题(下列每小题有1-2个选项符合题意)
16.氢气、木炭粉、一氧化碳分别跟灼热的氧化铜粉末发生反应,下列叙述正确的是( )
A.反应类型均属置换反应
B.反应后都有红色固体物质生成
C.反应后都有二氧化碳气体生成
D.反应都是氧化还原反应
17.某绿色能源物质在氧气中燃烧生成水和二氧化碳两种物质,实验测得1.6g该物质在氧气中燃烧后生成4.4g二氧化碳和3.6g水,则该物质的组成是( )
A.含有碳、氧、氯三种元素 B.只含碳元素
C.只含碳、氢元素 D.无法判断
18.现有氢气和氧气共10g,点燃使之反应完全得到7.2g水蒸气,则反应前氧气的质量可能是( )
A.0.8g B.3.6g C.6.4g D.9.2g
19.下列各组溶液,不加其他试剂就能鉴别的是( )
A.Na2CO3、H2SO4、HCl、NaNO3 B.NaOH、NaCl、FeCl3、KNO3
C.HCl、AgNO3、HNO3、MgCl2 D.K2SO4、Na2CO3、BaCl2、HNO3
20.现有烧杯、试管、量筒、带铁夹的铁架台、酒精灯、集气瓶、玻璃片、水槽、带导管的橡皮塞,仅用这些仪器不能完成的实验是( )
A.制取氧气 B.粗盐提纯
C.制取二氧化碳 D.用氯化钠配制l00g 5%的氯化钠溶液
三、填空题
21.日常生活中许多现象与化学有着密切联系,请选择适当的物质填空:医用酒精的溶剂是_________;冬天用煤火取暖,若通风不畅会发生中毒,是由__________引起的。
22.把生石灰、二氧化碳、食盐分别溶于水,依次得到A、B、C三种溶液,它们的pH由大到小的顺序是(用A、B、C表示,下同)________________,分别向这三种溶液中滴加酚酞试液后,显红色的是__________溶液。
23.浓硫酸的质量分数为A,敞口放置一段时间后的质量分数为B,则A______B(填“>”、“<”或“=”,下同);浓盐酸的质量为A,敞口放置一段时间后,测得其质量为B,则A______B;V1mL水和V2mL酒精混合后溶液的体积____(V:+V2)mL;质量为A的铁片插人硫酸铜溶液中,一段时间后取出铁片,测得其质量为B,则A______B。
24.某同学做了如下家庭实验:在一个玻璃杯底部放入一支短蜡烛,并铺一层纯碱。点燃蜡烛后,沿玻璃杯壁倒人一些醋(主要成分是醋酸),可观察到的实验现象是____________________________和____________________________,说明二氧化碳具有的性质是_______________,由此可推出二氧化碳的用途之一是___________。
25.过氧乙酸(CH3COOOH)是一种广泛、高效的消毒剂,是预防非典型肺炎的首选产品。过氧乙酸中碳、氢、氧三种元素的质量比为______________________;某同学需要配制2240g 0.5%的过氧乙酸溶液,需要20%的过氧乙酸_________mL(此种过氧乙酸的密渡为1.12g/cm3)。
26.现有Zn、Ba(OH)2溶液、CuSO4溶液、稀硫酸四种物质,若各取少量两两混合,能发生的化学反应共有_________个,其中属于置换反应的有_________个。
27.某学校化学实验室的废液缸中盛有一种无色色溶液,可能含有Na+、H+、C1-、SO42-。现欲证明两种阴离子是否存在,请你帮助完成实验:取适量废液,先向其中滴加足量的_____________溶液,若有白色沉淀生成,则证明S042-存在;再取上层清液滴加_________溶液,又出现白色沉淀,则可证明C1-存在。
28.分别选用一种试剂,用化学方法除去下列物质中的杂质:Zn(NO3)2溶液中混有少量Cu(NO3)2,可选用_____________;NaCl溶液中混有少量Na2CO3,可选用___________
29.有A、B、C、D四种物质,它们之间有如下转化关系:
A+AgNO3→B↓+Ba(NO3)2;A+H2SO4→C↓+HCl;A+K2CO3一→D↓+KCl。
是推断:A是_________ B是_________ C是_________ D是_________
四、简答题
30.解释下列问题(用化学方程式表示):
(1)为什么在一些烟花和照明弹中含有镁粉?
 (2)为什么不用铝制容器盛放硫酸铜溶液?
(2)为什么不用铝制容器盛放硫酸铜溶液?
(3)为什么用盐酸可以除去铁锈?
31.右图是测定空气中氧气含量的实验装置,请根据实验回答问题
(1)可观察到的主要实验现象是什么?写出反应的化学方程式。
(2)燃烧后,钟罩内剩余的气体主要是氮气。请结合本实验推测氮气的物理性质和化学性质。
32.向盛有一种固态物质的试管中加入一种无色溶液,有气泡产生。试推测固态物质
可能是哪几种?相应加入的无色溶液分别是什么?(至少答出三种推测)
33.下表是空气中的气体成分和人体呼出的气体成分含量对照表
| 气体成分 | 氮气 | 氧气 | 二氧化碳 | 水 | 其他气体 |
| 空气中的气体(%) | 78 | 21 | 0.03 | 0.07 | 0.9 |
| 呼出的气体(%) | 78 | 16 | 4 | 1. 1 | 0.9 |
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入气体成分的含量有什么不同,其主要操作步骤如下图所示。
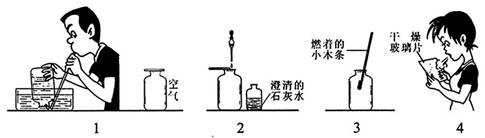
请依据图示将主要实验操作步骤及验证依据填人下表中:
| 实验步骤 | 验证依据 |
| 1. | |
| 2. | 根据___________________________________ 判断CO2含量不同 |
| 3. | 根据_________________________________ 判断O2含量不同 |
| 4. | 根据_________________________________ 判断水含量不同 |
五、计算题
34.常温下,将18.9g含有少量氯化钾的碳酸钾样品放人盛有185.5g稀盐酸的烧杯中,恰好完全反应,可得到200g不饱和溶液。求反应后所得溶液中溶质的质量分数。
参考答案
一、选择题(下列每小题只有1个正确选项)
1.C 2.B 3.A 4.D 5.A 6.B 7.D 8.C 9.B l0.C11.C 12.D 13.B
14.D 15.A
二、选择题(下列每小题有1-2个选项符合题意)
16.BD 17.C 18.CD 19.D 20.BD
三、填空题
21.水; 一氧化碳
22.A>C>B; A
23.>; >; <; <
24.有气泡产生; 片刻后蜡烛熄灭; 不支持燃烧; 灭火
25.6:1:12; 50
26.4; 2
27.Ba(N03)2;AgNO3
28.Zn; 盐酸(或氯化钡溶液等)
29.BaCl2; AgCI; BaS04 ; BaC03
四、简答题
30.(1)2Mg+O2![]() 2MgO;(2)2Al+3CuS04=3Cu+A12(S04)3;
2MgO;(2)2Al+3CuS04=3Cu+A12(S04)3;
(3)Fe203+6HCI= 2FeCl3+3H20
31.(1)红磷燃烧时有大量白烟生成,钟罩内水面上升,约占钟罩的1/5,
4P+5O2![]() 2P2O5
2P2O5
(2)物理性质:无色、不易溶于水;化学性质:氮气不与红磷反应(或氮气不支持燃烧)
32.推测一:BaC03 、稀盐酸;推测二:Zn、稀硫酸;推测三:CaC03、稀盐酸
33.(1)用排水集气法收集两瓶呼出的气体,另收集两瓶空气
(2)将澄清的石灰水分别滴入盛有呼出的气体和空气的集气瓶中;根据石灰水浑
浊程度的不同判断C02含量不同
(3)将燃着的木条分别放人盛有呼出的气体和空气的集气瓶中;根据木条燃烧情
况的不同判断O2含量不同
(4)取两块干燥的玻璃片,对着其中的一块呼气;根据玻璃片上水雾的不同判断水
含量不同
五、计算题
34.解:设混合物中K2C03的质量为x,反应后生成KCl的质量为y。
根据题意,反应后生成CO2的质量为:18.9g+185.5g一200g=4.4g
K2CO3+2HCl===2KCI+H2O十C02↑
138 149 44
x y 4.4g
138∶x=44∶4.4g x=13.8g
149∶y=44∶4.4g y=14.9g
反应后所得溶液中溶质的质量分数为:
![]()
答:反应后所得溶液中溶质的质量分数为10%。