九年级化学科酸碱盐达标检测
姓名: 成绩:
一、选择题:(每空2分,共20分)
1、农村有句谚语“雷雨发庄稼”,这是由于在放电条件下,空气中的氮气经过一系列复杂的化学变化,最后生成了易被农作物吸收的硝酸盐。雷雨给庄稼施加了( )
A、钾肥 B、磷肥 C、氮肥 D、复合肥
2、食用松花蛋时常感到有涩味,是因为制作过程中用到了熟石灰和纯碱等原料。为了减轻涩味,可在食用时添加调味品;这种调味品最好是 ( )
A.纯碱 B.白酒 C.白糖 D.食醋
3、下列物质在空气中质量会增加的是( )
A、稀硫酸 B、浓盐酸 C、氢氧化钾溶液 D、硝酸钠溶液
4、下列用途中,利用了物质化学性质的是( )
A、用稀盐酸除铁锈 B、用干冰作人工降雨剂 C、用金刚石切割玻璃 D、用活性炭吸咐毒气
5、下列各组气体中,均能用固体NaOH干燥的一组是( )
A、O2、CO、CO2 B、H2、O2、CO2 C、O2、SO2、HCl D、H2、O2、CO
6、为探究植物光合作用的实质,某校学生设计了如下实验装置(透明密闭).在阳光下,你预测数天后植物生长最茂盛的是( )
![]()
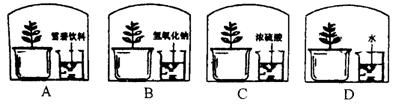
7、下列各组物质按氧化物、酸、碱、盐的顺序排列正确的是( )
A、MgO、H2SO4、Na2O、CaCl2 B、P205、NaHSO4、Ca(OH)2、KCl
C、MnO2、HNO3、KOH、K2CO3 D、CH3OH、CH3COOH、C2H5OH、CH4
8、用下列溶液分别滴入NaOH溶液、Ca(OH)2溶液、稀H2SO4中,产生三种不同现象的是( )
A、FeCl2溶液 B、KNO3溶液 C、Na2CO3溶液 D、无色酚酞试液
9、已知草木灰是农村常用的农家肥,其中草木灰中含有K2CO3,是碱性物质。下列化肥中,能与草木灰混合施用的是( )
A、NH4HCO3 B、KNO3 C、NH4NO3 D、过磷酸钙
10、下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
A、氧化铜和木炭粉 B、硝酸钾和硝酸钠 C、水和酒精 D、碳酸钠和碳酸钙
二、填空题:(方程式每条2分,其余每空1分,共22分)
11、一些食物的近似PH如下表:
| 食物 | 苹果 | 葡萄 | 牛奶 | 玉米 |
| PH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 6.8~8.0 |
(1)苹果汁和葡萄汁相比较,酸性较强的是__________,它能使石蕊试液变_______色。
(2)人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用的食物是_________。
(3)鸡蛋壳中含有CaCO3,以前因胃酸过多导致胃痛时,有人吃鸡蛋壳粉,其原因是(用化学方程式表示)___________________________________。现今,许多冶疗胃酸过多的药品的有效成分是氢氧化铝,而不是CaCO3,提出一种理由说明为什么氢氧化铝优越于碳酸钙:
_____________________________________________________ _____________。
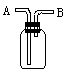 12、右图所示装置有多种用途,请回答下列问题:
12、右图所示装置有多种用途,请回答下列问题:
(2)洗气:除去CO2中的水蒸气,装置内应盛的物质是___________;
(2)检验:证明CO中混有CO2,装置内应盛____________________;
(3)贮气:若用排空气法收集H2时,气体应从装置的___ _端通入(填A或B,下同);若用排水法收集O2时,瓶内先装满水,气体从___ _端通入;若要用水将装置中的氧气排出进行实验时,水应从__ ____端通入。
13、烧碱在空气中很容易变质。现把在空气中已全部变质的烧碱少许加入稀盐酸中,观察到的现象是 ,反应的化学方程式为:
14、氯气(Cl2)和氧气一样,都是活泼的非金属单质。甲烷和氧气反应的化学方程式为:CH4+2O2![]() CO2+2H2O 。在一定条件下,甲烷和充足的氯气可反应,请推测并写出甲烷和氯气反应的化学方程式:
。
CO2+2H2O 。在一定条件下,甲烷和充足的氯气可反应,请推测并写出甲烷和氯气反应的化学方程式:
。
15、从C、H、Cl、O、Ca五种元素中选择适当元素,组成符合下列要求的物质(填化学式)。
(1)可于人工降雨的氧化物 (2)可用于金属表面除锈的酸
(3)可改良酸性土壤的碱 (4)可用作建筑材料的盐
(5)可作食品干燥剂的金属氧化物 (6)可用作调味剂的物质
三、简答题:(共42分)
16、有失去标签的六瓶溶液:HCl、Na2CO3 、Ba(NO3)2 、Na2SO4 、NaNO3.将其任意编号,进行两两混合,其现象如下表:
| 实验 | A+D | A+B | B+C | A、B、C、D分别与E |
| 现象 | 产生气体 | 产生沉淀 | 产生沉淀 | 无现象 |
(1)写出各物质的化学式:
A、 ; B、 ; C、 ; D、 ; E、 。
(2)写出有关反应的化学方程式
A+D B+C
17、试用两种方法区别澄清石灰水和氢氧化钠溶液:
| 实验方法 | 所选用的试剂 | 现象及结论 |
| 方法一 | ||
| 方法二 |
四、实验题:
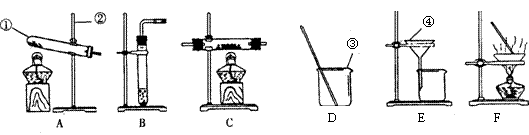
18、某同学为制备纯净干燥的氢气,准备了下图所示的A、B、C三种装置。其中A装置最大的特点是可以随时使反应发生或停止。
(1)装置A中发生反应的化学方程式为 ;
(2)关闭弹簧夹时,A内的反应随即停止是因为
(3)装置B的作用是 ,装置C的作用是 ;
(4)为制备纯净干燥的氢气,A、B、C三种装置的连接顺序为 → →
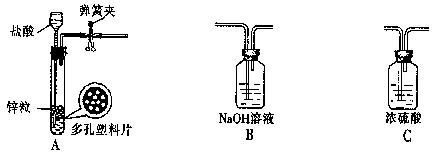
 19、现有下图所示的实验装置:
19、现有下图所示的实验装置:
(1)A装置可用于(填一个具体实验名称,下同) 的实验。
B装置可用于 的实验。
(2)现有稀H2SO4、CuO、Fe粉3种物质,请设计两种制取铜的实验方案。填写下表。
| 实验方案 | 有关反应的化学方程式 | 选用装置(填字母代号) |
| 方案一 | ① ② | |
| 方案二 | ① ② |
五、计算题:(共16分)(相对原子质量:C 12、 O 16、 N 14、 S 32、 Na 23、 Ca 40 )
20、(8分)蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应,生成氨基酸,蛋氨酸(C5H11O2NS)就是其中一种。
(1)蛋氨酸中各元素的质量比C:H:O:N:S=
(2)蛋氨酸中氮元素的质量分数为
(3)检验蛋白质的一种简单方法是
(4)合格奶粉每100g中含蛋白质约18g,蛋白质中氮元素的平均质量分数为16%,则每100g合格奶粉中氮元素的质量为
g。现测定某奶粉每100g中氮元素的质量为0.5g。则这种奶粉属于
(填“合格”或“不合格”)奶粉。
21、(8分)某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗100kg的这种石油产品,需要多少千克的NaOH?
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理100kg这种产品,可以节约多少经费?NaOH和Ca(OH)2的市场价格如下表:
| 名 称 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 6.00 | 24.00 |