九年级化学质检试卷(一)
(考试时间:80分钟 满分:100分)
班级 坐号 姓名 成绩
可能用到的相对原子质量C:12 H:1 O:16 N:14 Cu:64 Fe: 56 Al: 27
一、 选择题(本题包括15小题,每小题2分,共30分,每小题只有一个选项符合题意,将它的编号填入相应的括号中。)
1.下列变化不属于化学变化的是: ( )
A.光合作用 B.高炉炼铁 C.煤气中毒 D.粉碎矿石
2.日常生活常见的下列物质,属于有机物的是: ( )
A.白酒 B.不锈钢窗 C.大理石 D.冰水混合物
3.自来水生产中通常使用少量的氯气进行消毒,氯气与水反应的产物之一是盐酸,市场上有些不法分子高牟取暴利,用自来水冒充纯净水出售,为辨别真伪,可用来鉴别的:( )
A.酚酞 B.BaCl2 C.NaOH D.AgNO3
4.为了验证Fe、Cu、Ag三种金属的活动性顺序,现有所需金属,如果只选一种盐且实验最简单的是: ( )
A.AgNO3 B.CuSO4 C.FeSO4 D.ZnCl2
5.下列各组物质能在PH= 12的溶液中能大量共存的是 ( )
A.Na2CO3、NaOH、CaCl2
B.CaCl2、NaCl、KNO3
C.NaOH、Na2SO4、H2SO4
D.NaNO3、FeCl3、CuSO4
6.下列化肥属于复合肥料的是 ( )
A.CO(NH2) B.Ca(H2PO4)2 C.KNO3 D.KCl
7.元素之间最本质的区别在于 ( )
A.质子数不同 B.核外电子数不同
C.电子层数不同 D.最外层电子数不同
8.某温度时,将KCl的饱和溶液11.2克,蒸于后得到3.2克KCl固体,则该温度时KCl的溶解度为
( )
A.8.0克 B.28.6克 C.40.0克 D.71.4克
9.缺碘易使人患甲状腺亢进,因此在食盐中一般都加入碘酸钾这种物质。在碘酸钾中碘的化合价为+5价,而碘酸钾的化学式为 ( )
A.KIO B.KIO2 C.KIO3 D.KIO4
10.在Cu(NO3)2和Mg(NO3)2的混合溶液中,加入过量的铁粉,充分反应后过滤,留在滤纸上的物质是 ( )
A.Cu和Mg B.Fe(NO3)2和Mg(NO3)2 C.Fe和Cu
D.Cu
11.下列食品中蛋白质含量最高的是 ( )
A.米饭 B。黄瓜子 C。虾 D。面条
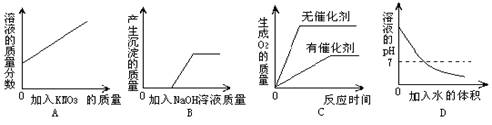
12.下列四个图像反映的变化趋势,分别对应四种操作过程,其中正确的是 ( )
A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B. 向氯化铁和盐酸的混合溶液中加入过量的氢氧化钠溶液
C.用相等质量的双氧水来制取氧气 D.氢氧化钠溶液中加足量的水稀释
13.“耐高温长寿命抗氧化陶瓷基复合材料应用技术”获2004年度国家技术发明一等奖。下列日常生活中的物品也属于“复合材料”的是: ( )
A.机动车的轮胎 B.玻璃
C.钢筋 D.农业上施用的复合肥
14.区别空气、氧气和二氧化碳三瓶无色气体最简便的方法是 ( )
A.把燃着的木条分别伸进三瓶气体中 B.分别将三种气体通人滴有石蕊的水中
C.分别将少量的澄清石灰水倒入三种气体中 D.通过实验测定气体在水中的溶解性
15.将一块部分变成铜绿[Cu2(OH)2CO3]的铜块研磨成粉末,在空气中充分灼烧成CuO,固体质量的变化情况可能是( )
A.增重30% B.增重10% C.减轻40%. D.减轻30%
二、(本题包括8个小题,共35分)
16.(5分)在横线上填写相应的符号:一个氮分子____,2个氢原子____,3个硫酸根离子____,+2价的镁元素 钙离子____。
17.(2分)某三价金属的氧化物中,金属元素与氧元素的质量比为9∶8,则该金属氧化物的名称是____。
18.(4分)有C、H、Cl、O、Na五种元素,请选用这五种元素中一种或几种写出符合下列要求的物质(用化学式表示)。
(1)实验室常用来制取CO2气体的酸_____
(2)生活中常用于调味和腌渍蔬菜、鱼、肉等食物的盐_____________
(3)地壳中含量最多的元素组成的单质_________
(4)天然气的主要成分_____________
19.(4分)烧碱(Na OH)属于 类物质(填“酸”、“碱”或“盐”)。向烧碱的水溶液中滴入酚酞试液,试液变 色,说明烧碱溶液呈 性,其pH 7(填“=”、“<”或“>”。
20.(6分)对知识的归纳和整理是学习化学的一种重要方法。现有三个化学反应如下:
1 C+O2 点燃 CO2 2 2H2+O2 点燃 2H2O
3 2Mg+O2 点燃 2MgO
通过比较可以发现它们有许多相似之处:
其一是___________________ 其二是_________________ _
请你另外写出一个符合这两点的化学方程式:___________________
21.(6分)甲、乙、丙是三种单质,其中甲、丙是固体,乙是气体;A、B、c、D、E都是化合物,其中E是B的水溶液,常存在于大量燃烧煤所导致的酸雨中,而很多建筑物因含有D,易受酸雨的侵蚀。上述物质的相互转化关系如下图所示(部分产物已略去):
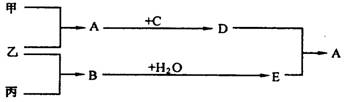 |
(1)写出下列物质的化学式:A____________,D______________;
![]() (2)写出反应乙+丙 B的化学方程式:_____________________________________。
(2)写出反应乙+丙 B的化学方程式:_____________________________________。
22.(3分)医疗用的碘酒是把碘溶解于酒精制成的,其中____是溶质,____是溶剂,碘酒是____。
23.(3分)稀释浓硫酸时,一定要把____沿着器壁慢慢地注入____,并不断搅动,使产生的热量迅速地扩散。切不可____。
三.实验题(本题包括2个小题,共22分)
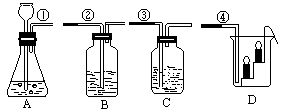
24.(12分)实验室按下图所示装置制取CO2,并检验CO2的性质。试回答以下问题:
(1)实验开始前,先应检查装置A的____ 。
(2)用装置A来制取CO2,所用的药品是____ 。(写化学试)
(3)若要用装置B鉴定CO2,在B中应盛放的试剂名称是____,当将标①和②的导管口连接时,B中看到的实验现象是____
。
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是____,当将标①和③的导管口连接时,C中看到的实验现象是____
。
(5)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是____
。
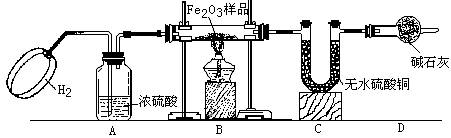
25.(10分)某中学化学兴趣小组利用下图所示装置测定样品中Fe2O3(样品中杂质高温下不分解,也不参加反应)的质量分数,回答下列问题。
 |
。
(1)实验开始时,应先挤压鼓气球持续一段时间,其目的是
。
(2)A装置的作用是 ;反应进行一段时间后C装置中的现象是 。
(3)反应前准确称量样品的质量为5g,完全反应后C装置增加了1.35g,则样品中Fe2O3的质量分数为 。
(4)若省去D装置,则实验所测定的样品中Fe2O3的质量分数比实际的质量分数会
(填“偏大”“偏小”或“不变”)。
六、计算题(本题包括2个小题,共13分)
26.(6分)今年2月,在某些蕃茄酱、辣椒酱等食品发现含有一种色素苏丹红(C16H12N2O),它能造成人体内肝脏细胞的DNA突变,显现致癌的特性,目前多数国家已禁止其作为食品添加剂使用。试求:(1)苏丹红的相对分子质量,(2)苏丹红中C、H、N、O四种元素的质量比,(3)苏丹红中氮元素的质量分数。
27.(7分)取10 gCO和CO2的混合气体,缓慢通过过量的石灰水,充分反应后,过滤得干燥的固体10g。求:(1)原混合气体中CO2的质量,(2)原混合物气体中CO和CO2所含碳原子个数比。