金属的化学性质(1)
1.过量的铁粉跟一定量的硫酸铜溶液反应后过滤,滤液中含有的溶质是・・・・・・・・・・・・・・・ 【 】
A.CuSO4 B.FeSO4
C.CuSO4和FeSO4 D.Fe2(SO4)3
2.镁带在空气中燃烧、铁丝在氧气中燃烧、铜在空气中加热,这三个反应的共同之处是 【 】
A.都生成黑色固体 B.都有火星四射现象
C.镁、铁、铜都是氧化剂 D.都是化合反应
3.用铁和铝分别跟足量的稀硫酸反应。若要制得相同质量的氢气,则需要用去铁和铝的质量比是 【 】
A.28:27 B.28:9 C.56:27 D.112:81
4.已知Fe、Cu、Ag三种金属的活动性由强到弱的顺序是Fe>Cu>Ag。则下列各组物质间能发生反应的是 【 】
A.Fe和CuSO4溶液 B.Ag和FeSO4溶液
C.Cu(NO3)2和Ag溶液 D.Cu和FeSO4溶液
5.下列金属中,导电性能最强的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.铜 B.铝 C.银 D.金
6.下列各金属可以跟盐酸反应的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
①Zn ②Fe ③Ag ④Cu ⑤Al
A.①②③, B.①②⑤ C.①③④ D.①③⑤
7.下列反应属于置换反应的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.NaOH+HCl→NaCl+H2O B.Cu(OH)2→CuO+H2O
C.CO+CuO![]() Cu+CO2 D.Cl2+2KI→I2+2KCl
Cu+CO2 D.Cl2+2KI→I2+2KCl
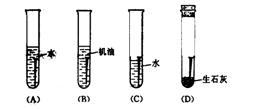
8.在下列条件下,铁钉最容易生锈的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
9.在硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出。则析出的少量金属是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.Cu和Fe B.Ag C.Cu D.无法确定
10.下列关于生铁的叙述中,错误的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.生铁的含碳量大于钢 B.生铁的熔点低于纯铁;
C.生铁可以锻造不可铸造 D.生铁是铁的合金。
11.将下列各组药品进行实验,能判断出铁比铜活泼的一组・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.Fe、Cu、稀H2SO4 B.Fe、Cu、ZnSO4溶液
C.Fe、Cu、AgNO3溶液 D.Fe,Cu、FeSO4溶液
12.在氧化铜和铁粉的混合物中加入一定量的稀硫酸,并微热,反应停止后滤出不溶物;向滤液中插一枚铁钉,未发觉变化。据此下列结论正确的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.滤出的不溶物一定含有铁 B.滤出的不溶物一定含有铜
C.滤出的不溶物一定含有铁和铜 D.滤液中一定含有硫酸亚铁,可能含有硫酸铜。
13.我国古代的“药金”外观和黄金相似,经常被误认为金子其冶炼方法为(ZnCO3)、赤铜(Cu2O)和木炭混合的物质加热至800℃左右,即得到金光闪闪的“药金”。试推断“药金”组成・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.Zn B.Cu C.Zn、C D.Zn、Cu
14.质量为5.6克的铁粉中混有一种金属杂质,当这些铁粉跟足量的盐酸完全反应后,生成氢气0.19克,则该铁粉中可能混有・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.镁 B.铝 C.锌 D.钙
15.现有等质量的①铁粉、②镁粉、③锌粉,分别跟同浓度的盐酸反应,它们的反应速率由快到慢的顺序是 【 】
它们产生氢气由多到少的顺序为・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.①>②>③ B.②>①>③ C.③>②>①; D.②>③>①
16.天平两端分别放置盛有足量盐酸的烧杯,把天平调至平衡,现向其中一只烧杯中投入5.3克Na2CO3,向另一只烧杯中投人适量铁片,如果要使天平最终保持平衡,投入铁片的质量是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.5.6克 B.5.3克 C.3.2克 D.3.9克
17.相同质量的金属镁、铁、锌、铝跟足量的盐酸反应,生成氢气最多的是・・・・・・・・・・ 【 】
A.镁 B.铁 C.锌 D.铝
18.在托盘天平两盘上各放一只烧杯,两烧杯中盛有等质量、等质量分数的足量盐酸,使两边保持平衡。此时向左盘烧杯中加入10克CaCO3,若要使天平再次保持平衡,需向右中加入CaO的质量是・・・・・・・・・・・ 【 】
A.10克 B.5.6克 C.2.2克 D.14.4克
19.下列置换反应正确的是・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 【 】
A.Cu+2HCl![]() CuCl2+H2
CuCl2+H2![]() B.2Al+6HCl
B.2Al+6HCl![]() AlCl2+3H2
AlCl2+3H2![]()
C.Fe+2HCl![]() FeCl2+H2
FeCl2+H2![]() D.Mg+HCl
D.Mg+HCl![]() MgCl2+H2
MgCl2+H2![]()
二、填空题
20.地壳中含量最多的金属以___________(填游离或化合)态存在。它与地壳中含量最多元素及空气中含量最多的元素一起形成化合物,其化学式为_________________________。
21.我国从西汉时期就开始冶炼铜,方法是先用硫酸与氧化铜反应,再用铁置换出铜,称为“湿法炼钢”。写出上述两步反应的化学方程式________________________________,
_________________________________氢气还原氧化铜也可以得到铜,发生反应的化学方程______________________________________________________________________。
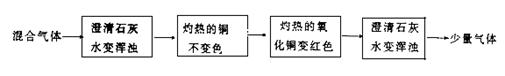
22.某混合气体中可能含有N2、O2、CO和CO2中的一种或几种,将混合气体依次通过装置(假设每次都反应完全),发生相应的变化如下:据上述现象,可推断该混合气体中一定含有
___________________________________,一定没有________________________________。
23.把足量的稀硫酸加入到盛有铝粉、铁粉和铜粉的混合物中,经充分反应后过滤,滤液中
的固体物质是__________(填化学式),滤液中溶质是______________________(填化学式)。
反应的化学方程式是:(1)___________________________(2)_________________________
24.在托盘天平左右两边盘上放甲、乙两只烧杯,并调节平衡,在烧杯中分别注入等质量等质量浓度的稀H2SO4,再在甲烧杯中放入m克锌,在乙烧杯中放人m克铁。
1)若反应后两个烧杯中的金属完全溶解,则天平指针_____________(填“不偏向甲”或“偏向乙”),其理由是_______________________________________________________________
(2)两烧杯中两种金属都有剩余,则天平指针____________________________,理由是_________________________________________________________________
(3)若两烧杯中一种金属有剩余,一种金属完全溶解,则剩余的金属是________________。
三.实验题
25.试设计两种不同类型的简便方法,证明铁与铜的性质活泼。除铁、铜之外,每种方使用试管和一种试剂。
方案1:________________________________________________________________________
方案2:________________________________________________________________________
26.黄金饰品中的假货常常鱼目混珠。社会上有些不法分子时常以黄铜冒充黄金进行诈骗。因为黄铜(铜、锌合金)单纯从颜色、外形上看,与黄金极为相似,所以很难区分。设计一个实验方案(化学方法)鉴别真假黄金,要求写出实验方法、现象和结论。
| 实 验 步 骤 | 实 验 现 象 | 结论 | |
| Ⅰ | |||
| Ⅱ |
 27.某废液中含有ZnCl2、FeCl2、和CuCl2,要从中全部回收金属铜。某化学兴趣小组的同学先加入稍过量的铁粉,充分反应后过滤,滤渣中含有_____________,如何用化学方法继续实验得到纯净的金属铜,请写出简要的实验步骤(包括加入试剂和操作方法)
27.某废液中含有ZnCl2、FeCl2、和CuCl2,要从中全部回收金属铜。某化学兴趣小组的同学先加入稍过量的铁粉,充分反应后过滤,滤渣中含有_____________,如何用化学方法继续实验得到纯净的金属铜,请写出简要的实验步骤(包括加入试剂和操作方法)
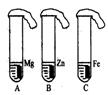
28.一般情况下,金属越活泼,与酸反应的速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下的实验.
[实验步骤]:
①取A、B、C三支试管,分别加入2mL浓度相同的盐酸溶液,
②分别加入足量的、大小相等的Mz、Zn、Fe,立即把三个相同的气球分别套在各试管口上.
[实验预测与分析]
(1)写出铁与盐酸反应的化学方程式:__________________
(2)气球膨胀速度最快的是_______________________(填试管编号)
(3)该实验表明,实验室一般选用锌而不选用镁、铁制取氢气的主要原因是:__________________________________________________________________________
 (4)步骤②是实验获得成功的关键,你认为在操作过程中小组成员之间应该:__________________________________________________________________________
(4)步骤②是实验获得成功的关键,你认为在操作过程中小组成员之间应该:__________________________________________________________________________
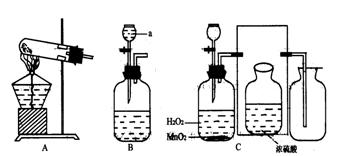
29.实验室常用氯酸钾晶体和二氧化锰粉末制取氧气(装置A),也可用过氧化氢溶液和催化剂二氧化锰粉末来制取氧气(装置B).装置B中的仪器a是分液漏斗,通过活塞的“开”、“关”可以随时滴加过氧化氢溶液,从而控制得到氧气的量。
(1)写出一种实验室制取氧气的化学方程式:________________________________
(2)从反应物状态和反应条件来比较装置A和B的差异:
| 装置A | 装置B | |
| 反应物状态 | ||
| 反应条件 |
(3)用装置B制得的氧气带有少量水蒸气,可用浓硫酸除奉水蒸气,请在C图方框中添上带橡皮塞的玻璃导管,完成除去水蒸气的实验装置图
(4)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收集满.这是利用了氧气的______________,______________性质.
四、计算题
30.用有一黄铜样品粉末(铜和锌的合金)19.5克,溶于足量的稀硫酸中,放出氢气2升(标准状况)。氢气在标准状况下的密度是0.09克/升。求黄铜样品中铜的质量分数。
31.还原1克氧化铜所需要的氢气,至少需要多少克含杂质5%的锌跟足量的稀硫酸反应才能获得?