初三化学学情调研题
可能用到的原子量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cu-64 Fe-56 K-39 Ca-40 Cl-35.5
一、选择题(每小题3分;。本题共33分)
1、等质量、等质量分数的盐酸和氢氧化钠溶液相混合后,再滴加石蕊试液,此时溶液显示:( )
A.蓝色 B.红色 C.紫色 D.无色
2、下列物质长期露置空气中会变质的是: ( )
A.食盐 B.浓盐酸 C.浓硫酸 D.烧碱
3、有甲、乙、丙三种金属,将甲、乙分别放入丙的硝酸盐溶液中,甲的表面有丙析出,乙无明显变化,则三种金属的活动性顺序是: ( )
A.甲>乙>丙 B.甲>丙>乙 C.丙>甲>乙 D.丙>乙>甲
4、要使不饱和的石灰溶液变成饱和的溶液,可采用的方法是( )
① 升温 ②降温 ③加水 ④加熟石灰
A ④ B ① C ① 和 ④ D ② 和 ④
5.要鉴别AgNO3、CaCl2、Na2CO3三种无色溶液,最好选用下列哪一种试剂:( )
A.H2SO4 B.NaOH C.BaCl2 D.HCl
6 、下列化肥中,氮元素质量分数最大的是: ( )
A.(NH4)2SO4 B.NH4NO3 C.CO(NH2)2 D.NH4HCO3
7 、试管内壁残留有下列物质,不能用稀盐酸浸泡除去的是: ( )
A.盛过石灰水后留下的白色固体。
B.硫酸铜溶液与氢氧化钠溶液反应后留下的蓝色固体。
C.盛放过生锈铁钉后留下的棕色固体。
D.用氢气还原氧化铜后留下的一层金属铜。
8、把t10C 和 T20C (t1 > t2 )时硝酸钾饱和溶液各100g蒸干,分别得到硝酸钾固体mg和ng ,m和n的关系是( )
A、m=n B、m>n C、m<n D、不能确定
9、下列各组物质可以大量存在于同一溶液中的是:( )
A、NaOH MgSO4 NaCl、 B、 BaCl2 Na2SO4 KNO3
C、AgNO3 HCl CuSO4 D、H2SO4 Cu(NO3)3 NaCl
10、用Mg、MgO、MgCO3、HCl、CuCl2来制取MgCl2的方法有: ( )
A.2种 B.3种 C.4种 D.5种
11、要除去CaCl2溶液中混有的少量HCl ,加入过量下列物质,其中最合理的是:( )
A、CaCO3 B、Ca(OH)2 C、CaO D、AgNO3
二、填空题(每空1分 ,共30分)
12、含有水蒸气、二氧化碳等气体的空气,通过氢氧化钠溶液时___________被吸收了,再通过浓硫酸时_________被吸收了,最后通过灼热的铜丝网________________被吸收了,最后剩余的气体是________________。
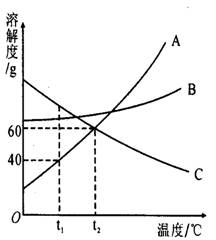 13、如图是A、B、C三种物质的溶解度曲线。 请回答:
13、如图是A、B、C三种物质的溶解度曲线。 请回答:
⑴ 、t10C时A、B、C三种物质的溶解度由大 到小的顺序是 ;
⑵、当A中混有少量B时,可用 方法提 纯A;
⑶、在t10C时,将25gA物质加入到盛有50g水的烧杯中,充分搅拌;再升温至t20C(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是 。
14、把镁粉和铁粉同时投入盛有CuSO4溶液的试管中,充分反应后过滤,固体中发现有镁粉剩余,则滤液中存在的阳离子有 ,所得固体除镁外,还有 。
15、按下列要求,从(A)烧碱、(B)浓盐酸、(C)熟大灰、(D)大理石、(E)浓硫酸中选出适当的物质,将所选物质的标号填在相应的空格上:①能跟活泼金属反应,并可在空气中形成白雾的是: ;
②可用于砌砖,抹墙和降低土壤酸性的是: ;
③固体可用于CO2气体的干燥剂,具有强烈腐蚀性的是: ;
④作为矿物存在于自然界中,可用作建筑材料和生产水泥的原料的是: 。
![]() 16、已知下列物质反应:① A + B → C + H2O,② C + NaOH → D↓(红褐色) + E,③ D → B + H2O,④ E + BaCl2
→ F↓+ NaCl (F不溶于稀HNO3),根据以上关系写出A、B、C、D、E、F六种物质的化学式(1)、A B C D E F
16、已知下列物质反应:① A + B → C + H2O,② C + NaOH → D↓(红褐色) + E,③ D → B + H2O,④ E + BaCl2
→ F↓+ NaCl (F不溶于稀HNO3),根据以上关系写出A、B、C、D、E、F六种物质的化学式(1)、A B C D E F
(2)、写出②和④的化学方程式:(4分)
② ;④ ;
17、为了检验CO2中是否混有氢气和一氧化碳,某同学设计如下实验装置:
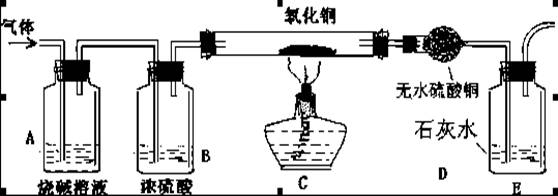
装置A的作用是_________________,装置B的作用是_________________
如果原气体中混有氢气,则装置C中出现的现象是_____________________,
而D中的现象是_______________________,
如果D装置中无明显现象发生,装置E中却有白色沉淀生成,则气体中一定混________________。
由于一氧化碳具有___________性,为了防止污染环境,所以E装置出来的气体应如何处理?_________________________________________________。
三、计算题(7分)
18、有碳酸钾与氯化钙的混合物49.8克,在40℃的条件下加入一定量的水搅拌后恰好完全反应,过滤后将滤渣洗涤、干燥后称重,其质量为20克,所得滤液104.3克,恰好是该温度下的饱和溶液。计算(1)混合物中碳酸钾的质量分数;(2)生成溶液溶质的质量分数。(7分)