初三化学第八章 1―4节测试题(原创1)
相对原子质量:Na―23;O--16;H―1;Cl―35.5;Ba―137;S―32;C―12;Fe―56;
K―39;Ag―108;Zn―65。
一、 选择题:(共15小题,共30分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
1、我省某些山地土壤浸出液的pH约为4,这种土壤对农作物生长不利,现要改良它,可以施用下列物质中的-------------------------------------------( ) A 石灰石 B 氯化钙 C 熟石灰 D 硝酸钾
2、下列物质变化属于化学变化的是------------------------------------- ( )
A 氯化氢溶于水 B 氯化钙潮解 C 二氧化碳制干冰 D 盐酸除锈
3、下列各组物质都属于混合物的是--------------------------------------( )
A、 盐酸、稀硫酸 B氯化钠 、蔗糖水 C 、生石灰、石灰石 D、氯化氢、澄清的石灰水
4、下列物质放入水中,能电离出大量氯离子的是----------( )
A、 氯酸钾 B、氯化银 C、 氯化氢 D、碳酸钙
5、下列物质贮存在敞口容器中质量会增加、变质的是------------------------------------( )
① 浓盐酸 ②浓硫酸 ③氢氧化钠 ④氢氧化钙 ⑤浓硝酸 ⑥氯化钠
A ①⑤⑥ B ②③④ C ①⑤ D ③④
6、在盛有少量稀盐酸的试管里,滴加硝酸银溶液和几滴稀硝酸,观察到的现象是( ) A 红褐色沉淀; B 蓝色沉淀 C 白色沉淀 D 无明显现象
7、根据下列物质的名称或俗称,判断属于同一种物质的一组是--------------- ( ) A氢氧化钙、碳酸钙 B生石灰、熟石灰 C甲烷、水煤气 D烧碱、苛性钠
8、下列有关叙述,正确的是 ---------------------------------------------( ) A 凡是能电离出氢离子的化合物都是酸. B 酸、碱、盐都能溶于水
C 碱性氧化物都是金属氧化物 D 非金属氧化物都是酸性氧化物
9、下列各组金属的活动性符合由强到弱顺序排列的是----------------------( ) A Fe、Cu 、Zn B Zn、Fe、Cu C Cu、Fe、Zn D Zn、Cu、Fe
10、下列各组物质中,能相互反应并生成无色盐溶液的是--------------------( )
A 氧化铜与稀盐酸 B铜与稀硫酸 C 氢氧化铜与稀硫酸 D 碳酸钠溶液跟盐酸
11、下列物质放入滴加了酚酞试液的水中,能使其变红的是----------------------------- ( )
①氢氧化钙②氢氧化镁③氧化铜④氯化钠溶液 ⑤烧碱溶液⑥氨水⑦盐酸⑧二氧化硫
A ①②③⑤⑥ B ④⑦⑧ C ①②⑤⑥ D ①⑤⑥
12、只用一种试剂就可以把盐酸、氢氧化钠溶液、澄清石灰水一一区别开的试剂是( )
A 石蕊试液 B 碳酸钾溶液 C 二氧化碳 D 硝酸银溶液 (1)
13、把下列各组物质的溶液相混和,再加足量盐酸,有沉淀生成的是-----------( )
A FeCl3和NaOH B HNO3和AgNO3 C Na2CO3和NaNO3 D CuCl2和HNO3
14、将20克20%的氢氧化钠溶液和20%的盐酸混和后,溶液的pH等于7,则盐酸的质量
为 --------------------( )A 18.25克 B 20.00 克 C 36.50 克 D 3.60克
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 15、如图所示,向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,直至恰好完全反应,静置片刻后,
15、如图所示,向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,直至恰好完全反应,静置片刻后,
![]()
![]() 塑料小方块 塑料小方块处于稳定状态(塑料小方块不与溶液反应),
则与滴加Ba(OH)2溶液之前相比,塑料小方块浸入液
塑料小方块 塑料小方块处于稳定状态(塑料小方块不与溶液反应),
则与滴加Ba(OH)2溶液之前相比,塑料小方块浸入液
稀H2SO4 体中的体积-------------------------------------------------( )
![]() A 变大
B变小
C不变
D 无法确定
A 变大
B变小
C不变
D 无法确定
二、填空题:(共 9小题,共34分)
16、澄清的石灰水中溶质的化学式为 。盐酸中溶质的化学式为 。
17、请完成下列化学方程式,并指出基本反应类型。
(1)氧化钙溶于水 属于 反应
(2) CuO +( )= CuSO 4 +( )
(3)铝和盐酸反应 属于 反应
(4) HCl +( )= AgCl↓ +( ) 属于 反应
18、钡餐透视检查胃肠疾病时,医生让病人口服硫酸钡,但误服碳酸钡就会中毒,原因是它与体内胃酸反应能生成可溶性的钡盐,则反应的化学方程式为
19、工业用盐酸中常含有H÷、Fe3÷、Cl---而略带黄色,该盐酸中杂质的化学式是 ,
若此盐酸中H+ 和Cl--- 的个数比为18:21,则Fe3+ 和Cl---- 的个数比为 。
20、下列物质中:A硫酸 B氢氧化钙C氢氧化铁D氢氧化钠E 氧化钙F氧化铜
(1)与粘土和砂子混和可制成三合土的是 。(填编号,下同)
(2)极易溶解于水、在空气中易潮解的碱是 。
(3)能与氯化钡溶液反应生成不溶于硝酸的白色沉淀的是 。
(4)在工业上用煅烧石灰石来制取的是 。
21、用化学方程式解释下列现象:盛苛性钠溶液的试剂瓶不应用玻璃塞(玻璃中含有SiO2),其原因为________ ;表面生锈的铁钉放入足量的盐酸中,无色液体逐渐变成黄色;过一段时间又看到铁钉表面冒气泡。其原因为_______________ 、 。
22、既能与稀硫酸反应生成白色沉淀,又能与硝酸银反应生成白色沉淀,且沉淀均不溶于稀硝酸,则此溶液可能是 溶液。
23、氨气溶于水,所得溶液中溶质电离生成NH4++和OH---。试写出氨气和稀硝酸反应的
化学方程式: 。其所得溶液中固体溶质受到猛烈撞击时发生爆炸,生成最常接触的两种气体和一种液体。写出该反应的化学方程式: 。
24、向盛有镁、氧化铜和氢氧化钠固体的混合物的烧杯中加入一定量的稀硫酸,充分反应后过滤,滤液中滴入无色酚酞试液呈红色,则滤纸上的物质是 ,滤液中含的溶质 (2)
是 。(写化学式)
三、实验题:(共4小题,共23分)
25、实验室仅提供下列五种装置,请根据装置图回答:(无水硫酸铜遇水由白变蓝)
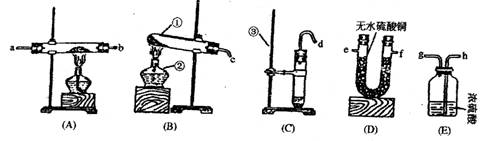
(1)将上图中标有数字的仪器的名称写在横线上。① ② ③
(2)实验室制氢气应该选用装置 ,制氧气应选用装置 ,制二氧化碳应选用装置 。(填编号)
(3)实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为
![]() ;实验室用锌粒与稀硫酸反应制取氢气的化学方程式为
。 (4)实验室用锌跟稀硫酸反应制取氢气,并用生成的氢气还原氧化铜。为了验证氢气还原氧化铜有水生成,在全部的实验过程中需要用到的装置有
(填编号),导气管接口从左到右的连接顺序依次为
(填字母)。
;实验室用锌粒与稀硫酸反应制取氢气的化学方程式为
。 (4)实验室用锌跟稀硫酸反应制取氢气,并用生成的氢气还原氧化铜。为了验证氢气还原氧化铜有水生成,在全部的实验过程中需要用到的装置有
(填编号),导气管接口从左到右的连接顺序依次为
(填字母)。
26、填写实验报告:
![]()
![]()
![]()
![]()
![]() 实验步骤
实验现象
化学方程式
实验步骤
实验现象
化学方程式
![]() 向蓝色溶液中滴加 产生 色沉淀
向蓝色溶液中滴加 产生 色沉淀
氢氧化钠溶液
![]() 熟石灰与纯碱(Na2CO3)产生 色的沉淀
熟石灰与纯碱(Na2CO3)产生 色的沉淀
溶液反应可制得烧碱
![]()
27、家庭小实验:张小明在家里找到了一些导线、干电池、一只小灯泡、一个小开关和两根碳棒,他用两根碳棒做电极,将这些连成一个串联电路,然后,用四个小瓶分别取家里的A:食盐晶体、B:食盐溶液、C:白酒、D:蔗糖,将两根碳棒分别插入小瓶中,发现能使小灯泡发光的是 。不能发光的是 。
28、推断题:有一包白色粉末,可能由氯化银、碳酸 钠、氢氧化镁、氯化钡、硫酸 钠和硝 酸钾中的某几种组成。为了鉴定其成分,实验如下:(1)将少量粉末放入足量水中,搅拌、静置、过滤、得白色沉淀和无色滤液。(2)向所得沉淀中加入足量稀 硝 酸,沉淀全部溶解,但无气体产生。(3)向滤液中滴加硝酸银 (3)
溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解。试根据以上现象推断该白色粉末中一定含有 ;一定没有 ;可能含有 。
四、计算题:(共 2小题,共13 分)
29.向100克稀硫酸中滴加10%的氯化钡溶液,至不再产生沉淀时用去氯化钡溶液208克。回答下列问题:
(1)此题中涉及的化学方程式为 ;
(2)列出求生成白色沉淀BaSO4(X)的比例式: ;
(3)生成白色沉淀BaSO4的质量为 克;
(4)则这种稀硫酸中溶质的质量分数为 。
30、有一瓶敞口放置过的氢氧化钠固体。取出60克该固体,烘干后质量为50.6克,再与足量稀盐酸反应,生成气体4.4克,试回答:
(1)写出该反应中涉及到的化学方程式 、
。
(2)求出固体中氢氧化钠的质量是 ;
(3)反应后的溶液中含有氯化钠的质量为 。
答案
一、 选择题:(共15小题,共30分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| C | D | A | C | D | C | D | C |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
| B | D | D | B | B | A | B |
二、填空题:(共 9小题,共34分)
16. Ca(OH)2 HCl
17. (1). CaO + H2O == Ca(OH)2 化合反应
(2)..CuO + H2SO4 == CuSO4 + H2O
(3) 2Al + 6HCl === 2AlCl3 + 3H2↑ (置换反应)
(4) HCl + AgNO3 === AgCl↓ + HNO3 (复分解反应)
18:2HCl+ BaCO3==== BaSO4 ↓+ H2O + CO2↑
19:FeCl3
20:(1):B (2):D (3) A (4) E
21:2NaOH + SiO2 == Na2SiO3 + H2O
Fe2O3 + 6HCl === 2FeCl3 + 3H2O Fe + 2HCl === FeCl2 + H2↑
22:BaCl2
23:NH3 + HNO3 == NH4NO3 NH4NO3 + O2 == NO2 +NO+2H2O
24:Mg(OH)2 、Cu(OH)2 、 NaOH
三、实验题:
25:(1)将上图中标有数字的仪器的名称写在横线上。① 试管 ② 酒精灯 ③ 铁架台
(2)实验室制氢气应该选用装置 C ,制氧气应选用装置 B ,制二氧化碳应选用装置 C 。(填编号)
(3实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为CaCO3 +2HCl =CaCl2+ H2O + CO2↑
实验室用锌粒与稀硫酸反应制取氢气的化学方程式为Zn + H2SO4 === ZnSO4 + H2↑
(4)实验室用锌跟稀硫酸反应制取氢气,并用生成的氢气还原氧化铜。为了验证氢气还原氧化铜有水生成,在全部的实验过程中需要用到的装置有 C、 A、D (填编号),导气管接口从左到右的连接顺序依次为 c、h、g、a、b、e (填字母)。
![]() 26、填写实验报告:
26、填写实验报告:
![]()
![]()
![]()
![]() 实验步骤 实验现象
化学方程式
实验步骤 实验现象
化学方程式
![]() 向蓝色溶液中滴加 产生蓝 色沉淀 CuSO4+2NaOH==Cu(OH)2↓ + Na2SO4
向蓝色溶液中滴加 产生蓝 色沉淀 CuSO4+2NaOH==Cu(OH)2↓ + Na2SO4
氢氧化钠溶液
![]() 熟石灰与纯碱(Na2CO3)产生 白 色的沉淀 Ca(OH)2 + Na2CO3
=== CaCO3↓+ 2NaOH
熟石灰与纯碱(Na2CO3)产生 白 色的沉淀 Ca(OH)2 + Na2CO3
=== CaCO3↓+ 2NaOH
溶液反应可制得烧碱
![]()
27:发现能使小灯泡发光的是 B 。不能发光的是 A、C、D。
28:一定含有 BaCl2、 Na2CO3 ;一定没有 AgCl、Na2SO4 ;可能含有 Mg(OH)2、、KNO3 。
四、计算题:(共 2小题,共13 分)
29:(1):H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl
(2):208:233==208g×10% :x
(3):20・8g (4):9、8%
30:(1) Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
HCl + NaOH ==== NaCl +H2O (2):50・6g-10・6g == 40g
(3):11・2g + 58・5g == 69・7g