初三化学第八章综合练习
相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39 Ca-40 Fe-56 Cu-64 Ag-108
一、选择题:
1、下列物质或溶液中存在自由移动的氯离子的是…………[ ]
A、氯酸钾溶液 B、氢氯酸 C、氯气 D、氯化钠晶体
2、下列各组离子,属于酸电离产物的是…………[ ]
A、K+、CO32- B、K+、H+、SO42- C、H+、MnO42- D、NH4+、NO3-
3、下列物质中既可以用于制造漂白粉,又可用于配制波尔多液的是…………[ ]
A、苛性钠 B、胆矾 C、浓硫酸 D、熟石灰
4、下列说法正确的是…………[ ]
A、紫色石蕊试液能使稀硫酸变红 B、氢氧化铁能使无色酚酞试液变红色
C、碳酸钠溶液能使无色酚酞试液变红色 D、浓硫酸沾在皮肤上应先用水冲洗
5、在稀硫酸中加过量的下列固体,不能使溶液PH升高到大于7的是…………[ ]
A、CaO B、NaOH C、Ca(OH)2 D、BaCl2
6、如果某溶液中的溶质发生化学反应,生成的几种物质都是沉淀或气体或水时,该溶液的导电性就会迅速降低,现要使CuSO4溶液的导电性迅速降低,可加入适量的下列试剂是………[ ]
A、烧碱溶液 B、氢氧化钡溶液 C、铁 D、过量的锌
7、下列说法正确的是…………[ ]
A、金属氧化物都是碱性氧化物 B、正盐中不可能含氢元素
C、碱中一定有金属元素 D、酸、碱、盐中都肯定有非金属元素
8、下列物质中肯定属于纯净物的是…………[ ]
A、盐酸 B、澄清的石灰水 C、蓝矾 D、排水法收集的氢气
9、除去食盐水中混有的烧碱和纯碱杂质最好应加入适量的…………[ ]
A、盐酸 B、稀硫酸
C、氢氧化钙溶液和盐酸 D、氯化钙溶液和盐酸
10、下列各酸中与NaOH反应只生成正盐的是…………[ ]
A、亚硫酸 B、硝酸 C、磷酸 D、氢硫酸
11、下列反应符合事实且配平也正确的是…………[ ]
A、Fe+H2CO3=FeCO3+H2↑ B、CO+CuO=Cu+CO2
C、Cu+2AgCl=CuCl2+2Ag D、Ag2CO3+2HNO3=2AgNO3+H2O+CO2↑
12、只用一种试剂一次性鉴别AgNO3、BaCl2、Na2CO3三种无色溶液可选用…………[ ]
A、CaCl2溶液 B、盐酸 C、稀HNO3 D、K2CO3溶液
13、下列物质中既能跟稀硫酸反应,又能跟硝酸银溶液反应的是…………[ ]
A、氧化铜 B、氯化钠溶液 C、盐酸 D、氯化钡溶液
14、几种物质溶于水,能电离出K+、Zn2+、SO42-、Cl-四种离子,已知其中三种离子个数比为K+:Zn2+:SO42-=2:3:2,则SO42-与Cl-的离子个数比为…………[ ]
A、1:1 B、1:2 C、2:3 D、3:2
15、验证Fe、Cu、Ag三种金属的活动性顺序,分别选用下列各组试剂,其中肯定不能达到目的的是…………[ ]
A、Fe、Cu、AgNO3溶液 B、Fe、CuSO4溶液、Ag
C、FeSO4溶液、Cu、Ag D、FeSO4溶液、Cu、AgNO3溶液
二、选择题:
16、有一无色溶液中滴入BaCl2溶液产生白色沉淀且不溶于稀HNO3,则此白色沉淀是……[ ]
A、AgCl B、BaSO4
C、BaCO3 D、可能是AgCl,也可能是BaSO4,不可能是BaCO3
17、由Na、S、O、H中的二种或三种元素组成四种化合物。甲能与BaCl2 反应生成盐和酸;乙能与NaOH反应生成盐和水;丙能与HCl反应生成盐和水;丁呈中性,与CaO或CO2都可化合,则下列推断错误的是…………[ ]
A、甲不一定是H2SO4 B、乙不一定为SO2 C、丙不一定为NaOH D、丁一定为H2O
18、NaNO3溶液中混有AgNO3、Ba(NO3)2、Cu(NO3)2,现要依次使Ag+、Ba2-、Cu2+逐一转化为沉淀并分离出来,可使用的试剂有Na2SO4、NaOH、NaCl溶液,试剂加入的顺序为…………[ ]
A、NaCl、NaOH、Na2SO4 B、NaOH、Na2SO4、NaCl
C、Na2SO4、NaCl、NaOH D、NaCl、Na2SO4、NaOH
19、下列变化中不属于化学变化的是…………[ ]
A、硫酸铜吸水后变蓝 B、生石灰吸水后变成粉末
C、晶碱风化 D、烧碱潮解成溶液
20、下列各组离子在同一强酸性溶液中可大量共存的是…………[ ]
A、Ag+、NO3-、Na+、Cl- B、Cl-、Mg2+、Ca2+、NH4+
C、NO3-、Cu2+、SO42-、OH- D、NH4+、SO42-、CO32-、K+
21、将100克稀硫酸分成四等份,分别与足量的下列物质充分反应,所得溶液中溶质质量分数最大的是…………[ ]
A、Fe B、FeO C、Fe(OH)2 D、FeCO3
22、下列实验设计可行的是…………[ ]
A、用稀硫酸可洗去石灰水瓶内壁的白色固体
B、用铁和硫酸铜溶液验证铁和铜的活动性强弱
C、向自来水中加硝酸银溶液有白色沉淀即可证明自来水中有Cl-
D、检验生石灰中有无未分解完的石灰石,可将生石灰溶于水,观察有无不溶物存在
23、可溶性钡盐有毒,误服BaCl2引起中毒,解毒时可服用的试剂是…………[ ]
A、Na2CO3溶液 B、CuSO4溶液 C、MgSO4溶液 D、NaOH溶液
24、人的胃液中胃酸过多时,可服用适量的某些物质与胃酸反应,但不可服用…………[ ]
A、含Al(OH)3的药物 B、少量NaHCO3溶液 C、含CaCO3咀嚼片 D、CaO固体
25、下列盐可由金属与酸发生置换反应生成的是…………[ ]
A、HgCl2 B、FeCl3 C、Fe(NO3)2 D、AlCl3
26、能与氢氧化钡溶液反应,但不加酚酞试液就看不出明显反应现象的是…………[ ]
A、稀硫酸 B、稀盐酸 C、碳酸钠溶液 D、二氧化碳气体
27、将SO3、CaO、NaCl、Na2CO3・10H2O、MgCO3各1克,分别放入99克水中充分搅拌,形成的溶液质量恰好为100克的有几种…………[ ]
A、2种 B、3种 C、4种 D、5种
28、下列反应中最能说明CO2是酸性氧化物的是…………[ ]
|
|
C、H2CO3==H2O+CO2↑ D、CaCO3 === CaO+CO2↑
29、用Mg、MgO、Mg(OH)2、MgSO4、HCl和CuCl2溶液制取MgCl2的方法有…………[ ]
A、三种 B、四种 C、五种 D、六种
30、10克不纯的CaCO3样品跟足量盐酸反应后,共收集到4.44克CO2,且溶液下方留有不溶物。据此,试分析在CaCO3的样品中,关于:(1)MgCO3;(2)K2CO3;(3)AgCl等杂质的含有情况,结论正确的是…………[ ]
A、肯定含有(1)和(3),肯定不含(2) B、肯定含有(1)和(3),可能含(2)
C、肯定含(2)和(3),肯定不含(1) D、肯定含(2)和(3),可能含(1)
三、填空题
+2 +4 -2 +1 +1 -2
31、现有 Cu、 C、 O、 H、 Na、 S,按规定的化合价,组成有关物质:(各写化学式一个)
①可溶性碱性氧化物 ;②酸性氧化物 ;③无机含氧酸 ;
④无氧酸 ;⑤可溶性碱 ;⑥无氧酸钠盐、正盐 ;
⑦碱式盐 ;⑧一种结晶水合物 。
写出符合下列要求的化学方程式:
①与水反应生成一种酸 ②与水反应生成一种碱
③分解反应生成三种氧化物
④分解反应有水和盐生成
⑤中和反应生成无氧酸钠盐
⑥可溶性碱在空气中变质
32、分别经过两步反应制备有关物质,写化学方程式,其它原料任选:
(1)石灰石制消石灰 , ;
(2)由镁制氢氧化镁 , ;
(3)由氯化钙制硝酸钙 , ;
(4)由铜制硫酸铜 , 。
33、描述反应现象时可从状态改变、颜色变化、有无沉淀物产生等方面描述,但不能直接说生成某某物质,请完成下表空格:
| 序号 | 实验内容 | 现象 | 化学方程式 |
| (1) | 在盐酸中滴加硝酸银溶液 | ||
| (2) | 在硫酸铜溶液中滴加烧碱溶液 | ||
| (3) | 在氯化铁溶液中滴加氢氧化钾溶液 | ||
| (4) | 在硝酸汞溶液中插入一根铜丝 | ||
| (5) | 滴有酚酞的石灰水中加足量硝酸 |
34、用一种试剂鉴别组内几种不同物质,不用组内物质间反应,写所用试剂的化学式:
(1)硫酸铜、硫酸钡、苛性钠、氯化钠四种白色固体
(2)石灰水、氢氧化钠溶液、稀硫酸
35、用不同的试剂鉴别NaOH溶液和稀盐酸,供选用的试剂有:(1)紫色石蕊试液;(2)洁净的铜丝;(3)氧化铜;(4)水;(5)硫酸铜溶液;(6)铁片;(7)氢氧化铜;(8)石灰石,哪两种试剂不可选用?写序号 和 。
36、(1)Zn、Fe、Cu三种金属与AgCl、CuCl2、AgNO3、CuCO3、H2CO3在水中两两混合,共能进行 个置换反应。
 (2)NaOH、Cu(OH)2、HCl、Na2SO4、BaCl2、FeCl3六种物质在水中两两混合,共能进行 个复分解反应。
(2)NaOH、Cu(OH)2、HCl、Na2SO4、BaCl2、FeCl3六种物质在水中两两混合,共能进行 个复分解反应。
四、推断及实验综合题
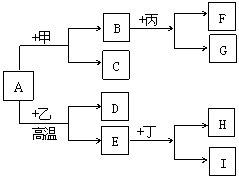
37、以下是有关物质相互转化的关系图,
其中A是一种金属氧化物,C为水,
G是红褐色沉淀,I的溶液呈浅绿色。
根据上述关系图和有关叙述回答下列问题:
(1)若F是由Na+和Cl-形成的溶液,则
甲物质是 ,丙物质是 。
(2)若D是能使石灰水变浑浊的气体,则乙物质可能是 。
(3)丁物质可能是属于氧化物、酸、盐中的 。
38、从下列试剂(都为溶液):①BaCl2 ;②KOH; ③Ba(OH)2; ④AgNO3; ⑤NaOH; ⑥盐酸 ⑦K2CO3中,选择试剂分别除去KCl中含有的MgCl2和K2SO4杂质,写所用试剂中溶质的化学式。
(1)加蒸馏水充分溶解固体混合物。
(2)先向含有杂质的溶液中加入过量的 溶液,产生两种沉淀。
(3)经过滤,滤液中加入稍过量的 溶液,过滤后,再向滤液中加入过量的
溶液至不产生气泡为止,再进行蒸发结晶,即可得纯KCl。
五、计算题:
39、根据硫酸铜晶体的化学式CuSO4・5H2O计算:
(1)CuSO4・5H2O的式量为 ;
(2)CuSO4・5H2O中结晶水的质量分数为 ;
(3)25克CuSO4・5H2O完全溶解于175克水中所得溶液中溶质的质量分数为 。
40、100克溶质的质量分数为20%的苛性钠溶液与一定量19.6%的稀硫酸恰好完全反应。求:
(1)有多少硫酸钠生成?(2)所得到溶液的溶质质量分数是多少?
参考答案
一、选择题:
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 答 案 | B | C | C | B | C | D | D | C | D | D | B |
| 题 号 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| 答 案 | A | A | D | D | C | B | D | AC | CD | B | B |
三、填空题:
23、CH4,尿素,熟石灰,食盐,石墨,不锈钢 24、黑,碳化,强烈的腐蚀性
25、NaNO3
(1)Na2SO4+Ba(NO3)2===BaSO4↓+ NaNO3 (2) Na2CO3 +2HNO3===2NaNO3+CO2↑+H2O
(3) NaCl+ AgNO3===AgCl↓+ NaNO3 (4) NaOH +HNO3===NaNO3+H2O 26、
| 名称 | 纯碱 | 氢氧化铜 | 熟石灰 | 硫化钠 |
| 化学式 | Na2CO3 | Cu(OH)2 | Ca(OH)2 | Na2S |
| 类别 | 盐 | 碱 | 碱 | 盐 |
27、CuCl2 ;Ba(OH)2;Na2SO4
28、A:AgNO3 B:K2CO3 C:Ca(NO3)2 D:KNO3 E:HCl
AgNO3+HCl== AgCl↓+HNO3,Na2CO3 +2HCl===2NaCl+CO2↑+H2O 。
29、(1) KOH、MgCl2,CuSO4 (2)BaCl2 (3)KNO3,K2CO3;Na2CO3。
四、实验题:
30、甲乙丙,铁,因为Fe排在Zn和H之间。
31、(1) CaO+H2O==Ca(OH)2、Ca(OH)2+Na2CO3==CaCO3↓+2NaOH (2) NaOH、NaCl
(3)稀盐酸,若出现气泡,若无气泡出现
32、(1)c→d→b(2)B瓶中品红褪色(3)D,澄清石灰水变浑(4)不能,气体经过前面溶液时会带出水蒸气。
五、计算题:
33、19.6%,28.6%,4g