初中毕业生学业暨高中招生考试化学试卷
(全卷共四个大题,满分70分,与物理共用120分钟)
| 题号 | 一 | 二 | 三 | 四 | 总分 | 总分人 |
| 得分 |
注意:凡同一题号下注有“课改实验区考生做”的题目供课改实验区考生做,注有“非课改实验区考生做”的题目供非课改实验区考生做,没有注明的题目供所有 考生做。
可能用到的相对原子质量:H 1 O 16 Na 23
一、选择题(本大题包括15个小题,每小题2分,共30分)每小题只有一个选项符合题意,将正确选项的序号填人括号内。
l.下列工艺制作过程中包含了化学变化的是………………………………………( )
A.红纸剪成窗花 B.泥土烧成瓷器
C.冰块制成冰雕 D.木板制成模型飞机
2.薯片等易碎食品宜采用充气袋包装,下列气体中最不适宜充入的是……………( )
A.O2 B.N2 C.C02 D.空气
3.给农作物施用下列一种化肥就能增加两种营养元素,这种化肥是………………( )
A.NH4HC03 B.K2S04 C.Ca3(P04)2 D.KNO3
4.下列物质中属于纯净物的是…………………………………………………………( )
A.天然气 B.乙醇汽油 C.纯碱 D.加铁酱油
5.“蓝天行动”被评为重庆直辖十年十大环保事件的候选事件,下列措施不利于‘‘蓝天行
动”。实旋的是…………………………………………………………………………( )
A.退耕还林,增大森林覆盖面积
B.密闭运输砂土,减少扬尘
C.大力发展火力发电
D.用天然气代替汽油作汽车燃料
6.下列叙述错误的是…………………………………………………………………( )
A.原子由原子核和电子构成 B.分子总是在不断运动
C.干冰中的分子间有间隔 D.原子失去电子后变成阴离子
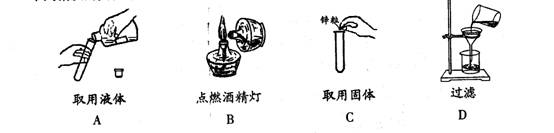
7.下列错误的实验操作中,可能引起安全事故的是……………………………( )
8.人体吸人的O2有2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用Na2SeO3清除人体内的活性氧,Na2Se03扣Se(硒)元素的化合价是…………( )
A.+2 B.+4 C. +6 D.-2
9.下列说法错误的是……………………………………………………………………( )
A.化学反应是人类获取能量的重要方式B.过滤是一种净水的方法
C.催化剂在化学反应前后质量不发生改变
D.铁在干燥的空气中容易生锈
10.(课改实验区考生做)下列叙述正确的是…………………………………………( )
A.青少年的生长过程需要大量蛋白质,所以要多吃水果
B.油脂和糖类物质都能够为人体提供热量
c.合成纤维、合金、合成橡胶都是合成材料
D.焚烧塑料是解决“白色污染”的好办法
![]()
(非课改实验区考生做)某原子结构示意图为 有关它的说法错误的是・・’( )
A.它的核内有12个质子 B.它属于非金属元素
C.它有3个电子层 D.它的最外层有2个电子
11.香烟烟雾中含有CO、CO2、SO2等气体,这3种气体的共同点是………………( )
A.都是氧化物 B.都含有氧分子 C.都能燃烧 D.都有毒
12.水是生命之源,既普通又宝贵。下列对水的“多”与“少”的描述错误的是……( )
A.地球上水的总量多,淡水少
B.我国水资源总量多,人均水量少
C.“南水北调”工程说明南方水的储量多,北方水的储量少
D.生活中接触的纯净水多,水溶液少
13.下列物质中既存在离子又存在分子的是……………………………………………( )
A.氯化钠晶体 B.金刚石
C.氯化钠溶液 D.液氧
14.森林初发火灾时,可以使用爆炸灭火的方法,将灭火弹抛到火场爆炸将火扑灭。关于爆
炸灭火原因的分析不合理的是………………………………………………………( )
A.爆炸使燃烧处暂时缺氧 B.爆炸气浪降低了可燃物的温度
C.爆炸气浪降低了可燃物的着火点 D.炸起的沙土覆盖可燃物,隔绝空气
15.下列化学方程式的书写正确的是…………………………一………………………。( )
A. 3CO+Fe2O3 ![]() 2Fe+3CO2 B. Cu+AgNO3==Cu(NO3)2+Ag
2Fe+3CO2 B. Cu+AgNO3==Cu(NO3)2+Ag
C. Cu+H2SO4===CuSO4+H2 ↑ D. CuCl2+K2SO4==CuSO4+2KCl
二、填空题(本大题包括6个小题,共22分)
16.(3分)用化学符号表示:
2个氢原子 ;2个氯离子 ;含有钠元素的碱 。
17.(2分)右边是雪碧汽水标签中的部分内容。
 (1)小虎同学取适量雪碧汽水于试管中,稍稍加热后产生大量气泡,发生反应的化学方程式为:
(1)小虎同学取适量雪碧汽水于试管中,稍稍加热后产生大量气泡,发生反应的化学方程式为:
(2)将雪碧汽水充分煮沸后滴人石蕊试液,溶液呈红色,使石
蕊变红的物质是
18.(4分)高纯度的单质硅是信息产业的核心材料,没有硅就没有你喜欢的计算机。请用你学过的知识回答下列问题:
(1)地壳中含有大量的硅元素,它的含量仅次于 元素。
(2)SiO2是沙的主要成分,工业上制取粗硅的化学方程式为:SiO2+2C
![]() Si+2R,R
Si+2R,R
的化学式为 ;该化学反应的基本类型是下列中的 。
①化合反应 ②分解反应 ③置换反应 ④复分解反应
(3)硅能在O2中燃烧生成SiO2,并放出大量的热,有科学家正研究将硅作为新能源。与化石能源相比较,硅燃烧没有CO2排放,因而有助于解决的环境问题是 。
19.(5分)每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
(1)取小袋内物质,加入稀盐酸中,发生反应的化学方程式为:
(2)将袋内物质放在足量O2中燃烧,写出反应的化学方程式:
①
②
(3)将袋内物质加入一定量的CuSO4溶液中,充分反应后过滤,滤液中的溶质一定
有 (填写化学式)。
20.(4分)食盐是人们生活中不可缺少的调味剂,随着人们健康意识的提高,市场上出现
了“加碘盐”、“叶绿素锌钠盐”、“低钠盐”等。某种低钠盐由NaCl、KCl、MgSO4三
种物质组成,用它进行以下实验(假设每步均恰好完全反应)。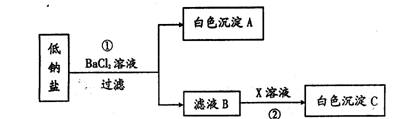
(1)写出步骤①的化学方程式:
(2)当x是AgNO3时,白色沉淀C是 ,当x是NaOH时,白色沉淀C是
21.(4分)学习了溶液的概念后,老师的提问及同学的回答如下图所示:

(1)以上三位同学中能够正确描述溶液特征的是 同学。
老师接着问:“你们还想知道什么?”
王华回答:“不溶于水的物质能溶于其它溶剂吗?”
李佳回答:“影响物质在水中溶解能力的因素有哪些?”
(2)如果用实验回答王华的问题,则应该选择的溶质和溶剂分别是:
、 。
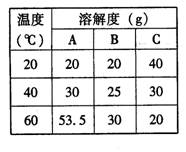
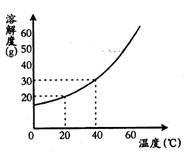
(3)针对李佳的问题,老师引导同学们进行了一系列探究,包括绘制A、B、C三种固体物质的溶解度曲线,下表列出了从探究实验中获取的部分数据,李佳根据下表中的数据绘制了一条溶解度曲线,它是 物质的溶解度曲线。
三、实验题(本大题包括2个小题,共12分)
22、今天是实验室的开放日,某小组的同学来到实验桌前,桌上摆放有下列仪器:
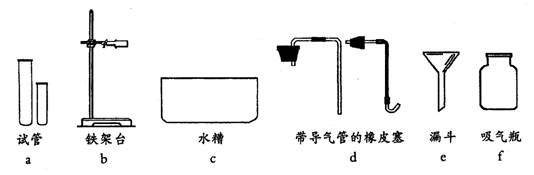
 (1)组长让大家完成的第一个任务是写出仪器的名称,同学们完成任务的情况如上图所示,其中名称有错误的是
(填序号)。
(1)组长让大家完成的第一个任务是写出仪器的名称,同学们完成任务的情况如上图所示,其中名称有错误的是
(填序号)。
(2)用高锰酸钾制取氧气还需要补充的玻璃仪器是 。
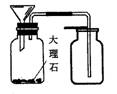
(3)某同学想用右图装置制取CO2,组长指出,这需要太多的稀盐酸
才能淹没漏斗的下管口,起到液封的作用。张兵同学选用了上面
的一种仪器,加在右图装置上,既解决了液封的问题,又可以减
少酸的用量.请把该仪器画在图中应该放置的位置。
23.(7分)刘丽同学在某食品包装袋内取出一小袋干燥剂,上面写着“干燥剂,主要成分为生石灰”。她将这袋干燥剂全部倒人一定量水中,充分搅拌后过滤,得到白色沉淀和滤液。
(1)刘丽同学测定了滤液的酸碱度,你认为结果可能是 。
(2)刘丽同学又对白色沉淀的组成提出了以下假设:
假设l 是CaO和CaCO3的混合物
假设2 是Ca(OH)2和CaCO3的混合物
假设3 只有CaCO3
假设4 只有Ca(OH)2
其中假设 不合理。
(3)为了判断其他几种假设的合理性,刘丽同学继续进行实验:
①取少量沉淀放在试管中,加人稀盐酸,出现气泡,该反应的化学方程式为:
由此可否定假设 。
②为了得到最后结论,她再取少量沉淀放在另一支试管中,加少量水振荡、静置后,滴入
酚酞试液,显红色,说明只有假设 合理。
四、计算题(本大题包括1个小题,共6分)
24.(6分)电解水时,常常要加入少量氢氧化钠使反应容易进行。现将加有氢氧化钠的水
通电一段时间后,产生lg氢气,其中氢氧化钠的质量分数也由4.8%变为5%。计算:
(1)生成氧气的质量。 (2)电解后剩余水的质量。