2006年下期化学第三次月考试卷
可能用到的相对原子质量: H:1 O:16 C:12 Ca:40 Mg:24 Al:27 Ba:137
一.选择题:(每题2分,共28分)
1.下列现象中一定发生化学变化的是
A.食物腐烂 B.湿衣服晾干 C.矿石粉碎 D.海水晒盐
2.由一种元素组成的不同单质互称为同素异形体.则下列互为同素异形体的是
A.CO和CO2 B.金刚石和石墨 C.氧气和液氧 D.水和冰
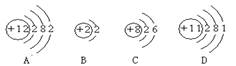
3.某化合物的化学式为AB2,则B的原子结构示意图最有可能是
4.现代医学证明,人类牙齿由一层称为碱式磷酸钙的坚硬物质保护着。碱式磷酸钙的化学式中除钙离子外,还含有一个氢氧根离子和三个磷酸根离子,则其化学式正确的是
A.Ca2(PO4)3(OH) B.Ca3(PO4)3(OH) C.Ca4(PO4)3(OH) D.Ca5(PO4)3(OH)
5.“2005年中国十大科技进展新闻”之一:我国科学家成功实现首次单分子自旋态控制。是世界上首次实现单个分子内部的化学反应。单个分子内部的化学反应中发生变化的是
A.原子种类 B.分子种类 C.元素种类 D.原子个数
6.由碳、氧两种元素组成的气体中,碳与氧的质量之比为3:5,则该气体可能是:
A.由CO或CO2单独组成的纯净物 B.由CO和CO2共同组成的混合物
C.由CO2和O2共同组成的混合物 D.无法确定
7.为及时发现煤气(主要成分是CO)泄漏,常加入少量有特殊气味的乙硫醇(化学式为C2H5SH)。乙硫醇完全燃烧的化学方程式为2C2H5SH
+ 9O2![]() 4CO2 + 6H2O + 2X 。下列说法中正确的是
4CO2 + 6H2O + 2X 。下列说法中正确的是
A.CO是一种有刺激性气味的气体 B.X的化学式是SO2
C.CO、CO2都是污染空气的有毒气体 D.乙硫醇是由四种元素组成
8.空气质量日报是环境监测部门对一个地区空气质量情况所做的监测报告。目前计入空气主要污染物的是可吸入颗粒物、一氧化碳、二氧化碳、二氧化硫、氮的氧化物。下列情况能直接造成空气污染的是
A、把煤作为主要燃料 B、随意丢弃塑料垃圾
C、随意丢弃废电池 D、利用太阳能、风能、等清洁能源
9.“绿色奥运”是2008年北京奥运会的主题之一,为了减轻大气污染,在汽车尾气排放加装“催化净化器”,可将尾气中的NO、CO转化为参与大气循环的无毒的混合气体,该混合气体是
A、CO2、NH3 B、O2、CO2 C、N2、CO2 D、NO2、CO2
10.“达菲”是治疗人类感染禽流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H1005)存在于我国盛产的八角茴香中。下列说法正确的是( )
A.莽草酸中碳、氢、氧三种元素的质量比为42:5:40
B.莽草酸的相对分子质量为87 C.每个莽草酸分子中含有21个原子
D.莽草酸中碳元素的质量分数约为2l%
11.供家用煤炉燃烧的煤制成的蜂窝状,这是为了
A.增加空气中氧气的体积分数 B.使煤燃烧产生的热量不易散失
C.增加煤与氧气的接触面积 D.延缓煤的燃烧时间,节约能源
12.下列五种物质中含有碘元素,它们按下列顺序排列:①NaI ②I2 ③HIO ④X
⑤KIO4根据这种排列规律,X不可能是
A.I(IO3)3 B.AgI C.I2O4 D.I2O5
13.A、B、C三种物质各15g,当它们相互反应完成时,生成30g新物质D。若再增加10gC,它们又继续反应到完成时,A与C恰好消耗完毕。则参加反应的A与B的质量比是
A.2∶3 B.2∶1 C.1∶1 D.3∶2
14.把盛有等质量盐酸的烧杯,分别放在天平托盘上,天平平衡后,将铝粉放入左杯,镁粉放入右杯,充分反应后酸仍足量,如果使天平仍保持平衡,则加入铝镁两种金属的质量比是
A.24∶27 B.27∶24 C.33∶32 D.35∶36
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
二.填空题(每空1分,共15分)
15.用化学用语表示: ① 3个亚铁离子______ ② +2价的镁元素_____
16.物质的结构决定物质的性质。已知氢元素原子的核电荷数为1。试分析:
①H+是结构最简单的一种阳离子,H+中含有的质子数为 ,电子数为 。
②NaH是一种离子化合物,其中Na元素的化合价为+1,则该化合物中氢元素的化合价为 。已知反应物中具有还原性的物质,发生氧化反应后,有元素化合价升高。请判断NaH+H2O=NaOH+H2↑反应中,反应物 (填化学式)具有还原性。
17.航天技术的发展为科学研究开辟了新的领域。“神舟六号”飞船的航天员费俊龙和聂海胜在太空中每人每天大约需要0.9Kg氧气、2.5L水、0.6Kg食物,排出1.0Kg二氧化碳、1.8Kg水蒸气等。上述有着重号的物质中,属于单质的是 ,属于氧化物的是 ,属于混合物的是 。
18.甲、乙是两个实验示意图,根据右图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
⑴所发生的二个反应有共同点:集气瓶底部预先均装有少量水。它们的作用分别是:
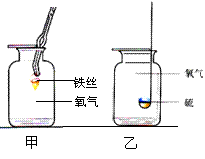 甲中
,
甲中
,
乙中 。
⑵通过比较,发现它们还有许多相似之处,请你写出其中两点:
① ,
② 。
⑶任选上述二个实验中的一个,写出反应的化学方程式:
。
19.取一定质量的CO和CO2的混合气体通入到足量的Ba(OH)2溶液中,充分反应后过滤,发现生成的沉淀和所取的混合气体质量相等,求混合气体中碳原子与氧原子的个数比____________.
 三.实验题:(每空1分共11分)
三.实验题:(每空1分共11分)
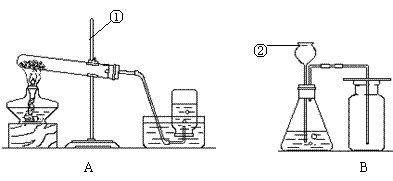
20.根据下装置图回答问题。
(1)写出图中仪器①、②的名称① ,② ;
(2)实验室用常用氯酸钾与二氧化锰混合制取氧气,选用的装置为 ____(填写装置代号,下同),反应的化学方程式为 ;
(3)B装置用来制取CO2,你认为是否合理 (填“是”或“否”),改正的方法是 。(若前空填“是”,改空填“无需改正”)
 21.用来测定空气成分的方法很多, 某校化学兴趣小组设计了如图1所示的装置。
21.用来测定空气成分的方法很多, 某校化学兴趣小组设计了如图1所示的装置。
|
A.蜡烛 B.红磷 C.硫粉 D.铁丝
(2)为了确保实验的成功,在装药品之前应 ,同时药品的用量应保证足量。
(3)小组的同学对实验进行反思后,提出了改进方法(如图2 所示 ),你认为改进后的优点是: 。
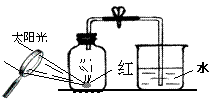 (4)在充分讨论后,他们进行了实验。实验结束后,
(4)在充分讨论后,他们进行了实验。实验结束后,
大家整理的数据如下:(注:集气瓶容积为100mL)
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 集气瓶中进入水的体积(mL) | 20 | 19 | 20 | 20 | 22 | 20 |
|
|
通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。通过实验还可以推断集气瓶中剩余气体的性质(任答一点) 。
四.计算题(6分)
22.石灰石是我国主要矿产之一。学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成的CO2质量/g | 1.76 | 3.52 | 4.4 | m |
(1)哪几次反应中矿石有剩余?
(2)上表中m的数值是 。
(3)试计算这种石灰石矿石中碳酸钙的质量分数。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| A | B | C | D | B | B | B | A | C | A | C | B | D | C |
15.略
16. 1 0 -1 NaH
17. 氧气 ; 水、二氧化碳 ; 食物
18.
(1)甲:防止生成的红热熔化物溅落,炸裂瓶底 乙:吸收燃烧产物,防止SO2 污染空气。
(2)①都是化合反应;②都与氧气反应;③生成物都是氧化物;④反应都放出大量的热;⑤反应条件都是点燃;⑥都是气体与固体反应等
(3)S+O2![]() SO2 或 3Fe+ 2O2
SO2 或 3Fe+ 2O2 ![]() Fe3O4
Fe3O4
19.181:209
20.(1)①试管 ②酒精灯
(2)A 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
(3)是, 无需改正。
21.(1)B(2)检查气密性(3)装置始终密闭,空气没有逸出,实验结果准确
(4)1/5,不支持燃烧,也不支持燃烧,难溶于水、化学性质不活泼
22.(1)3、4两次 (2)4.4 (3)80%