初三化学第一学期期末考试试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 K-39 Cu-64 Zn-65 P-31
第Ⅰ卷(选择题 共36分)
一、选择题(36分。每题只有一个选项符合题意,请将该选项所对应的字母填入上面的答题栏中。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | |||||||||
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
1.6000多年前,半坡居民所从事的生产生活中,发生了化学变化的是( )
A.建造土房 B.烧制土陶 C.磨制石器 D.用麻织布
2.将白醋、食用油、食盐、酒精分别放入水中,不形成溶液的是( )
A.白醋 B.食用油 C.食盐 D.酒精
3.下列人类做法中,不会加剧酸雨、臭氧层空洞、温室效应等环境问题的是( )
A.使用太阳能淋浴器 B.燃烧原煤 C.超音速飞机尾气排放 D.使用氟利昂作制冷剂
4.下列各组物质中,前者为单质,后者为混合物的是( )
A.银、氯化钾 B.白磷、冰水混合物 C.水银、洁净的空气 D.铁粉、二氧化碳
5.葡萄糖(C6H12O6)是一种人体最易吸收的糖类物质,以下说法正确的是( )
A.它是由碳、氢、氧三种原子构成的 B.葡萄糖分子中含有水分子
C.葡萄糖充分燃烧后的产物只有CO2和H2O D.葡萄糖是一种混合物
6.冬季来临时,人们常在树杆下涂上一层石灰浆,其作用是( )
A.美观 B.标记 C.杀菌 D.以上都不对
7.西汉刘安曾记载“曾青得铁则化为铜”。这里的“铜”是指( )
A.铜元素 B.铜单质 C.氧化铜 D.铜原子
8.“摇摇冰”是一种即用即冷的饮料,吸食时,只要将饮料罐隔离层中的物质与水混合后摇动,即可制冷。该物质可能是( )
A.氯化钠 B.硝酸铵 C.氢氧化钠 D.生石灰
9.下列实验仪器中,不能用作反应容器的是( )
A.试管 B.烧杯 C.集气瓶 D.量筒
10.图书馆中图书档案资料等着火时,可用液态二氧化碳灭火器扑灭,液态二氧化碳灭火中的主要作用是
A.降低燃烧物的着火点 B.防止燃烧产物污染空气 C.降温和隔绝空气 D.分解出能灭火的物质
11.室温下,饱和食盐水露置在空气中一段时间后,有少量的固体析出,这是因为( )
A.氯化钠的溶解度变小 B.溶液质量分数变小 C.溶剂质量减少 D.溶液变为不饱和溶液
12.下列变化中属于分解反应的是( )
A.蒸发液态空气生成氮气和氧气 B.少许二氧化锰投入双氧水中制得氧气
C.酒精完全燃烧生成了水和二氧化碳 D.蔗糖溶于水形成糖水
13.我们的生活和生产离不开铁制品,但铁制品在一定的环境中容易生锈,为了防止铁生锈,在铁制品表面,不宜采用的方法是( )
A.刷一层油漆 B.涂一层油 C.镀一层其它金属 D.随时用水冲洗
14.下列有关实验现象描述正确的是( )
A.铁丝在空气中被点燃,火星四射,生成一种黑色的固体
B.氢氧化钠溶液中滴加硫酸铜溶液,产生白色沉淀
C.把光亮的铜片放入盐酸中,表面出现气泡
D.将生石灰放入水中,发现水沸腾
15.下列化学方程式书写正确的是( )
A.2Fe+6HCl==2FeCl3+3H2↑ B.4Al +3O2==2Al2O3
C.3Fe+2O2==Fe3O4 D.2H2O==2H2↑+O2↑
16.下列叙述正确的是( )
A.不同元素的根本区别是在与其相对原子质量不同 B.一种元素只能组成一种单质
C.某单质与氧气完全反应后得到的产物一定含有氧化物 D.原子一定是由质子和中子构成的
17.人体中化学元素含量的多少,会直接影响到人体的健康。下列元素中,因摄入量不足容易导致人患骨质疏松症的是( )
A.铁 B.碘 C.钙 D.锌
18.在抢救大出血的危症病人时,常需用静脉点滴输入0.9%的氯化钠溶液(俗称“生理盐水”),这是由于人体血液中的“矿化度”(即无机盐的相对含量)为0.9%。另有研究证明,30亿年前地表原始海水的矿化度为0.9%。对此,下列猜测或评论中不足取的是( )
A.人类祖先可能是从原始海洋中逐渐进化到陆地上的
B.人体血液和原始海水的矿化度均为0.9%,纯属巧合
C.人体血液中,仍然带有着原始海水的某些印痕
D.人体血液和原始海水之间存在着某些尚未被认识的关系
第Ⅱ卷(非选择题,共64分)
二、填空题(33分)
19.(4分)(1)“侯氏制碱法”关键一步的反应原理为:NH3+CO2+H2O+NaCl==NaHCO3↓+A,则A为___________(填化学式),A中氮元素的化合价为_________。
(2)请选用C、H、O、Ca四种元素中的一种或者是几种写出符合下列要求的化学式:
①打开汽水瓶盖时,大量逸出的气体__________;②溶于水后会放出大量的热的固体_____________;
③我国建设的“西气东输”工程中,这里的“气”指的是___________;
④在抢救危急病人时,用呼吸机输入的单质气体是___________;
⑤相对分子质量最小的氧化物_______________;
⑥具有可燃性,炼铁过程中产生大量的高炉气中的主要成分_____________。
20.(3分)用数字和化学符号表示。
2个钠离子__________; (2)3个氢氧根离子__________;
(3)保持氧气的化学性质的微粒_________; (4)碳酸钠中碳元素的化合价为+4价___ ___;
![]() (5)n个硅原子_____________ (6)
表示的微粒是__________。
(5)n个硅原子_____________ (6)
表示的微粒是__________。
21.(6分)请用化学方法除去下列各组物质中括号中的物质,写出化学方程式,并标明化学反应类型。
(1)铜粉(铁粉)_______________________________________________( );
(2)生石灰(石灰石)___________________________________________( );
(3)二氧化碳(氧气)_______________________________________( );
(4)氯化钠(碳酸钠)_______________________________________;
(5)一氧化碳(二氧化碳)_______________________________________;
22.(3分)(1)实验室现有质量分数为10%的NaOH溶液100g,由于实验要求,急需一定量的20%的NaOH溶液,我们可以往10%的溶液中加入NaOH固体_________g,或者蒸发水________g均可达到目的。
(2)现有t℃下200g某物质的溶液,若蒸发掉20g水后,析出固体为5g,若蒸发30g水,析出固体为15g,则在t℃下该物质的溶解度为____________g。
23.(2分)金属材料在生活中普遍使用。铁制品表面的锈要及时除去,这是因为铁锈结构___________,会加快铁制品的生锈。铝制品不需要除锈,这是因为铝表面能形成_____________,可以阻止铝进一步氧化。
24.(1分)课本上有“烧不坏的手帕”实验:将2体积95%的酒精和1体积的水混合。把一块棉布手绢浸入配好的混合液中,浸透后取出,轻轻拧干,用坩埚钳夹持,在酒精灯上点燃,并轻轻抖动手绢。火熄灭后,观察到原来浸透酒精的手绢并没有烧毁,其中的原因为________________________________________。
25.(3分)在赤壁之战中,周瑜的军队点燃战船,熊熊燃烧的战船借助东风直冲曹军的大船,使曹军的木船燃起大火,根据我们学过的燃烧条件的填写:曹军的木船是______,木船燃烧的条件是________、_______。
26.(6分)下表是硝酸钾和氯化钠两物质在不同温度下的溶解度
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 硝酸钾(g) | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| 氯化钠(g) | 35.5 | 35.8 | 36 | 36.3 | 36.6 | 36.9 | 37.3 | 37.7 | 38.4 | 39 | 39.9 |
(1)根据以上溶解度数据,在下面坐标纸上完成硝酸钾及其氯化钠的溶解度曲线
(2)由上图可知:两物质的溶解度受温度影响较小的是____________;当温度________℃时,硝酸钾的溶解度大于氯化钠的溶解度。
(3)若硝酸钾中混有少量的氯化钠,可采取__________方法提取KNO3。
(4)在90℃时,若有1000g饱和的硝酸钾溶液,则该饱和溶液中溶质质量分数为_________。
27.(2分)根据下表填空
| 气体 | 二氧化氮 |
|
| 颜色 | 棕色 | 无色 |
| 溶解性 | 易溶于水 | 微溶于水 |
| 反应 | 3NO2+H2O==2HNO3+NO | |
(HNO3,即硝酸,是化学常见的强酸之一,易溶于水)
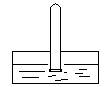
如右图所示,将一支充满二氧化氮的棕色气体的试管倒立在水槽中,试描述试管内可能出现的实验现象。
 ①__________________________________________
①__________________________________________
②__________________________________________。
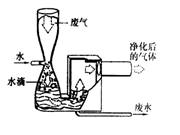
28.(5分)随着工业与交通运输业的迅速发展,有害气体和烟尘的排放
,对空气造成了严重的污染,控制大气污染的主要途径是减少排放
(1)曾经有过一段时间,许多工厂试图通过建造很高的烟囱来解决排放
问题,然而这样做并没有达到目的,原因是_______________________
如今,他们通过在烟囱中安装了过滤装置,可以有效地控制________的排放;安装烟囱净化洗涤装置(如图所示)可以除去废气中部分有害气体,根据该装置的净化原理分析,被除去的有害气体所具有的共同性质是______________________。
(2)按规定汽车应安装尾气处理装置,如在排气管上安装催化转化装置,使尾气中的一氧化碳与一氧化氮在催化剂的作用下,转化为二氧化碳和氮气,该反应的化学方程式为 __________ __________________。
(3)在控制大气污染方面,你认为还有哪些措施或途径,请写出其中的一种:
_____________________________________________________________________________。
三、计算题(10分)
29.(4分)磷酸二氢钾(KH2PO4)大晶体应用于我国研制的巨型激光器“神光二号”中。试计算:
(1)磷酸二氢钾的相对分子质量; (2)磷酸二氢钾中各元素的质量比;
(3)多少千克的磷酸二氢钾与43.5kg硫酸钾中含钾量相等。
30.(6分)将10g不纯的锌粒(杂质不溶于水也不溶于酸)投入到100g稀硫酸中完全反应,得到了0.2g气体。试计算:
(1)锌粒的纯度;(2)参加反应的稀硫酸的质量分数;
(3)反应得到的溶液的溶质质量分数;
(4)如果我们要用98%的浓硫酸来配制500g反应使用的稀硫酸,需要浓硫酸多少毫升?水多少毫升?(浓硫酸的密度为1.84g/mL
四、实验题(13分)
31.(3分)化学实验操作中,有很多步骤是需要有“先”与“后”,对化学实验结果、师生安全等具有十分重要的意义。我们在进行化学实验时,若遇到下列情况,应如何操作。
例:给试管中的药品加热,必须先预热,后集中加热;
(1)点燃可燃性气体(如CO等)时,都要先_____________,后点燃;
(2)CO还原Fe2O3实验结束时,要先______________,后___________________。
(3)类似情况,请你再举出一例:
________________________,要先___________________,后__________________。
32.(6分)根据下图所示的实验装置图回答:
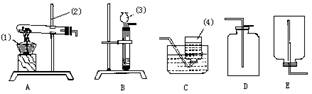 |
(1)写出设有编号的仪器名称:
①_______________;②______________;③_____________;④____________。
(2)实验室用高锰酸钾制氧气时,应选用的发生装置是________,收集装置___________。
(3)实验室制取二氧化碳时应选用的发生装置是___________,收集装置为___________。
(4)装置B可制取的气体除了上述的气体之外,还有_____________等。
(5)实验室用块状固体硫化亚铁(FeS)与稀硫酸反应制取硫化氢(H2S)气体,硫化氢气体的密度比空气的密度大,能溶于水形成氢硫酸。根据以上知识推断:实验室制取硫化氢气体应选用的发生装置为_____________________,收集装置为__________________。
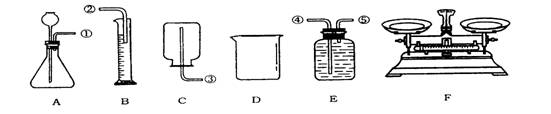 33.(4分)某化学兴趣小组的同学将一块锌铜合金加工成粉末,并称取相同质量的样品数份,用稀硫酸和下图所示的适当装置进行实验,粗略测定合金中铜和锌的质量分数。
33.(4分)某化学兴趣小组的同学将一块锌铜合金加工成粉末,并称取相同质量的样品数份,用稀硫酸和下图所示的适当装置进行实验,粗略测定合金中铜和锌的质量分数。
实验方案如下:
(1)甲同学的方案:取定量样品一份,加入稀硫酸至气体不再产生,测出氢气体积,求出氢气质量,再根据化学方程式进行计算。)采用该方案进行实验,应选用的装置有(用字母表示)______________,组装装置时导管口的连接顺序是(填导管接口处序号)_________________________________。
(2)乙同学的方案:取定量样品一份,加入足量的稀硫酸充分反应,称出铜的质量,再进行计算。
采用该方案进行实验,需要增加的玻璃仪器有________________________________。
(3)丙同学认为只选用D、F进行实验,也可以粗略的测定出合金中锌和铜的质量分数。请分析丙同学的实验方案,采用该方案进行实验,如果要使称量的次数最少,应该称量的数据有________________________。
五、探究题(6分)
34.当学完溶液的性质的相关内容,某学校的初三学生了解到了某些溶液能够导电,老师就留下了一道思考题:溶液导电的原因是什么?为此,同学开始了讨论,假设有很多:
同学甲:我认为,溶液形成时,构成物质的微粒被分散到溶液中,可以自由移动的缘故。
同学乙:某些物质是由离子构成的,离子是带电的微粒,我觉得这正是溶液导电的原因。
同学丙:…………
如果你是该班级的学生,你的假设是______________________________________________。
请你设计具体的对比实验,证明你的假设正确性(在空格中填写缺少的仪器及试剂)
实验仪器:导线若干、小电珠、电池组、________、石墨电极、玻璃棒等。
实验试剂:蔗糖固体、食盐固体、______等。
实验步骤:
| 实验步骤 | 实验现象 | 实验结论 |
| 总结:溶液导电的原因是______________________________________________________。 | ||
张家港市永联学校初三化学2004―2005学年度第 一 学 期期末考试试卷答案
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | B | B | A | C | C | C | B | B | D |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | C | C | B | D | D | B | C | C | B |
二、填空题
|
20.2Na+ 3OH- O2 Na2CO3 nSi Cl
21.Fe+2HCl=FeCl2+H2↑ 置换反应
CaCO3 高温=CaO+CO2↑ 分解反应
![]() 化合反应
化合反应
Na2CO3+2HCl=2NaCl+ H2O+ CO2↑
CO2+2NaOH= H2O + Na2CO3
22.⑴12.5 50 ⑵100
23.多孔疏松 致密的氧化膜
24.燃烧产生热,促使酒精和水分挥发,带走热量,使手帕无法达到着火点
25.可燃物 温度达到着火点 东风或氧气
26.⑴⑵NaCl >24 ⑶降温结晶 ⑷66.9%
27.水面上升 棕色消失
28.⑴这样还是污染了上层空气 粉尘 易溶于水
⑵![]()
⑶控制矿质、原煤的合理燃烧等合理答案均可
三、计算题
29.⑴Mr(KH2PO4)=39+2+31+64=126
⑵m(K)∶m(H)∶m(P)∶m(O)=39∶2∶31∶64
⑶设磷酸二氢钾的质量为x
![]()
![]()
x=63kg
答:略
30. 解:设反应的锌粒质量为x,参加反应的稀硫酸溶质质量为y,反应后生成的硫酸锌质量为z
Zn+H2SO4=ZnSO4+H2↑
65 98 161 2
x y z 0.2g
![]()
![]()
![]()
⑴锌粒的纯度=![]()
⑵参加反应的稀硫酸的质量分数=![]()
⑶反应得到的溶液的溶质质量分数=![]()
⑷设需要浓硫酸的体积为a
a×1.84g/ml×98%=500g×15.1% a=41.87ml
V(H2O)=![]()
答:略
四、实验题
31.⑴验纯 ⑵停止加热 停止通氢气 ⑶CO还原CuO实验开始时 通CO 加热
32.⑴酒精灯 铁架台 长颈漏斗 集气瓶 ⑵A C或D ⑶B D ⑷H2 ⑸B D
33.⑴AEB ①⑤④② ⑵漏斗 玻璃棒
⑶反应前金属、烧杯和溶液的总质量、反应后烧杯和溶液的总质量
五、探究题
34.溶液导电原因是由于溶液中存在着自由移动的离子 烧杯 蒸馏水
| 实验步骤 | 实验现象 | 实验结论 |
| ⑴取少量食盐溶于水,形成食盐溶液,用导线、小电珠、电池组、石墨电极等测其导电性 ⑵分别取少量蔗糖固体、食盐固体、蒸馏水,分别测它们的导电性 | 发现小电珠亮了 发现小电珠均不亮 | 食盐溶液能够导电 蔗糖固体、食盐固体、蒸馏水均不导电 |
| 溶液中存在着自由移动的离子 | ||
注:其他合理答案均可,注意“对比”
 一氧化氮
一氧化氮