海淀区初三化学一模试卷
(答题时间:120分钟)
一. 选择题:(每小题只有一个选项符合题意,每小题1分,共30分)
1. 在下列各组物质的变化中,前者是物理变化,后者是化学变化的是( )
A. 钢锭轧成钢条,工业制氧
B. 电解水制氧气,冰变成水
C. 空气液化,煤燃烧
D. 蜡烛燃烧,蜡烛受热熔化
2. 下列化合物中,氯元素的化合价最低的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
3. 下列各物质的分类中,有错误的是( )
A. 氧化物:干冰、水
B. 酸:氢氯酸、硝酸
C. 碱:纯碱、烧碱
D. 盐:明矾、石灰石
4. 下列说法正确的是( )
A. 均一、稳定的液体都是溶液
B. 131.6克硝酸钾溶液蒸干得31.6克硝酸钾,硝酸钾溶解度为31.6克
C. 浓溶液一定是饱和溶液
D. 温度升高,固体溶解度不一定都增大
5. 硫在氧气里燃烧时产生( )
A. 蓝紫色火焰 B. 白烟
C. 耀眼强光 D. 淡蓝色火焰
6. 下列化学方程式正确的是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
7. 医生建议患甲状腺肿大的病人多食海带,这是因为海带中含有较丰富的( )
A. 氟元素 B. 碘元素
C. 锌元素 D. 钙元素
8. 下列物质不能在饮用品中出现的是( )
A. 乙醇 B. 甲醇
C. 醋酸 D. 水
9. 当前世界上最重要的三大化石燃料是( )
A. 氢气、煤、石油 B. 煤、石油、天然气
C. 煤、石油、一氧化碳 D. 氢气、一氧化碳、碳
10. 下列物质中,既有可燃性又有还原性的气体单质是( )
A. 氢气 B. 活性炭
C. 一氧化碳 D. 二氧化碳
11. 氯化钠、碳酸钠、![]() 、生石灰溶于水,其溶液能使石蕊试液变红的是()
、生石灰溶于水,其溶液能使石蕊试液变红的是()
A. 氯化钠 B. 碳酸钠
C. 二氧化碳 D. 生石灰
12. 下列各组物质能发生反应,并且有氯化铜生成的是( )
A. 铜和盐酸 B. 氧化铜和盐酸
C. 铜和氯化银 D. 氯化钠溶液和氧化铜
13. 区别氢气、氧气、二氧化碳的方法是( )
A. 将燃着的木条分别伸入三种气体的集气瓶中
B. 将气体分别通入澄清石灰水
C. 将气体分别通过灼热的氧化铜
D. 将气体分别通入灼热的铜网
14. 已知:甲为固体,乙、丙、丁为气体,在一定条件下,它们之间可发生下列反应:甲+乙→丙;乙+丁→丙;甲+丙→丁,则甲可能是()
A. ![]() B.
B. ![]() C.
C. ![]() D. C
D. C
15. 下列溶液中通入(加入)括号中的物质,能使溶液中的pH明显增大的是( )
A. 饱和石灰水(二氧化碳)
B. 稀硫酸(氯化钡)
C. 氢氧化钙的饱和溶液(碳酸钠)
D. 稀盐酸(氢氧化钠溶液)
16. 下列各组物质的溶液混合,如果其中的酸过量,仍有沉淀生成的是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
17. 下列实验操作,正确的是( )
A. 把水倒入盛浓硫酸的量筒里
B. 把氢氧化钠放在天平托盘上的滤纸上称量
C. CO还原氧化铜完毕,先停止通CO,再熄灭酒精灯
D. 制取氧气结束时,先将导管移出水面,再熄灭酒精灯
18. 在盛放酒精的试剂瓶的标签上应印有下列警示标记中的( )
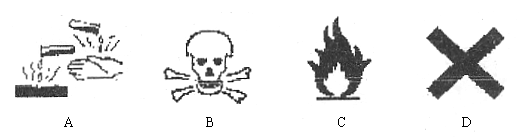
19. 下列物质中不属于合金的是( )
A. 生铁 B. 不锈钢 C. 铁锈 D. 锰钢
20. 能保持氧气化学性质的微粒是( )
A. 氧元素 B. 氧离子
C. 氧原子 D. 氧分子
21. 国际上推广使用中国铁锅,这是因为铁锅( )
A. 是单质 B. 含碳,属于混合物
C. 化学性质活泼 D. 易使食物中含人体所需的铁元素
22. 过氧化氢(![]() )是隐形眼镜的洗液成份,下列说法正确的是()
)是隐形眼镜的洗液成份,下列说法正确的是()
A. 它是由氢气和氧气组成
B. 它是由两个氢元素和两个氧元素构成
C. 它是由氢元素和氧元素组成
D. 它是由一个氢分子和一个氧分子构成
23. 在化合反应、分解反应、置换反应、复分解反应四类反应中,可能生成水的反应共有( )
A. 1类 B. 2类 C. 3类 D. 4类
24. 将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清的石灰水变浑浊,珍珠中一定含有下列离子中的( )
A. 氯离子 B. 硫酸根离子
C. 碳酸根离子 D. 氢氧根离子
25. 在![]() 反应中,已知34 g A与80 g B完全反应生成54
g D,若已知C的相对分子质量为30,则A的相对分子质量为( )
反应中,已知34 g A与80 g B完全反应生成54
g D,若已知C的相对分子质量为30,则A的相对分子质量为( )
A. 68 B. 34 C. 17 D. 51
26. 下列关于金属的用法,说法正确的是( )
A. 用铅制作铅笔芯
B. 用钨制灯丝
C. 用铝箔包装食品更好
D. 古代人用铁比用铜历史早
27. 50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐)。则反应产生氢气的质量是()
A. 2g B. 3g C. 3.5g D. 4.5g
28. X、Y、Z、Q四种元素的核电荷数分别为a、b、c、d,若它们的离子![]() 、
、![]() 的电子层数相同,则下列关系正确的是()
的电子层数相同,则下列关系正确的是()
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
29. 下图中A、B、C、D是立在水田中电线杆的铁丝拉线的四个部位,其中最易生锈的是( )
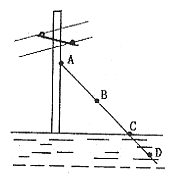
A. A处 B. B处 C. C处 D. D处
30. ![]() 的混合物中,氢元素的质量分数为y,则碳元素的质量分数为()
的混合物中,氢元素的质量分数为y,则碳元素的质量分数为()
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
二. 填空题(32题每空0.5分,其余每空1分,共26分)
31. 某微粒的结构示意图为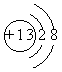 。该元素的原子:核内有__________________个质子、最外层上有__________________个电子,该元素属(金属或非金属)__________________元素。该元素的单质放入稀硫酸中除产生气泡外,还生成另一种物质,写出该反应的化学方程式____________________________________。
。该元素的原子:核内有__________________个质子、最外层上有__________________个电子,该元素属(金属或非金属)__________________元素。该元素的单质放入稀硫酸中除产生气泡外,还生成另一种物质,写出该反应的化学方程式____________________________________。
32. 按要求写出下列化学符号。
(1)钠元素__________________
(2)负二价的氧元素__________________
(3)硫酸根离子__________________
(4)氩气__________________
(5)两个氢分子__________________
(6)三个铁原子__________________
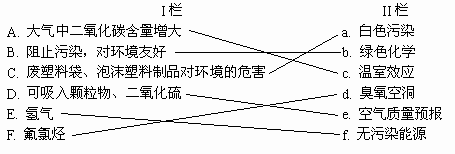
33. 将I与II栏中相互有联系的内容用直线连接起来。
| I栏 | II栏 |
| A. 大气中二氧化碳含量增大 B. 阻止污染,对环境友好 C. 废塑料袋、泡沫塑料制品对环境的危害 D. 可吸入颗粒物、二氧化硫 E. 氢气 F. 氟氯烃 | a. 白色污染 b. 绿色化学 c. 温室效应 d. 臭氧空洞 e. 空气质量预报 f. 无污染能源 |
34. 有铁、盐酸、烧碱溶液和硫酸铜溶液四种物质。根据要求写出由上述四种物质作为反应物的化学方程式各一例:
(1)反应前后溶液总质量不变的反应_________________________。
(2)反应后溶液质量增加的反应_____________________________。
(3)反应后溶液质量减小的反应_____________________________。
35. 某工厂有甲、乙、丙三个车间,各自排放的污水中均无沉淀物,各车间的污水分别含有以下六种物质中的各两种:![]() (注意
(注意![]() 与
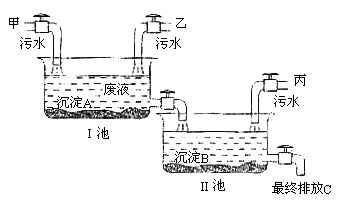
与![]() 不能共存)。为防止污染水源,某中学化学兴趣小组配合工厂进行污水检测,结果如下表。可确定丙车间排放的污水中含有______________。为变害为利,化学兴趣小组与工厂研究设计如下图污水处理方案。问:沉淀A、沉淀B分别是______________、______________。若各步处理均完全反应,最终排放液C的溶质是______________,在农业上它可用作复合肥料。
不能共存)。为防止污染水源,某中学化学兴趣小组配合工厂进行污水检测,结果如下表。可确定丙车间排放的污水中含有______________。为变害为利,化学兴趣小组与工厂研究设计如下图污水处理方案。问:沉淀A、沉淀B分别是______________、______________。若各步处理均完全反应,最终排放液C的溶质是______________,在农业上它可用作复合肥料。

36. 将![]() 和
和![]() 混合气体依次通过足量的
混合气体依次通过足量的![]() 溶液、氢氧化钠溶液、灼热铁丝、灼热氧化铜、浓硫酸最后剩下的气体是__________________。
溶液、氢氧化钠溶液、灼热铁丝、灼热氧化铜、浓硫酸最后剩下的气体是__________________。
37. 下图是某学生设计的一种有洗气、检验、储气等用途的装置。
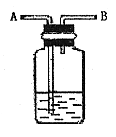
(1)当除去氧气中混有的水蒸气时,混合气体应从__________________(填“A”或“B”)处导管进入,瓶中盛有的物质可以是__________________;
(2)当检验实验室制取氢气中是否含有氯化氢时,瓶中盛有的试剂可以是_____________。
(3)当用排水取气法收集一氧化碳时,瓶内先装满水,气体从_____________(填“A”或“B”下同)处导管通入。若要用水将瓶中一氧化碳排出使用,水应从____________处导管进入。
三. 实验题(39题第3空2分,41题(1)每空0.5分,其余每空1分,共16分)
38. 用一个大的饮料瓶收集二氧化碳,迅速倒入约10毫升的饱和的M溶液,马上用橡皮塞将瓶口密封好,塑料饮料瓶很快瘪了,则M溶液中溶质的化学式可能为____________,试写出有关的化学方程式_______________________;再用注射器将饱和N溶液从橡皮塞处注入,已经变瘪的饮料瓶又渐渐鼓起来了。则N溶液中溶质的化学式可能为____________,试写出有关的化学方程式________________________。
39. 通过实验探究的方法对未知事物进行探索是化学学习的一种重要学习方式。请回答下列有关问题:
小明在研究某气体(纯净物)的性质时做了如下实验:“将铜丝绕成螺旋状放在酒精灯火焰上加热,铜丝表面由光亮的红色变为黑色,趁热将表面变黑的铜丝放入盛有这种气体的集气瓶中并密闭集气瓶,观察到铜丝表面的黑色又变为光亮的红色。”上述变化中黑色物质是(写名称)____________,根据实验现象推断这种气体可能是(要求写一种化学式)____________。如果要验证你的推断,在上述密闭集气瓶中,还需要继续进行的实验是(步骤、现象、结论)________________________________________________。通过以上探究,该气体具有的化学性质是________________________。
40. 如下图所示,烧杯内盛有一定量的稀硫酸,闭合开关后往烧杯内逐滴加入![]() 溶液直至过量。在整个过程中:
溶液直至过量。在整个过程中:
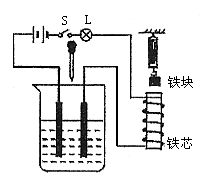
(1)灯L的亮度变化情况是:____________________________________
(2)灵敏弹簧秤的读数变化情况是:____________________________________
41. 根据下图所示,回答问题。
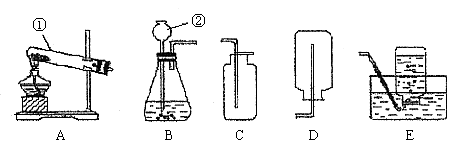
(1)写出下图中有标号仪器的名称①____________,②____________。
(2)在实验室中,常用加热固体![]() 和
和![]() 混合物的方法制氨气。已知在标准状况下,氨气的密度为0.771 g/L(空气:1.293 g/L),且在常温常压下,1体积的水能溶解700体积的氨气,氨气的发生装置应选用________________________,收集装置应选用________________________。
混合物的方法制氨气。已知在标准状况下,氨气的密度为0.771 g/L(空气:1.293 g/L),且在常温常压下,1体积的水能溶解700体积的氨气,氨气的发生装置应选用________________________,收集装置应选用________________________。
(3)用C装置收集二氧化碳气体时,可用____________放在____________来检查是否已充满二氧化碳。
四. 计算题(8分)
42. 用2000吨含氧化铁80%的赤铁矿,可炼出含铁95%的生铁多少?(杂质中不含铁),用一氧化碳还原这些氧化铁,需用一氧化碳多少?(最后结果精确到0.1)
43. 取碳酸钠和氯化钠的固体混合物13.6g,与一定质量的稀盐酸恰好完全反应,得到10%的氯化钠溶液147g。计算:(最后结果精确到0.1%)
(1)固体混合物中碳酸钠的质量分数;
(2)生成二氧化碳的质量;
(3)该盐酸的溶质的质量分数。
【试题答案】
相对原子质量:Mg�24,Zn�65,Fe�56,C�12,H�1,O�16,N�14,Na�23,Cl�35.5,Cu�64
一. 选择题:(每小题只有一个选项符合题意,每小题1分,共30分)
1. C 2. B 3. C 4. D 5. A 6. C
7. B 8. B 9. B 10. A 11. C 12. B
13. A 14. D 15. D 16. C 17. D 18. C
19. C 20. D 21. D 22. C 23. D 24. C
25. C 26. B 27. C 28. B 29. C 30. A
二. 填空题(32题每空0.5分,其余每空1分,共26分)
31. 13,3,金属,![]()
32. (1)![]() ;(2)
;(2)![]() ;(3)
;(3)![]() ;(4)
;(4)![]() ;(5)
;(5)![]() ;(6)
;(6)![]()
33.
34. (1)![]()
(2)![]()
(3)![]()
35. ![]()
36. ![]()
37. (1)A,浓硫酸
(2)硝酸银溶液
(3)B,A
三. 实验题(39题第3空2分,41题(1)每空0.5分,其余每空1分,共16分)
38. ![]() (答案合理就给分)
(答案合理就给分)
![]() (答案合理就给分)
(答案合理就给分)
39. 氧化铜,![]() 或CO
或CO
![]() :往上述密闭集气瓶中加入少量白色的无水硫酸铜粉末,
:往上述密闭集气瓶中加入少量白色的无水硫酸铜粉末,
若粉末变蓝,说明![]() 与氧化铜反应生成了水,则推断成立。
与氧化铜反应生成了水,则推断成立。
(![]() :往上述密闭集气瓶中注入适量澄清的石灰水,若出现浑浊,说明该气体与氧化铜反应生成了二氧化碳,则推断成立。)
:往上述密闭集气瓶中注入适量澄清的石灰水,若出现浑浊,说明该气体与氧化铜反应生成了二氧化碳,则推断成立。)
还原性
40. (1)灯L的亮度逐渐变暗直至熄灭,又逐渐变亮。
(2)读数先变小,后来又变大。
41. (1)①试管;②长颈漏斗
(2)A,D
(3)燃着的木条,集气瓶的瓶口
四. 计算题(8分)
42. 解:2000吨赤铁矿中氧化铁的质量=2000吨×80%=1600吨
铁元素的质量=1600吨×2![]() =1120吨
=1120吨
生铁的质量=1120/95%=1178.9吨(1分)
设:参加反应的一氧化碳的质量为x
![]() (1分)
(1分)
160 3×28
1600吨 x
![]()
![]() 吨(1分)
吨(1分)
答:略。
43. 解:设混合物中碳酸钠的质量为x,生成的二氧化碳的质量为y,反应生成的氯化钠的质量为z
![]() (1分)
(1分)
106 73 117 44 ![]() (1分)
(1分)
x z y ![]()
![]() (1分)
(1分)
碳酸钠的质量分数![]() (1分)
(1分)
设:稀盐酸的质量为m,根据质量守恒定律
![]()
![]() (1分)
(1分)
答:(略)