化学单元练习(1、2章)2006.9.8
班级 姓名 成绩
一、选择题(每小题只有一个选项符合题意,答案填入下表。每小题2分,共30分。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 |
1. 如果没有化学的发展,世界就不可能像今日这样丰富多彩。下列事实与化学没有密切关系的是:
A.食物、衣料和日常用品的丰盛 B.新材料的开发和利用
C.环境污染的预防和治理 D.物体机械运动的规律
2. 人类生活需要能量。下列能量主要由化学变化产生的是:
A.电水壶烧开水时需要的热量 B.水电站利用水力发出的电能
C.点燃的酒精灯放出的热能 D.风力发电站所利用的风能
3.
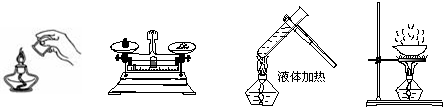 下列实验操作正确的是:
下列实验操作正确的是:
A B C D
4. 下列现象中,与蜡烛燃烧时所观察到的现象不符的是:
A.发出黄白色的火焰
B.火焰上方如果罩一干燥烧杯时能发现烧杯内壁上有水珠
C.蜡烛靠近火焰处熔化变成液体
D.蜡烛燃烧时浓烟滚滚
5. 下列实验中不含有分解反应的是:
A.加热碳酸氢铵固体 B.木炭在氧气中燃烧
C.用双氧水制氧气 D.用高锰酸钾制氧气
6. 水可以造福人类,但水被污染后就会给人类造成灾难。为了防止水的污染,下面①~⑤项措施合理的是:
①控制水中所有动、植物的生长 ②不任意排放工业废水
③绝对不许施用农药、化肥 ④生活污水经过净化处理后再排放
⑤控制二氧化硫和二氧化氮的排放,防止酸雨的形成
A.①④⑤ B.①③⑤
C.②③④ D.②④⑤
7. 下列用途中,不属于氮气的用途的是:
A.用作粮食瓜果的保护气 B.用作灯泡填充气
C.制氮肥 D.制霓虹灯
8. 下列变化中,不属于缓慢氧化的是:
A.牛奶变酸 B.钢铁生锈
C.镁条在空气中燃烧 D.农家肥料腐熟
9. 日常生活中下列物质可以看作是纯净物的是:
A.矿泉水 B.酸牛奶
C.冰水 D.自来水
10.
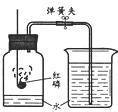 某班同学用右图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是
某班同学用右图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是
①甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
②甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
③乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
A.只有①③ B.只有②④
C.只有①②③ D.只有①②③④
11. 水是宝贵的自然资源,以下关于水的叙述中正确的是:
A.冰的密度大于水的密度 B.水由氢气和氧气组成
C.硬水和软水可用肥皂水区别 D.淡水资源取之不尽
12. 建设节约型社会人人有责。下列节约行为中合理可行的是:
A.直接用工厂排出的废水灌溉农田
B.吃经高温蒸煮后的霉变大米
C.把用剩的药品放回原试剂瓶
D.用淘米、洗菜水、洗衣服的水浇花、拖地、冲厕所
13. 下表是三种气体的密度(在0℃、101kPa条件下测定)和溶解程度。实验室要收集二氧化硫气体,可采取的方法是:
| 气体 性质 | 氢气 | 二氧化碳 | 二氧化硫 |
| 密度(g・L-1) | 0.08987 | 1.975 | 2.716 |
| 溶解程度 | 极难溶于水 | 能溶于水 | 易溶于水 |
A.向上排空气法 B.向下排空气法
C.排水集气法 D.无法判断
14. 实验室制取二氧化碳一般有如下5步:①检查装置气密性;②按要求装配好仪器;③向漏斗中注入稀盐酸;④向锥形瓶中加几小块大理石;⑤收集气体。正确的操作顺序是:
A.①②③④⑤ B.②①④③⑤
C.①④②③⑤ D.②③④①⑤
15. 在一密闭容器中充满空气,经测定其中含氮气体积为100L,则其中氧气的体积约为:
A.20L B.30L C.25L D.40L
二、选择题(每小题有1~2个选项符合题意,答案填入下表。每小题2分,共10分。)
| 题号 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
16. 将实验室制取二氧化碳和用高锰酸钾制取氧气相比较,下列说法正确的是:
A.气体发生装置可能相同 B.反应条件相同
C.气体收集方法可能相同 D.反应的基本反应类型相同
17. 为了区别O2与CO2两瓶(或两种)无色气体,下列方法中不可行的是
A. 分别通入紫色石蕊溶液中
B. 用燃着的木条分别伸入瓶中
C. 分别闻气味
D.用塑料可乐瓶分别盛满上述两种气体,各倒入1/5容积的水,盖紧瓶盖,振荡
18. 下列化学反应中,属于化合反应的是:
![]()
![]()
![]()
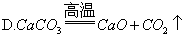
19. 下列叙述中,错误的是:
A.用量筒量取液体时,视线与液体凹液面最低处保持水平
B.可以向燃着的酒精灯中添加酒精
C.含硫火柴燃烧产生的二氧化硫气体能使紫红色的高锰酸钾溶液退色
D.蒸发食盐水得到食盐固体时,应加热至水分完全蒸干才能停止加热
20. 超临界流体是一种介于液、气两态之间的物质,有着超强的溶解能力。超临界流体有水、二氧化碳、甲烷、乙烯、乙醇等,其中超临界H2O流体和超临界CO2流体又被誉为“绿色环保溶剂”。下面关于超临界H2O流体和超临界CO2流体的说法正确的是
A.超临界CO2流体可替代许多有害、有毒、易燃的有机溶剂
B.超临界H2O流体的密度仍为1 g/cm-3
C.超临界CO2流体是一种特殊的物质,容易燃烧
D.超临界H2O流体性质特殊,与普通水的组成不一样
三、填空题(每空1分,共24分)
21. 下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明。
| 配 料 | 含 碘 量 |
| 氯化钠、碘酸钾 | (20mg~40mg)/kg |
| 贮藏指南 | 食用方法 |
| 避热、避光、密封 | 勿长时间炖炒 |
试回答:
(1)“加碘食盐”属于 (选填“纯净物”或“混合物”)
(2)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是 。
(3)根据你们生活经验写出碘酸钾的物理性质之一是 。
22. 哪些事实说明空气中含有下列成分?
(1) ,说明空气中含有氧气。
(2) ,说明空气中含有水蒸气。
(3) ,说明空气中含有二氧化碳。
23. 用文字(或符号)表达式解释下列现象的原因。
(1)向盛有紫色石蕊试液的试管中通入适量的CO2,溶液变为红色;
;
(2)通入CO2变红的石蕊试液,加热后又变成紫色;
。
24.

![]() 干冰是固态的二氧化碳,在常温下易升华,右图是干冰升华时的情景,根据图中信息,从“
”这一角度分析干冰具有的性质和用途。
干冰是固态的二氧化碳,在常温下易升华,右图是干冰升华时的情景,根据图中信息,从“
”这一角度分析干冰具有的性质和用途。
⑴干冰升华时 (填“吸收”或“放出”)大量热,因此可作致冷剂或用于人工降雨。
⑵干冰转化成二氧化碳气体后能参与绿色植物的光合作用,故在大棚蔬菜种植中作 。
⑶ 。
25. 二氧化碳是导致地球上发生“温室效应”的主要气体,现代人类已意识到它的排放必须控制。
(1)空气中二氧化碳的主要来源是 ,绿色植物通过光合作用吸收二氧化碳,同时放出 (填名称)。
(2)为了减缓大气中二氧化碳含量的增加,以下建议合理的是 (填序号)。
①开发太阳能、水能、风能、地热等能源;
②减少化石燃料的使用;
③大量植树种草,禁止乱砍滥伐。
26. 电解水实验中,在水中加入稀硫酸或氢氧化钠的作用是 ,在电源的正负两极分别产生 和 气体,其体积比是 ,其中正极的气体能使燃烧着的木条 ,而负极产生的气体遇到燃烧的木条能 。该实验说明了 。
27. 茶叶中含有的茶多酚有益人体健康。茶多酚是一种白色粉末,易溶于热水,易氧化变色,略有吸水性。实验室从茶叶中提取茶多酚的步骤可简述为:
 |
(1)请写出上述实验过程中的操作名称:操作① ,操作② ;
(2)保存茶多酚晶体时应注意 。
四、实验题(每空1分,共36分)
28. 写出下列实验所需仪器的名称(各写一种)
(1)量取一定体积的液体需用 ;
(2)用作收集或贮存少量气体时需用 ;
(3)溶解较多量固体时用 ;
(4)给试管里的物质加热时需用的热源是 ;
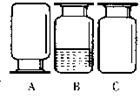 (5)少量试剂反应时需用容器为
。
(5)少量试剂反应时需用容器为
。
29. 在实验室里分别用集气瓶收集氧气、氢气和二氧化碳三种气体,
如图所示,图中:A中是__________,
B中是__________,C中是____________。
30. 请根据下图所示的实验装置图填空。
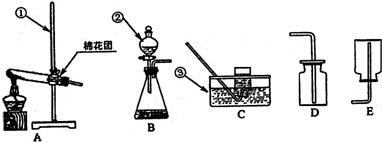
(1)指出图中标有数字的仪器的名称:① ,② ,③ 。
(2)在实验室用高锰酸钾制氧气时,试管口的棉花团的作用是 ,写出反应的文字(或符号)表达式: 。
(3)当用B装置制取氧气时,仪器②内盛放的液体是 ,仪器②的作用是
。
(4)在实验室制取并收集二氧化碳可选用 装置(填序号),写出实验室制取二氧化碳常用反应的文字(或符号)表达式: 。
31. 课堂上老师做了一个实验:将液态空气倒入一只烧杯中,发现立即冒出大量气泡,把一根燃着的小木条置于烧杯口,小木条火焰熄灭;过一会儿再把燃着的小木条置于烧杯口,此时小木条不但没有熄灭,反而燃烧更旺。据此实验现象回答下列问题:
(1)由于液氮的沸点比液氧的沸点 (填“高”或“低”)导致 首先从液态空气中蒸发出来;
(2)“过一会儿,小木条不但没有熄灭,反而燃烧更旺”,其原因是
。
32. 下表是研究性学习小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据: 用10mL H2O2制取150mL所需的时间(秒)
| 浓度 反应条件 | 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
请你分析回答:
(1)该研究小组在设计方案时。考虑了浓度、 、 等因素对过氧化氢分解速率的影响。
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?
。
33. 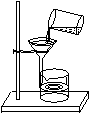 如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤。
如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤。
(1)加明矾的作用是__________________________________________。图中缺少的一种仪器是______________,其作用是_________________;漏斗下端紧靠在烧杯内壁是为了________________________________。
(2)过滤实验中除了漏斗下端紧靠在烧杯内壁以外,还要注意些什么?
___________________________________________________________;_____________________________________________(至少写出两种)。
(3)过滤后,小新发现,滤液仍然浑浊,可能的原因是_________________________________。
小新改进了实验,得到了澄清透明的水,如果他想制取纯水,还需采用净化的方法______。
34. 小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫过氧化钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙来制取氧气。
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可作增氧剂、杀菌剂等。
【猜想与验证】
(1)小明依据 ,提出猜想Ⅰ。
猜想Ⅰ:加热过氧化钙可制取氧气。
| 实验装置 | 实验主要过程 |
|
| ①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到 ,松开手后,有液体进入导管。 ②加入过氧化钙,加热,导管口有大量气泡冒出。 ③收集满一瓶气体。 ④停止加热。熄灭酒精灯前,应先 。 |
【实验结论】加热过氧化钙可制取氧气。
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想II。
猜想II:过氧化钙与水反应可制取氧气
| 实验装置 | 实验主要过程 |
|
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出。 |
【实验结论】不能用过氧化钙与水反应可制取氧气。
【分析与反思】
①虽然没有快速收集到大量氧气,由此实验现象,小明认为农民用过氧化钙作增氧剂的主要原因是 。
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议是 。
以上建议是否可行,还需进一步通过实验验证。
参考答案
一、选择题:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 | D | C | A | D | B | D | D | C | C | D | C | D | A | B | C |
二、选择题
| 题号 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | C | A、C | B、D | A |
三、填空题:
21.(1)混合物(2)受热、见光易分解(3)白色固体或易溶于水
22.(1)蜡烛在空气中可以燃烧等。(2)在空气中盛有冰水的杯子外壁会出现水珠等。(3)澄清石灰水长期露置空气中,表面出现一层白膜等。
23.(1)二氧化碳+水→碳酸(2)碳酸→水+二氧化碳
24.(1)吸收(2)气体肥料(3)二氧化碳不可燃、不支持一般可燃物的燃烧,密度比空气大,故可用于灭火。
25.(1)化石燃料的燃烧、生物的呼吸作用等(2)氧气(3)①②③
26.增强水的导电性, 氧气、氢气, 1:2, 燃烧更旺, 燃烧, 水由氢氧两种元素组成。
27.(1)①过滤②蒸发(结晶) (2)隔绝氧气和水或密封保存
28.(1)量筒(2)集气瓶(3)烧杯(4)酒精灯(5)试管
29.A中氢气 B中氧气 C中二氧化碳
30.(1)①铁架台②分液漏斗③水槽
(2)防止高锰酸钾粉末进入导管,堵赛导管,高锰酸钾→锰酸钾+二氧化锰+氧气
(3)双氧水,控制液体滴加速度和加液量,从而控制反应速率
(4)B、D 碳酸钙+盐酸 →氯化钙+二氧化碳+水
31.(1)低 液态氮气(2)液氮蒸发完全后液氧蒸发,氧气支持木条燃烧
32.(1)温度、催化剂(2)温度升高,过氧化氢分解速率加快等
33.(1)吸附水中悬浮杂质而沉降。 玻璃棒 ,引流
(2)滤纸紧贴漏斗内壁;滤纸边缘低于漏斗边缘;漏斗中液面低于滤纸边缘等
(3)滤纸破损或漏斗中液面高于滤纸边缘或承接滤液的烧杯不干净
34.(1)过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气。
导管口有气泡冒出, 将导管移出水面。
(2)①过氧化钙在水中持续缓慢放出氧气。
②加热过氧化钙和水的混合物或加入催化剂。