2006年初中毕业暨升学考试
化 学 模 拟 试 题
| 题号 | 一 | 二 | 三 | 四 | 五 | 总计 |
| 得分 |
可能用到的相对原子质量:K―39 N―14 O―16 Ag―108 C―12 H―1
一、 选择题(本题包括16个题,每小题1分,共16分,每小题只有1个选项符合题意)
1、化学变化的特征是 ( )
A、产生气体或沉淀 B、重量增加,产生热量 C、物质颜色改变 D、有新物质生成
2、下列物质中不属于混合物是 ( )
A、生铁 B、煤 C、胆矾 D、空气
3、水结成冰是因为 ( )
A、分子组成发生了变化 B、分子间的间隔发生了变化
C、分子大小发生了变化 D、分子变成原子
![]() 4、能说明CO2是酸性氧化物是
( )
4、能说明CO2是酸性氧化物是
( )
![]() A、CaCO3+2HCl===CaCl2+H2O+CO2↑ B、CO2+C===2CO
A、CaCO3+2HCl===CaCl2+H2O+CO2↑ B、CO2+C===2CO
C、H2CO3===H2O+CO2↑ D、CO2+Ca(OH)2===CaCO3↓+H2O
5、地壳中含量最多的金属元素是 ( )
A、硅 B、氧 C、铁 D、铝
6、下列变化不属于缓慢氧化的是 ( )
A、食物腐烂 B、呼吸作用 C、铁在潮湿的空气中生锈 D、石蜡的燃烧
7、构成物质的基本粒子有 ( )
A、单质、化合物 B、质子、中子、电子 C、分子、原子、离子 D、酸、碱、盐
8、“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制易拉罐、铜导线等可以归为一类加以回收,它们属于 ( )
A、氧化物 B、盐 C、金属或合金 D、碱
9、今年春季沙尘暴频繁侵袭我国北方地区,会造成空气中下列哪种有害成份增加( )
A、SO2 B、NO2 C、可吸入颗粒物 D、CO
10、空气中体积分数最大的是 ( )
A、氮气 B、氧气 C、二氧化碳 D、水蒸气
11、下列化肥属于复合肥料的是 ( )
A、CO(NH2)2 B、KNO3 C、K2CO3 D、Ca(H2PO4)2
12、决定元素种类的是 ( )
A、核内质子数 B、核外电子数 C、核内中子数 D、相对原子质量
13、下列符号中,既能表示一种元素,又能表示该元素的一个原子,还能表示该元素组成的单质是 ( )
A、Al B、N2 C、Cl D、H
14、露置在空气中,不易发生化学变化的是 ( )
A、白磷 B、石墨 C、烧碱 D、生石灰
15、下列物质中,不属于有机物的是 ( )
A、甲烷 B、酒精 C、醋酸 D、碳酸钙
16、下列物质中,能使紫色石蕊试液变红的是 ( )
A、盐酸 B、氢氧化钠溶液 C、氯化钠溶液 D、蒸馏水
二、 选择题(本题包括12个题,每小题2分,共24分,每小题只有1个选项符合题意)
17、能证明生石灰中含有碳酸钙的最简便的方法是 ( )
A、高温加热 B、滴入碳酸钠溶液 C、加水搅拌 D、滴加稀盐酸
18、下列物质不会使人中毒的是 ( )
A、一氧化碳 B、甲醇 C、氯化钠 D、亚硝酸钠
19、只用一种试剂除去NaNO3溶液中混有的少量CuSO4杂质,应加入适量的( )
A、NaOH溶液 B、Ba(NO3)2溶液 C、Ba(OH)2溶液 D、Na2CO3溶液
20、下列各组物质在同一溶液中能大量共存的是 ( )
A、CuSO4和KNO3 B、Na2SO4和BaCl2 C、FeCl3和KOH D、K2CO3和CaCl2
21、可由金属和稀硫酸直接反应制取的物质是 ( )
A、Fe SO4 B、CuSO4 C、Fe 2(SO4)3 D、Ag2 SO4
22、氢氧化钠固体必须密封保存是因为①易吸收空气中的水蒸气而潮解②具有强腐蚀性③易吸收空气中的CO2而变质④能与酸发生中和反应。正确的说法为 ( )
A、①② B、②④ C、①③ D、①③④
23、根据反应方程式: Na2S2O3+H2SO4===Na2SO4+S+X+H2O 推断X物质的化学式为 ( )
A、SO2 B、SO3 C、H2S D、Na2O
24、若下列四种物质均能溶于水,则在水溶液中一定能发生复分解反应的是( )
A、盐和酸 B、盐和盐 C、盐和碱 D、酸和碱
25、向AgNO3 、Cu(NO3)2 、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后、过滤,不能存在的情况是 ( )
A、滤纸上有Ag ,滤液中有Ag+、Cu2+、Mg2+、Zn2+
B、纸上有Ag、Cu ,滤液中有Cu2+、Mg2+、Zn2+
C、滤纸上有Ag、Cu ,滤液中有Ag+、Mg2+、Zn2+
D、滤纸上有Ag、Cu、Zn ,滤液中有Mg2+、Zn2+
26、下列反应不能一步完成的是 ( )
A、Ba(OH)2 → BaCl2 B、CuO → Cu(OH)2
C、Fe2O3 → Fe D、 BaCl2 → Ba(NO3)2
27、下列物质的稀溶液一般不跟其它物质发生化学反应的是 ( )
A、氯化钠 B、硝酸钠 C、硫酸铵 D、硝酸钙
28、现有A、B、M、N 四种金属,将它们分别投入稀硫酸中,只有M、N发生反应并产生气体。将N投入到M中的硝酸盐溶液中,有金属M析出。将A投入到B的氯化物溶液中,无明显现象,这四种金属的活动性顺序是 ( )
A、N>M>A>B B、N>M>B>A C、B>A>M>N D、M>N>A>B
三、 填空题(6个小题,共36分)
29、(5分)用数字和符号表示下列粒子
⑴ 2个氢原子 ⑵ 2个亚铁离子
⑶ +2价的碳元素 ⑷ 3个一氧化碳分子
⑸ 2个氢氧根离子
30、(6分)现有⑴干冰 ⑵天然气 ⑶氧气 ⑷石墨 ⑸熟石灰 ⑹稀盐酸等六种物质,用化学式填写以下空白:
⑴用于人工降雨的是 。⑵用作火箭中氧化剂的是 。
⑶用作电极材料的是 。⑷用于改良酸性土壤的是 。
⑸可做气体燃料的是 。⑹用于清除铁锈的是 。
31、(3分)结构示意图 2 8 可代表多种微粒。若该示意图代表原子,则X的值为 ;
若X的值为11,则该粒子为 ;若X的值为8,则该微粒与镁离子形成的化合物的化学式为 。
32、(6分)有一包固体粉末,可能由CaCO3 、Na2SO4 、CuSO4 、KNO3 、BaCl2中的一种或几种组成,做实验得以下结果:
⑴将此固体粉末加到水中,得到白色沉淀,上层清液为无色;
⑵该白色沉淀不溶于稀硝酸。
从实验可以判出,该粉末中一定含有 ,一定不含有 ,
可能含有 。
33、(10分)按要求写出反应的化学方程式。
⑴用氢氧化铝治疗胃酸过多: 。
⑵用稀盐酸清洗久盛石灰水的试剂瓶: 。
⑶工业上制取烧碱的化学反应: 。
⑷盐酸除铁锈: 。
⑸实验室不用催化剂的条件制氧气: 。
34、(6分)在做实验时,出现下列情况,请用文字说明有关原因。
⑴铁丝在盛满氧气的集气瓶中燃烧,瓶底破裂。 。
⑵加热高锰酸钾制氧气并用排水法收集时,水槽中的水变成了紫色。 。
⑶用氢气还原氧化铜时,由黑变为红,后来又变为黑色。 。
四、 实验题
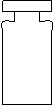
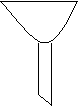
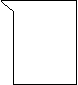
35、(6分)请根据下图回答回答问题:
 | |||||||
 | |||||||
 | |||||||
① ② ③ ④
⑴按序号写出仪器名称:① ② ③ ④
⑵可用于过滤的仪器是(填序号,下同) 用于收集气体的仪器是
36、(6分)为了除去铜粉中少量的铁粉,甲、乙两位同学设计了以下两个实验方案。
甲 加入足量稀H2SO4
![]() Cu(Fe)
Cu
Cu(Fe)
Cu
振荡后过滤
乙 加入CuSO4溶液
![]() Cu(Fe)
Cu
Cu(Fe)
Cu
你认为两个方案中较好的是哪一个,简述理由。
五、计算题
37、(6分)近年来,乳酸成为人们研究的热点之一,乳酸在医药、食品等工业中应用前景广阔。乳酸的化学式为C3H6O3,试计算:
⑴乳酸的相对分子质量?
⑵乳酸中碳、氢、氧元素的质量比?
⑶乳酸中碳元素的质量分数?
38、(6分)为了对氯化钾样品(含少量KNO3)进行分组分析,甲、乙、丙三位同学分别进行实验,他们实验数据如下表,请仔细观察和分析数据,回答下列问题。
| 甲 | 乙 | 丙 | |
| 所取固样品的质量/g | 20 | 10 | 10 |
| 加入AgNO3溶液的质量/g | 100 | 100 | 150 |
| 反应后所得的沉淀质量/g | 14.35 | 14.35 | 14.35 |
⑴三位同学中,哪一位所用的KCl与AgNO3刚好互相完全反应(填写编号) 。
⑵样品中的KCl的质量分数是多少?(小数点后保留两位数字)
⑶三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的滤液是只含有一种溶质的溶液?此溶液的溶质的质量分数是多少?(小数点后保留两位数字)
参 考 答 案
一、 选择题
1、A 2、C 3、B 4、D 5、D 6、D 7、C 8、C 9、C 10、A 11、B
12、A 13、A 14、B 15、D 16、A
二、 选择题
17、D 18、C 19、C 20、A 22、C 23、A 24、D 25、C 26、B 27、B 28、B
![]() 三、29、⑴2H ⑵2Fe2+ ⑶ C ⑷3CO ⑸2OH―
三、29、⑴2H ⑵2Fe2+ ⑶ C ⑷3CO ⑸2OH―
四、30、⑴CO2 ⑵O2 ⑶C ⑷Ca(OH)2 ⑸CH4 ⑹HCl
31、10;钠原子;MgO
32、Na2SO4 BaCl2 、 CuSO4 CaCO3 、 KNO3
33、⑴Al(OH)3+3HCl===AlCl3+3H2O ⑵CaCO3+2HCl===CaCl2+H2O+CO2↑
⑶Ca(OH)2+Na2CO3===CaCO3↓+2NaOH ⑷6HCl+Fe2O3===2FeCl3+3H2O
![]() ⑸2KMnO4===K2MnO4+MnO2+O2↑
⑸2KMnO4===K2MnO4+MnO2+O2↑
34、⑴事前没有在集气瓶中装少量的水或铺一薄层细沙。
⑵试管口没有放一团棉花
⑶实验完毕,没有继续通入一会氢气直到试管冷却
35、⑴①漏斗 ②烧杯 ③试管 ④集气瓶
⑵①② ④
36、甲(2分) 反应充分(2分) 易分离(2分)
五、37、⑴C3H6O3的相对分子质量=3×12+6×1+3×16=90
⑵C : H : O=3×12 : 6×1 : 3×16=6 : 1 : 8
3C
![]() ⑶C%=
×100%=36/90 ×100%=40%
⑶C%=
×100%=36/90 ×100%=40%
C3H6O3
38、⑴乙 …………………………1分
⑵解:设生成14.35克沉淀需消耗氯化钾的质量为x,生成硝酸钾的质量为y。
KCl+AgNO3===AgCl↓+KNO3 …………………………1分
74.5 143.5 101
x 14.35g y …………………………1分
74.5
![]() 143.5
143.5
x 143.5克 x=7.45克。…………………………1分
7.45克
![]() ×100% =74.5%
…………………………1分
×100% =74.5%
…………………………1分
10克
⑶ 乙
143.5
![]() 101
101
14.35克 y y=10.1克 …………………………1分
10.1克+(10克-7.45克)
![]() KNO3%=
×100% =13.23%
KNO3%=
×100% =13.23%
10克+100克-14.35克
答:略。