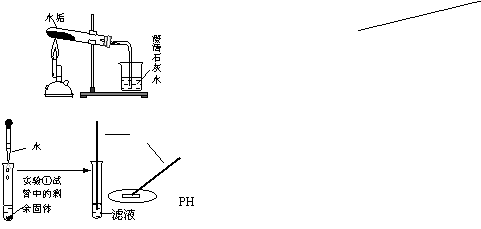
�ֶ�����2005ѧ��ȵ�һѧ����ĩ�������
������ѧ�Ծ� ��(�Ե�ѧУ�½̲�)�������� 06.01
(���ʱ��:90���ӡ��� ����: 100��)
| ��� | һ | �� | �� | �� | �ܷ� |
| �÷� |
�����õ������ԭ�������� H-1 �� C-12 ��N-14����O-16 �� Mg-24����S-32������
һ������� ��ÿ��1�֣���20�֣�
1��������Ӧ���������ƺͻ�ѧʽ��
| �������� | �������� | ʯ�� | ʳ �� | ��ʯ�� | |||
| ��ѧʽ | Fe(NO3) 2 | He | H2CO3 |
2�����뻯ѧ���Ż�ѧ���ű�ʾ�����壺
| ��ѧ���� | H2O |
| NO3 |
| |
| ��ʾ������ | ������ԭ�� | 3������������ |
3��д�����л�ѧ����ʽ��������й����ݣ�
| ��ѧ��Ӧ | ��ѧ����ʽ | ���� |
| ��˿��������ȼ�� | �������������������������� | |
| ���ˮ | ������������������������Ϊ������������ | |
| þ���ڶ�����̼��ȼ�� | ��Ӧ���������Ϊ�������������������������� | |
| ˫��ˮ�ֽ� | ����������_____ɫ�Ĺ��� |
����ѡ���⣨ÿ��1�֣���26�֣�
4���������ڻ�ѧѧ���о����ݵ��ǡ��������������������������������������������������������������������������������������������������������������������������� ������(���� )
A��������ʻ�еļ��٣�
B��ɽ��������DNA�ӽ���������һ������Ķ������ɽ��
C�����������������ת��Ϊ���ܣ�
D���ڴ��������һ�ֿ�ȼ���������о�������ɡ����ʺ���;��
5�����������У�ǰ��������ѧ�仯�������������ʵ��������ʵ��ǡ������������������������� (���� )
A���������ƾ��𡡸ɱ����������� B�������л���̿������ζ������������ˮ
C�������� ̼����в��ȶ��ԡ��� �� D��ú���ж�������������ȼ��
6��ŷ�˹��ҽ��ӽ��������ˮ���¶ȼƣ���Ϊ����ʹ���������飬й©ˮ����Σ��
���彡����ˮ�����ڡ����������������������������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A��������������� B������������ C�����ʡ��� ������D��������
7���͡��Ρ��������dz��õĵ�ζƷ�����е�ζƷ��ˮ��ֻ�ϲ����γ���Һ�ģ� ���� ��
A�������͡�����������������B��ʳ�Ρ���������C�����͡������������� D���״�
8��I2O5�ɲⶨ������Ⱦ�ij̶ȣ��йط�ӦΪI2O5+5CO��I2+5CO2����˵����ȷ���� ( ������)
A��I2O 5����ԭ�������е�Ԫ��Ϊ��2�ۡ����� B��CO����ԭ��������ԭ
C��I2O 5������ԭ��Ӧ�����е�Ԫ��Ϊ��5�ۡ� D��I2O 5�������������е�Ԫ��Ϊ��2��
9��������������ֱ����������������ǡ������������������������������������������������������������������������������������������������������������� (���� )
A���ú���ú��ȼ�ϡ���B��������������C������̫���ܷ��硡 D��ȼ���̻�������
10���÷��ӵĹ۵����������������ǡ����������������������������������������������������������������������������������������������������������������� ��������
A�����������D�D���Ӵ�С���¶ȵı仯���ı䡡B���������硪�����Ӳ�ͣ���˶�
C��ú��ȼ�ա������ӷ����仯���������������������������� D���ƾ��ӷ��������Ӽ������
11��һ�֡���ʳ�����Ϳ�͡��ʺ��������ʱʹ�á����ڲ����������������Ѽӹ��õ�ʳƷ����ȡ��հ�װ�ķ����������ֱ��װ���������ʣ�ʹ��ʱ����Ԥ����������ߣ�ʹ���������ʻ�ϼ�������Ӧ��ͬʱ��ɶ��ڲ��ʳ����м��ȣ���������������ʵ�ѡ���ǣ���������
A����ʯ����ˮ ������B����ʯ����ˮ������ C��ʯ��ʯ��ˮ������ D���Ȼ�����ˮ
12���������к����ḻ�İ�«������ѧʽΪC14H12O3���������п����ԣ������ư�ϸ���������������йذ�«����˵������ȷ���ǡ������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A��������C,H,OԪ����ɵġ� B��������̼���⡢��ԭ�ӹ��ɵĻ����
C��������������������� D����«���У�̼���⡢������Ԫ�ص�������Ϊ14��12��3
13���ڡ����ܷ���������X��Y��M��N�������ʣ��ڡ��������·�Ӧ����ʱ���÷�Ӧǰ������ʵ��������£�
| ���� | X | Y | M | N |
| ��Ӧǰ����(g) | 10 | 10 | 10 | 10 |
| ��Ӧ������(g) | 10 | 15 | 8 | 7 |
���ƶϸ��ܱ������з�����ѧ��Ӧ�Ļ��������ǡ������������������������������������������������������������������������������������������� .(����)��
A���ֽⷴӦ��������������B�����Ϸ�Ӧ��������������C��������ԭ��Ӧ���� D����ȷ��
14���ڵ�10��Ļ�ѧ��Ӧ�У�X�����п����Ǹ÷�Ӧ�еġ��������������������������������������������������������������������������� (���� )
A���������������� B����ԭ���������� C�������������� D��������
15��ijЩ��˯������ĥ������Ϊȱп������ġ�п����ָ������������������������������������������������������������������������������ (���� )
A�����ӡ������� �¡�ԭ�ӡ����������� �á�Ԫ�ء������� �ġ�����
16��ij��ũҵ�Ƽ��������ڽ��С������ũҵ����Ӱ�켰��Բߵ��о����У��ó������pH��С��С��������ȹ�ϵ��һ���������±���ʾ�����������жϣ�����˵����ȷ���ǣ���������
| �����pH | 3��58 | 4��59 | 4��86 |
| �������%�� | 10 | 5 | 3 |
A�� �����pHԽ��С���������Խ��B�������pHԽС��С���������Խ��
C�� ���������Խǿ��С���������ԽС�� D�����������Խ����С���������Խ��
17�������к������������ǡ����������������������������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A��N2������������ B��O2�������������� C��CO2 ������������D��He
18��Ҫʹ20��ʱ����صIJ�������Һ��ɱ�����Һ�����д�ʩ����ʵ�ֵ��ǡ� ���� (���� )
A�������¶ȡ����� B����������ء�������C����������ˮ������D�������¶�
19�� ���д�������У�ͨ��ʹȡ�õ������õ�����ƫС���ǡ����������������������������������������������������� (���� )
A������Ͳȡ10mLˮ�����ø��ӷ���ȡ�õ���
B������Ͳ�ⶨҺ����������ø��ӷ�����õ�����
C��������������̣���ʹ�����룬�����������ʵ���������õ���������
D����pH��ֽ��ˮ��ʪ��ⶨij���������
20�� ���������š��ijɹ���������գ������ҹ������˺��켼���Ѿ�����ͻ���Խ�չ���ڷɴ��Ļ���ƽ����г�װ��Һ̬�£���X��ʾ����Һ̬˫��ˮ��H2O2�������ǻ��ʱ�ķ�Ӧ����ʽΪ��2H2O2+X=N2+4H2O�����£�X���Ļ�ѧʽΪ (���� )
A��N2H6������������������������������������ B��N2H4�������������������������������������������� C��NH2���������������������������������������������� D��N2H4O2
21�����г��ӵķ���������ǡ����������������������������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A����ȥCO��������CO2��ͨ����������ʯ��ˮ B����ȥCO2��������CO����ȼ������塡
C����ȥ����ع����е�����ʳ�Σ����½ᾧ���� D����ȥ�Ȼ����л��еĶ������̣����˷�
22������ʵ�������ʵ���������������ȷ���ǡ��������������������������������������������������������������������������������������������������������� (�� ��)
A����ȴ�ȵ�����ͭ������Һ��������ɫ����ͭ����
B����������ݳ�ȥʢʯ��ˮ������ƿ�ڵİ�ɫ����
C�����ڿ�����ȼ�ղ�������ɫ����
D����ѧʵ�����ֱ�Ũ�������ˣ����ô���ˮ��ϴ����Ϳ̼��������Һ
23���мס��ҡ���������ƿ��ɫ���壬��֪�����������������������Ͷ�����̼��Ϊ��
�������ǣ����з����������ǡ��������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A���۲���ɫ���������������������� �������� B���ֱ�������ʯ��ˮ
C����ȼ�ŵ�ľ���ֱ�������ƿ���塡�������� D���ֱ����һֻС����
24��ʵ������ȡ���ռ�������̼ʱ��Ҫ�õ������������ǡ����������������������������������������������������������������������������� (���� )
A������©��������ƿ��ˮ�ۡ��������������� B�� ����ƿ����Ͳ��ˮ�ۡ�
C���ƾ��ơ����ƿ������ƿ���������������� D�� ����ƿ����ƿ������Ƥ���ĵ���
25������������ʹ��ɫʯ�����ɫ���ǡ������������������������������������������������������������������������������������������������������������������������������������� (���� )
��̼������Һ �ڰ״ס���ѩ����ˮ ��������ʯ�ҷ���ˮ�� ������ˮ ��ʳ��ˮ �߰�ˮ
A���ڢۢޢߡ��������� B���٢ܢޡ������� C���ۢܢޢߡ������� D���٢ܢ�
26������������ʵ���ٶ���������ڰ�����ȼ����ʳ�︯�ã��ܻ�ҩ��ը�����ǵĹ�ͬ����
A��������ͷ��� B�������ڻ���������Ӧ��C����������ը�� D��������������Ӧ
27��Ũ��Һ����ˮϡ�͵Ĺ�����, ���ֲ�������ǡ��������������������������������������������������������������������������������������������������� (���� )
A����Һ��Ũ�ȡ�B���ܼ��������������� C����Һ������ ��D�����ʵ�����
28����������������Σ�յ��ǡ����������������������������������������������������������������������������������������������������������������������������������������������������������� (���� )
A����ʯ�ҽ�Ĩǽ������������������ B���øɱ�������̨�ϵ�����Ч��
C���û������Ȼ���Ƿ�й©������ D����������Ͱײ˵ĵؽ�ǰ���Ƚ��еƻ�ʵ��
29�����������к�ˮ�����������ǡ��������������������������������������������������������������������������������������������������������������������������������������������� (���� )��
A��6.02��1024��ˮ���� �� B��1 mol��ˮ���� C��36gH2O ������D��20 mL��ˮ
��������� (ÿ��1��,�� 26��)
30����C��O2��H2��CO��CH4���������У������ƽ�������յĸ�������Ⱦ��ȼ�������������� ����ʹ�����ǵ�ľ����ȼ�����������������п�ȼ�����л�ԭ�Ե���̬���������� ___���� ������л������������� �����ڳ��������ʽ��ȶ�����������̼��īˮ����_________��
31���ڵؿ��к������Ľ���Ԫ�غͷǽ���Ԫ����ɵĻ�����Ļ�ѧʽ��____�� ____��
32�����й���������ͬ�����������ͼ�Ĺ��������ڽ�����ɡ�C9H3O7N7P����ɻ������ʵ�һ���֣�����________��Ԫ����ɣ�ÿ�������й���������������ԭ�ӣ�̼��Ԫ�ص�ԭ�Ӹ�����Ϊ�������� ��0.5Ħ��C9H3O7N7P������������ԭ��Ϊ���������� mol��
33�� ��ͼ��a��b�������ʵ��ܽ�����ߡ�
��1��t1��ʱb�ı�����Һ100 g������������40 gˮ����Һ������������__________��
��2��t2��ʱa����30 g����80 gˮ�г���ܽ���Һǡ�ñ��ͣ�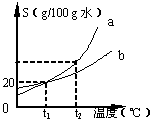 ��t2��ʱa���ʵ��ܽ����______________g/100 gˮ��
��t2��ʱa���ʵ��ܽ����______________g/100 gˮ��
��3����t1��ʱ�ĵ�������a��,b�ı�����Һ�ֱ����µ�t2�棬��ʱ������Һ����������������ϵΪ��a��Һ������������_______b��Һ������������������ڡ�����С�ڡ����ڡ���
��4��t1��ʱ����30��b���ʷ���100��ˮ�г���ܽ⣬�ɵõ���
��Һ__�� ___�ˣ���������������Ϊ_������____��
34��Ŀǰ�״���CH3OH����Ϊһ������ȼ�����ܵ��㷺���ӣ��״�ȼ�տ�������ˮ�Ͷ�����̼��������κλ�����Ⱦ����δ�����������ȼ�ϡ�
��1����д���״�ȼ�յĻ�ѧ����ʽ_____________________________________ ��
��2��1mol�״����ȼ�����ĵ����������ʵ�����___�� __mol��
|
|
|
|
![]()
![]()
![]()
![]() ������ A������������
B������������
C����������������
B��������������
������ D
������ A������������
B������������
C����������������
B��������������
������ D
��1����������һϵ�б仯�ƶ�ABCD�Ļ�ѧʽ��
������ A______________��B______________��C______________��D______________��
��2��д���仯�۵Ļ�ѧ����ʽ��_______________________________________________��
��3���仯����������������_____________���ܵķ�Ӧ����ʽΪ________________________��
| ��Ҫԭ�ϣ�̼��� ʳ�÷�����ÿ��1�Σ�ÿ��1Ƭ����ʳ�� |
36��ij����ʳƷ���װ��ǩ�ϵIJ�����������ͼ��
��1������θҺ�к��м�ϡ����������������������ʳ���Ϊ�����Ӫ����������Һ�в��ܺܺõر����������ա�Ŀǰ�������ϳ��۵IJ��Ƽ��д���������ˮ������̼��Ʒ�ĩ�����û�ѧ����
��ʽ������Ϊ���ܱ����塰�����������գ�_________________________________________��
��2��ʳ�÷����С���ʳ�������ڸƵ����գ���ʳ�����þ���____________________________��
�ġ�ʵ���⣨��28�֣�
37���������ֻ�ѧ��������������ɫ��Һ�壺����ˮ�ʹ���
| �١����� | �֡� �� | �ᡡ �� |
38�����Ȼ��ƹ�������100����������Ϊ10%��ʳ����Һ��
�š���ȷ��ʵ�鲽���ǣ�������ظ�ѡ��__________________________________
�ٳ������ڹ��ˡ����ܽ⡡���������ݼ���
���õ��IJ�����������������������������������������������
����ѡ�õ���Ͳ�Ĺ��ӦΪ������ĸ������������
A��10mL������B��50mL������C��100mL������ D��250mL
(4)�ֽ�50�����ƺõ�10����ʳ����Һ��ϡ�ͳ�5�����Ȼ�����Һ�����ˮ__________�ˡ�
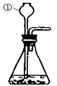
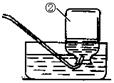
 39������������ʾʵ��װ�ã��ش��й����⡣
39������������ʾʵ��װ�ã��ش��й����⡣
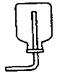 |
������ A������������������ B������������������ C�������������� D
��1���������ƣ������������� ���������������� ����
��2��������غͶ���������ȡ���ռ�����������װ���ǣ�����ĸ�� ����������
��ѧ����ʽ��ʾΪ�������������������������������������� ��
��3��ʵ�����������IJ�������һ��ɷ�Ϊ���ٵ�ȼ�ƾ��ƣ������Թܣ��ڼ��װ�������ԣ��۽�����غͶ������̻����װ���Թܣ��ô����ܵ���Ƥ�������Թܣ����̶�������̨�ϣ��� ����ˮ���ռ���������Ϩ��ƾ��ƣ������ܴ�ˮ����ȡ����
����ȷ�IJ���˳����______________________________________��
��4���ռ�������������_______________________���������ַ����ռ�����ʱ�����������Ƿ����ķ�����_____________________________________________________________��
��5������ȡ������������ʵ�顣
| ʵ���� | ���� | ��������Ļ�ѧ����ʽ |
|
| ����ʯ��ˮ ����� | �������������������������� |
|
| ��ɫ��ˮ����ͭ����ɫ | �������������������������� |
| �ƶϣ�����������ʵ��֤������������һ������������������ Ԫ�ء� | ||
40��Ϊ���о��ӳ���ʹ�õ���ˮƿ�е�����Ƭ״���壨ˮ�����ijɷ֣�С�ս�������̽����
| �١��� �� | �֡� �� | ���ۻ����� | |
| ʵ �� �� |
| ˮ����ס������� | |
| ����ʯ��ˮ����� | ���ۣ� ˮ���ֽ���������������� ��д��ѧʽ�� | ||
| ʵ �� �� | ���岿���ܽ⣬���PHԼΪ12 | ����������Һ��ʹ��ɫ��̪�Լ���______ɫ�� |
��
��������̽�������ƴ�ˮ���ijɷ��к����������������������� ��д�������ƣ���
��д��ʵ�����ˮ���ֽ��ʵ����з�����Ӧ�Ļ�ѧ����ʽ��
���� ������������������������������������������������������������������������ ��
�ֶ�����2005ѧ��ȵ�һѧ����ĩ�������
������ѧ �ο��𰸺�������� ���Ե�ѧУ�½̲ģ� 06.01
1. �������ơ��������ƺ��������д������������֣����÷֡�
2����ѧ����ʽ�л�ѧʽд�����÷֣���ͷ����ƽ����Ӧ������ȱ©������ÿ�����ܿ�1�֡�
3. �����к����𰸾��ο�����Ҫ����֡�
һ����� ��ÿ��1�֣���20�֣�
1��������Ӧ���������ƺͻ�ѧʽ��
| �������� | �������� | ʯ�� | ʳ �� | ||||
| ��ѧʽ | SiO2 | He | H2CO3 | CaO |
2�����뻯ѧ���Ż�ѧ���ű�ʾ�����壺
| ��ѧ���� | 2O |
| 3Fe2O3 | ||
| ��ʾ������ | ˮ��һ��ˮ���� | ��2�۵�þԪ�� | һ������� |
3��д�����л�ѧ����ʽ��������й����ݣ�
| ��ѧ��Ӧ | ��ѧ����ʽ | ���� |
| ��˿��������ȼ�� |
3Fe+2O2�������� Fe3O4 | ����ȼ�գ��������䣬���ȣ�������ɫ���� |
| ���ˮ |
2H2O �������� 2H2��+ O2�� | 1:2 |
| þ���ڶ�����̼��ȼ�� |
2 Mg+CO2�������� 2 MgO+C | 48��44��Ҳ�ɻ���Ϊ12��11�� |
| ˫��ˮ�ֽ� |
2H2O2�������� 2H2O������O2 �� | ��ɫ |
����ѡ���⣨ÿ��1�֣���26�֣�
| ��� | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| �� | D | A | C | A | C | C | A | B | A | B | C | C | B |
| ��� | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| �� | A | A | A | B | B | D | C | D | D | D | D | C | A |
��������� (ÿ��1��,����� 26��)
30��H2 ��O2��CO��CH4��C�� ������ 31��Al2O3
32��5��27��9��3����3��1����1.5mol
33����1��16.7������2��37.5����3������ ��4��120��16.7����
![]() 34��
34��
��1��2CH3OH��+ 3O2���������� 2CO2���� 4H2O�������ȡ���
![]() ��2��1��5
��2��1��5
35����1��A��O2��B��CO2�� C��CO�� D��H2CO3 ��2��CO+CuO���������� Cu+ CO2�� ����
��3����죻������������������������ ��4��H2O��CO 2������H2CO3
36����1��CaCO3+2HCl������ CaCl2+H2O+ CO2 ��
��2������Ӧ��ĽӴ�������ٽ��Ƶ����գ�
�ġ�ʵ���⣨��28�֣�
37��
| �١����� | �֡� �� | �ᡡ �� |
| ��1�֣��ֱ�ȡ�����Թ��У��μ���ɫʯ���Լ� | ��1�֣�һֻ��죬һֻ���������� | ��1�֣������Ǵ��ᣬ�����������ˮ |
| ��1�֣��ֱ�ȡ�����Թ��У��������ʯ | ��1�֣�һֻ�Թ��еĴ���ʯ����ð���ݣ�һֻ���������� | ��1�֣�ð���ݵ��Ǵ��ᣬ�ޱ仯��������ˮ |
�����������ֱ�ⶨ����Һ���pH��pH����7��Һ��������ˮ��pHС��7��Һ���Ǵ���
38���š��ݢ٢ۡ�1�� �����ձ� ������ ©�� ��Ͳ�� 2�� �ǡ�C����1��(4)50��1��
39����1���ٳ���©�������ڼ���ƿ������2��A C��2�� 2KClO3������ 2KCl+3O2 �� ��1��
��3���ڢۢ٢ܢޢ� ��2��������4�� �����ſ�����1�������������ǵ�ľ�����ڼ���ƿ�ڣ���ȼ���������Ѿ�������1��
��5��CO2 + Ca(OH)2������CaCO3�� + H2O�� 1���� CuSO4+5H2O ����CuSO4 ��5H2O�� 1��
������һ������̼����Ԫ��1��
![]() 40������5����CO2�� �죻 ̼��ƣ�
40������5����CO2�� �죻 ̼��ƣ�
CaCO3�� ��������CaO+CO2���������� CaO+ H2O�� Ca(OH)2 ��������