晋江市05-06年度秋化学科期末考试卷
(满分:100分,考试时间:90分钟)
相对分子质量:H-1 C-12 O-16 Ca-40 Cl-35.5
| 题号 | 一 | 二 | 三 | 四 | 总分 |
| 得分 |
|
|
|
|
|
一、选择题:(每小题只有一个正确选项,请把正确选项的标号填在下表相应题号的空格内,本题共30分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 |
1、绿色化学又称环境友好化学,下列不属于它的特点的是
A、产品的颜色是否绿色 B、原料是无毒无害的
C、反应条件是无毒无害的 D、原料的原子都被产品所消耗,做到“零排放”
2、下列广告用语使用不当的是
A、珍惜水资源,不然看到的最后一滴水就是你自己的眼泪
B、爱护水资源,请使用无磷洗衣粉
C、保护臭氧层,请使用无“氟”冰箱
D、吸有过滤嘴的香烟,不会对人体造成危害
3、1969年7月20日,美国宇航员阿姆斯特郎第一个登上月球,在月球上,他发现没有空气和水,那么他在月球上可能完成的实验活动是
![]() A、点燃蜡烛 B、土壤取样分析
C、种植花草 D、放养动物
A、点燃蜡烛 B、土壤取样分析
C、种植花草 D、放养动物
4、过氧乙酸可以起到消毒作用,其分子结构如下图(注: 表示碳原子

![]() 表示氧原子 表示氢原子)下列有关过氧乙酸的叙述中不正确是
表示氧原子 表示氢原子)下列有关过氧乙酸的叙述中不正确是
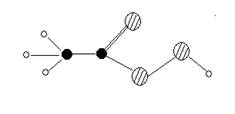 A过氧乙酸的化学式是C2H4O3
A过氧乙酸的化学式是C2H4O3
B、其相对分子质量为76
C、C、H、O三种元素的质量比为2:4:3
D、完全燃烧生成CO2和H2O
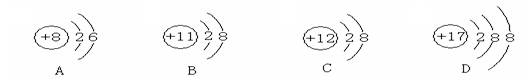 5、下列粒子在人体中起着重要的作用,其中属于原子的是
5、下列粒子在人体中起着重要的作用,其中属于原子的是
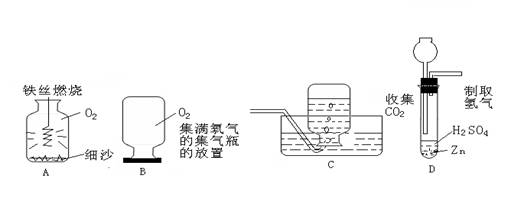
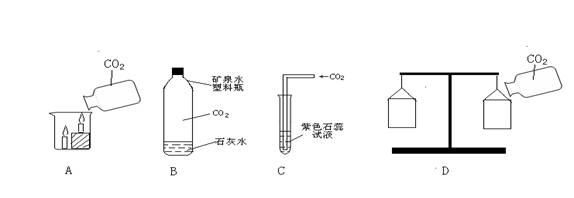 6、在进行二氧化碳的性质研究中,设计了如下四个实验装置,其中只能证明二氧化碳物理性质的实验是
6、在进行二氧化碳的性质研究中,设计了如下四个实验装置,其中只能证明二氧化碳物理性质的实验是
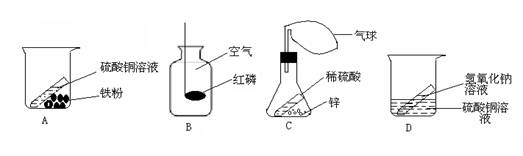 7、在探索质量守恒定律实验中,设计了如下图的实验装置,其中反应前后容器中物质的总质量不相等的是
7、在探索质量守恒定律实验中,设计了如下图的实验装置,其中反应前后容器中物质的总质量不相等的是
8、下列是空气与人呼出的气体成分的差异研究做法或想法中,正确的是
A、呼出的气体中水蒸气比较少
B、取用石灰水时,实验设计中未说明用量时,只取了约1.5毫升
C、人呼出的气体只有二氧化碳存在
D、人呼出的气体中有一氧化碳存在
9、某同学为探究分子的性质特征,设计如下四个实验,其中能说明分子在不断运动的是
A、吸有相同体积空气和水的注射器,前者比后者容易被压缩
B、铁丝在氧气中燃烧后,生成的黑色固体不会被磁铁吸引
C、局部碰瘪的乒乓球放入热水中凹下部分会重新鼓起
D、打开香水瓶盖,整个房间很快充满香味
10、天然气是一种清洁能源,我市正在建设的一大工程是使用天然气作燃烧,使用天然气对提高人的生活质量有以下好处,你认为其中不宜宣传的是
A、天然气无毒,泄露不具有危险性
B、可以有效减少空气污染,提高空气质量
C、可以大大减轻水陆运输压力
D、可以控制温室气体的排放,减少温室效应
11、下列不能证明水是由氢元素和氧元素组成的是
A、电解水生成氢气和氧气
B、氢气在氧气燃烧只生成水
C、利用太阳能将水分解成氢气和氧气
D、植物在光合作用时,吸收水和二氧化碳转化成淀粉和氧气
12、下列物质与有关性质的对应关系错误的是
A、青铜----人类最早利用的合金
B、不锈钢----永不生锈的钢铁
C、铁----会生锈
D、硬铝----质轻、强度高
13、一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的,
并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是
A、浓硫酸与水 B、氯化钠与水
 C、熟石灰与水
D、生石灰与水
C、熟石灰与水
D、生石灰与水
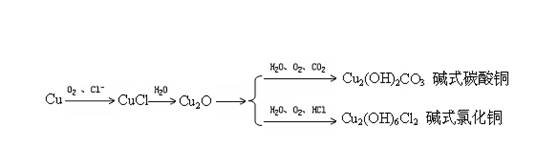
14、埋藏在地下的青铜器锈蚀过程可以表示为:
根据以上青铜器锈蚀过程,青铜器出土后防止青铜器锈蚀的关键是
A、与H2O隔绝 B、与O2隔绝
 C、与H2O、O2和CO2或HCl隔绝 D、保持铜器表面清洁
C、与H2O、O2和CO2或HCl隔绝 D、保持铜器表面清洁
15、下列实验操作正确的是
二、填空题:(共27分)
16、(1)(共3分)在日常生活中,用于制导线的紫红色的金属是 ;家用热水瓶内胆壁的银白色的金属是 ;体温计中填充的金属是 ;
(2)(共4分)用化学式填写出相应物质:大量排放会导致温室效应的气体是 ;一种化合物 ;一种常见的酸 ;“西气东输”的气体是 。
17、(共6分)2005年10月12日我国第二艘载人宇宙飞船“神舟六号”发射获得圆满成功。发射飞船的火箭使用的燃料是偏二甲肼[化学式为C2H8N2],试回答:
①偏二甲肼由 种元素组成,一个偏二甲肼分子中含有 个原子,组成的三种元素C:H:N的质量比为 ;偏二甲肼中氮元素的质量分数 。
②偏二甲肼在助氧剂N2O4中燃烧生成二氧化碳、水和一种空气中含量最多的气体。写出其反应的化学方程式 。
18、(共4分)目前正在利用和正在开发的部分能源有:煤、石油、天然气、太阳能、风能、潮汐能、氢气、“可燃冰”等。回答下列问题:
①属于不可再生的能源的是 ;
②我国“西气东输”工程输送的能源物质是 ;
③埋藏于海底,目前开采在技术上还存在很大困难的能源物质是 ;
④通过非化学反应产生的能源是 。
 三、19、(共7分)某化学兴趣小组在进行某种加碘、加钙盐成分的研究中,收集到包装标签上的文字如右下图所示,买来一包,请你与他一起完成以下研究:
三、19、(共7分)某化学兴趣小组在进行某种加碘、加钙盐成分的研究中,收集到包装标签上的文字如右下图所示,买来一包,请你与他一起完成以下研究:
①此包物质属于 ;
(“纯净物”或“混合物” )
②包装标签上碘含量是指 ;
(填“单质碘”或“碘酸钾”或“碘元素” )
③碘酸钾的化学式是KIO3,其中K为+1价,
O为-2价,则KIO3中I的化合价是 ;
④为了检验该盐中是否含有碳酸钙,在 家庭
厨 房里可选 用的物 质是 ;
写出检验过程的有关操作、现象和结论:
。
20、(共3分)用“<”或“>”或“=”填写空格:
①把50毫升酒精注入50毫升蒸馏水中,注入前总液体的体积 注入摇匀后液体的体积;
②加热碱式硫酸铜后,剩余固体的质量 原碱式硫酸铜的质量;
③在原子中,质子数 核外电子数。
四、实验题(共19分)
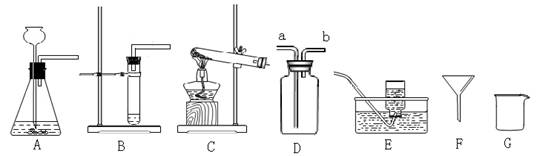 21、根据下图回答:(装置图用序号填写)
21、根据下图回答:(装置图用序号填写)
⑴指出仪器名称:F ;G ;
⑵指出仪器G的用途(填写一种用途): ;
⑶实验室制取CO2时可选用的发生装置是 ;若用D装置收集CO2,则CO2应从导管口 通入。
⑷实验室用KMnO4制取O2时应选用的发生装置是 ;可选用的收集装置是 ;你选用收集装置的根据是 ;
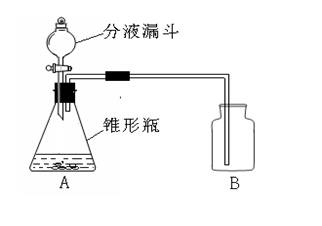 ⑸实验室用过氧化氢溶液和二氧化锰混合制取氧气,分液漏斗可以通过调节活塞控制液体的滴加速度,回答下列问题:
⑸实验室用过氧化氢溶液和二氧化锰混合制取氧气,分液漏斗可以通过调节活塞控制液体的滴加速度,回答下列问题:
①利用此装置制取氧气时,在锥形瓶中
应放入的物质是 ,
从分液漏斗加入的物质是 ;
②在此反应中二氧化锰是 剂;
③若锥形瓶中反应很剧烈,据此提出实验
安全注意事项是
A、控制液体滴加速度 B、用体积较小的锥形瓶 C、加热反应物
④某同学在观察到锥形瓶内有大量气泡时,开始收集氧气,过一段时间后,用带有火星的木条伸入集气瓶口、瓶中、瓶底,都未见木条复燃。可能的原因是
。
⑤写出锥形瓶中发生反应的化学方程式: 。
22、(共8分)某同学晚上帮助妈妈做饭,切完青菜就将菜刀放砧板上,第二天早晨发现菜刀生锈了,请问:
①这一变化属于 变化(填“化学”或“物理” );
②菜刀为什么会生锈? ;
③为了防止这把菜刀生锈,该同学应该怎么做? ;
④湿法冶金的原理其中之一是铁与可溶性铜盐溶液反应制得单质铜。其有反应的方程式是 ;
属于 反应(填“化合”或“分解”或“置换” )。
![]() 23、(共6分)当电力充裕时,氢能源的开发可用电解水的方法,电解水过程中正极产生的气体是
;负极产生的气体是
;当正极产生的气体是2ml时负极产生的气体是
ml;电解水的方程式可表示为
23、(共6分)当电力充裕时,氢能源的开发可用电解水的方法,电解水过程中正极产生的气体是
;负极产生的气体是
;当正极产生的气体是2ml时负极产生的气体是
ml;电解水的方程式可表示为
2H2O X H2↑+ O2↑,则X的值是 。
五、计算题:
24、(共10分)桂林山水甲天下,那里里溶洞中的千姿百态的石笋、石柱主要成分是碳酸钙。某兴趣小组为了测定石笋的纯度,取25克石笋放入盛有85克稀盐酸中,待石笋完全反应后,(杂质不与盐酸反应)。烧杯中混合物的质量为101.2克,求该石笋中碳酸钙的质量。
分析:由于题目中出现的3个数据都是混合物的质量不能直接代入方程式计算。则可根据 定律,求出生成二氧化碳的质量为 ,再把生成的二氧化碳的质量代入有关反应方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑进行有关计算。则计算过程为:(请同学们帮他完成)
晋江市05-06年度秋化学科期末考试卷参考答案
(满分:100分,考试时间:90分钟)
相对分子质量:H-1 C-12 O-16 Ca-40 Cl-35.5
一、选择题:(每小题只有一个正确选项,请把正确选项的标号填在下表相应题号的空格内,本题共30分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 | A | D | B | C | A | D | B | B | D | A | D | B | D | C | A |
二、填空题:
16、(1)铜;银;汞(化学式也得分)(每空1分)
(2)CO2;H2O;HCl;CH4 (每空1分)
17、①三;12;6:2:7;46.7% (每空1分)
![]()
②C2H8N2+2N2O4 2CO2↑+4H2O+3N2↑ (每空1分)
18、①煤、石油、天然气、可燃冰(任写一种即可)(每空1分)
②天然气(每空1分)
③可燃冰(每空1分)
④潮汐能(每空1分)
19、①混合物(1分)
②碘元素(1分)
③+5(1分)
④醋(1分);取少量样品于试管中加入适量的醋,有气泡冒出说明含有碳酸钙,反之则没有(3分)
20、①> ②< ③= (每空1分)
21、⑴漏斗;烧杯(每空1分)
⑵加热液体等(1分)
⑶A;a(每空1分)
⑷C;E或D;氧气不易溶于水(每空1分)
⑸①双氧水(1分);二氧化锰;(1分)
②催化剂(2分)
③A(2分)
④装置漏气等(2分)
⑤2H2O2 2H2O+O2↑(2分)
22、①化学(1分)
②菜刀上有水、与氧气接触能生锈(2分)
③把菜刀洗净擦干,放在干燥处,涂上食用油(2分)
④Fe+CuSO4=FeSO4+Cu(2分);置换(1分)
23、氧气(1分);氢气(1分);4(2分);2(2分)
24、解:质量守恒(2分);8.8克(2分)
设:石笋中碳酸钙的质量为X ( 计算共6分 )
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 8.8g
100:44=X:8.8g
X=20g
答:石笋中碳酸钙的质量为20克.