初三综合练习
A卷
班级_____ 姓名_____ 得分_____ 等第_____
一、选择题(每小题2分,共40分;每小题只有1个选项符合题意)
1.下列化合物中含有+5价元素的是 ( )
A.KMnO4 B.K2CO3 1.C
C.KClO3 D.K2SO4
2.铝在氧气中燃烧生成氧化铝,铝、氧气、氧化铝的质量比是 ( )
A.27∶32∶102 B.27∶24∶43 2.D
C.4∶3∶2 D.9∶8∶17
3.在10℃时,某物质的溶解度为5克,在此温度下该物质饱和溶液里,下列相互之间的质量比例关系正确的是 ( )
A.溶液︰溶质=21︰1 B.溶剂︰溶质=19︰1 3.A
C.溶液︰溶剂=20︰21 D.溶质︰溶液=1︰20
4.在“5H2O”中,水的式量是 ( )
A.160 B.90 4.D
C.26 D.18
5.60℃时KNO3的溶解度为110克,在此温度下,将饱和KNO3溶液42克蒸干,可得到KNO3晶体的质量是 ( )
A.2.75克 B.5.5克 5.D
C.11克 D.22克
6.某化合物x的溶解度在80℃时为40克,在同样温度下,100克饱和溶液中,溶质x的含量是 ( )
A.40克 B.40/7克 6.D
C.100/7克 D.200/7克
7.40℃时,把2克固体物质溶解在10克水中变成饱和溶液,该物质在20℃时的溶解度是 ( )
A.2克 B.20克 7.B
C.12克 D.无法计算
8.在①钾盐 ②铵盐 ③硝酸盐 ④硫酸盐 ⑤盐酸盐 ⑥碳酸盐中,均能溶于水的一组盐是 ( )
A.①②⑤ B.②③④ 8.C
C.①②③ D.①③⑥
9.含下列离子的溶液中,溶质全部为碱的是 ( )
A.Na+、OH-、NO3- B.H+、Cl-、SO42- 9.C
C.K+、Ca2+、OH- D.Na+、Mg2+、SO42-
10.下列化学反应方程式书写错误或不符合事实的是 ( )
A.Fe+H2SO4====FeSO4+H2↑ 10.D
B.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C.CaCO3+2HCl===CaCl2+H2O+CO2↑
D.CuO+H2O===Cu(OH)2
11.nH2O与mH2SO4的质量比是 ( )
A.9n∶49m B.n∶m 11.A
C.17n∶96m D.(2n+16)∶(2m+96)
12.硫酸钾中钾元素、硫元素、氧元素的质量比是 ( )
A.78∶32∶32 B.2∶1∶4 12.D
C.39∶32∶16 D.39∶16∶32
13.含3.5克的氮元素,所需硝酸铵(NH4NO3)的质量是 ( )
A.5克 B.8克 C.10克 D.20克 13.C
14.某石灰石样品,经分析含CaCO3 90%,则样品中钙的质量分数为 ( )
A.40% B.36% C.80% D.90% 14.B
15.跟40克SO3所含氧元素质量相等的CuO的质量是 ( )
A.40克 B.80克 C.120克 D.160克 15.C
16.将鸡蛋壳浸入稀盐酸中,有气泡产生,这是因为鸡蛋壳中含有 ( )
A.硫酸根 B.碳酸根 C.氢氧根 D.硝酸根 16. B
17.下列叙述中,不正确的是 ( )
A.硫在氧气中燃烧,发出蓝紫色火焰 17.B
B.检验集气瓶中是否已集满二氧化碳气体,可将一根燃着的木条插入瓶内,看木条是否熄灭
C.水在直流电的作用下,可以分解成氢气和氧气
D.煤、石油、天然气是当今世界上最重要的三大矿物燃料
18.实验室制取氧气,并用排水法收集。下列操作正确的是 ( )
A.装置连接好后,即装入药品加热 18.D
B.加热药品,导管口刚冒出气泡,立即收集氧气
C.收集满氧气的集气瓶,取出倒放在桌上
D.实验完毕后,先把导管移出水面,再熄灭酒精灯火焰
19.区别H2、O2、CO2三种气体最简便的方法是 ( )
A.将气体分别通入石灰水中 19.B
B.用燃着的木条分别伸入盛有三种气体的集气瓶里
C.将气体分别通过灼热的氧化铜
D.将气体分别通过红热的铜丝
20.下列各组物质中,两种物质混和后,溶液质量不会发生变化的是 ( )
A.氢氧化钠溶液和盐酸 B.氯化钠溶液和硝酸银溶液 20.A
C.碳酸钠溶液和盐酸 D.硝酸钡溶液和稀硫酸
二、选择题(每小题2分,共10分;每小题有1~2个选项符合题意。若正确答案只包括一个选项,多选时该题为0分;若正确答案包括两个选项,只选一个且正确的给一分,选两个且都正确的给2分,但只要选错一个,该小题就为0分)
21.对下列实验过程的评价,正确的是 ( )
A.某固体中加入稀盐酸,产生了无色气体,证明该固体一定含CO32- 21.C
B.某溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀,该溶液中一定含SO42-
C.无色溶液滴入酚酞试液显红色,该溶液不一定是碱溶液
D.验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl-
22.新买的铝锅、铝壶用来烧开水时,凡是水浸到的地方都会变黑,说明水中
溶有 ( )
A.钾盐 B.钠盐 C.钙盐 D.铁盐 22.D
23.下列关于溶液的说法,正确的是 ( )
A.饱和石灰水一定是浓溶液 B.无色的液体一定是溶液 23.C
C.溶液一定是均一、稳定的 D.溶液一定是固体溶于水形成的
24.某电镀厂排出的酸性污水中,含有有毒的Cu2+,欲除去Cu2+,并降低其酸性,加入适量下列物质不能达到目的的是 ( )
A.碳酸钠 B、生石灰 C.氯化铁 D.铁粉 24.C
25.某元素的氧化物式量为M1,其硫酸盐的式量为M2,则该元素的化合价可能是下列关系中的 ( )
A.![]() B.
B. ![]() C.
C.![]() D.
D.![]()
25.AC
三、填充题(共16分)
26.(9分)为了证实下列实验结论,请选用下列各相应的实验方法及实验现象,用各对应的符号(A、B、C……a、b、c……)填入括号内
实验结论:
(1)某黑色粉末是氧化铜 ( ) (2)某无色溶液是氯化钡 ( )
(3)某无色液体是稀盐酸 ( ) (4)集气瓶甲中是一氧化碳 ( )
(5)集气瓶乙中是氧气 ( ) (6)集气瓶丙中是二氧化碳 ( )
实验方法:
A.把纯净的一氧化碳通入灼热的某黑色粉末,并把尾气通入澄清的石灰水
B.把带有火星的木条伸入贮有某气体的集气瓶
C.将燃烧的木条伸入贮有气体的集气瓶
D.向液体中加锌粒;反应后再滴入硝酸银溶液,并滴加稀硝酸
E.取出少量加硫酸钠和稀硝酸;另取少量加硝酸银和稀硝酸
实验现象:
a.带有火星的木条立即燃烧起来
b.瓶内气体燃烧,呈蓝色火焰;倒入石灰水振荡后出白色浑浊
c.木条熄灭,倒入的石灰水呈白色浑浊
d.黑色粉末逐渐变亮呈红色;尾气能使石灰水变浑浊
e.有气泡生成;有白色沉淀生成且不溶于稀硝酸
f.均有不溶于稀硝酸的白色沉淀生成
26 ⑴A;d ⑵E;f ⑶D;e ⑷C;b ⑸B;a ⑹C;c
27.(3分)50℃时,将不饱和的氯化铵溶液50克,分成两等份。一份蒸发掉5克水,另一份加入2.5克氯化铵,都恰好饱和。则50℃时,氯化铵的溶解度为____________克。
27 50
28.(4分)电解水时,插入正极的玻璃管汇集的气体是__________,插入负极的玻璃管汇集的气体是_______________,两种气体的体积比前者与后者约_____________。该反应的化学方程式是______________________________________________。
28 O2; H2;
1︰2; 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
四、简答题(共8分)
29.(4分)完成下列化学方程式:
(1) Fe+( )──Cu+( )
(2) FeCl3+( )──NaCl+( )
(3) AgNO3+( )──( )+NaNO3
(4) NaOH+( )──Cu(OH)2↓+( )
29.⑴ CuSO4+Fe===FeSO4+Cu;⑵FeCl3+3NaOH=== 3NaCl+Fe(OH)3↓;⑶AgNO3+NaCl=== NaNO3+AgCl↓;⑷CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
30.(4分)判断下列说法是否正确,正确的在括号内打“√”,错误的打“×”。
①凡含氧元素的化合物都是氧化物。 ( )
②凡升高温度,均可使饱和溶液变成不饱和溶液。 ( )
③溶液和浊液都是混和物,它们本质的区别在于溶液是无色透明的。( )
④将1克蓝矾溶解在99克水中,就能配制成1%的硫酸铜溶液。 ( )
30.①×②×③×④×
五、实验题(共14分)
31.(4分)下表的图中各有一处错误,请在表中写出错误所在:
 |
31. 不能用向下排空气法收集二氧化碳; 漏斗下端管口要紧靠烧杯内壁
32.(10分)为了制取纯净干燥CO2气体,并验证碳、一氧化碳等物质的化学性质,设计了如下实验装置。试根据装置图,回答下列问题:
(1)指出图中选用药品的错误:①_____________________、②___________________。
(2)把错误改正后,指出在实验过程中,下列几处所见到的现象:
A处:______________________、E处:___________________、F处:_________________。
(3)指出下列几处装置的作用:
B处:___________________、C处:___________________、F处:_____________________。
(4)写出下列几处发生化学反应的方程式:
D处:_____________________________、E处:_________________________________。
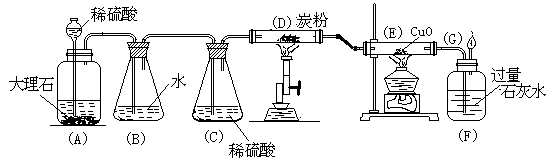
32 ⑴ ①与大理石反应用稀硫酸是错的 ②装置C中用稀硫酸是错的 ⑵
A:稀盐酸与大理石激烈反应,产生大量气泡,大理石逐渐减少 E:黑色氧化铜变成光亮的红色F:澄清的石灰水变浑浊 ⑶
B:用水除去CO2中可能混有的HCl气体 C:用浓硫酸除去CO2中的水分 F:验证CO与CuO反应的生成物中有CO2 ⑷
D:CO2+C![]() 2CO E:CO+CuO
2CO E:CO+CuO ![]() CO2+Cu
CO2+Cu
六、计算题(共12分)
33.(5分)锌和稀H2SO4总质量为30克,完全反应后质量减少至29.8克,求有多少克的锌发生了反应。
33 6.5克
34.(7分)70℃时,NH4Cl的溶解度是60克。将320克此温度的饱和NH4Cl溶液蒸发掉40克水,仍然保持在70℃,求:
⑴蒸发后溶液的溶质质量分数。
⑵析出晶体的质量。
34. ⑴37.5% ⑵24克