2002/2003初三化学(下)总复习测试卷(一)
化学基本概念和原理
可能用到的相对原子质量:H:1 O:16 S:32 C:12
一、选择题:以下各题,只有一个符合要求的答案(每小题2分,共30分)
1、市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等,这里的“钙”、“锌”、“碘”是指( )
A、分子 B、元素 C、单质 D、阴离子
2、下列现象,不一定发生了化学变化的是( )
①有水滴产生的过程 ②浓硫酸放在空气中质量增加了
③碳酸氢铵露置空气中质量减轻了 ④爆炸
A、①④ B、②③ C、①③ D、③④
3、下列变化中,可以用来证明分子在化学变化中是可分的是( )
A、分离液态空气得到氮气和氧气 B、分解液态水得到氢气和氧气
C、分离KNO3和NaCl,得到KNO3晶体 D、对天然水加热时有气泡冒出
4、已知用碳还原烘干的铬酸钠可制得氧化铬4Na2CrO4+4C+O2==4Na2CO3+2Cr2O3,在这反应前后的两种含铬的化合物中,铬的化合价依次是( )
A、7、3 B、6、3 C、6、5 D、5、6
5、下列各组物质中,在物质分类里前者从属于后者的是( )
A、纯净物、混合物 B、氧化物、化合物 C、单质、化合物 D、金属、非金属
6、过氧化氢(H2O2)是隐形眼镜的洗液成分,下列说法正确的是( )
A、它由氢气和氧气组成 B、它由一个氢分子和一个氧分子构成
C、它由两个氢元素和两个氧元素构成 D、它由氢元素和氧元素组成
7、一个CO分子的质量为a千克,其中氧原子的质量为b千克,若以一个碳原子质量的1/12作为标准,则CO的相对分子质量是( )
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
8、将下列物质分别加入或通入到水中,所得溶液pH小于7的是( )
A、CuO B、CaO C、CO2 D、NaCl
9、使25克甲与5克乙充分反应,所得混合物中含10克甲和11克丙,还有另一种新物质丁,若甲、乙、丙、丁的相对分子质量分别为30、20、44、18,其化学式分别用A、B、C、D表示,则下列化学方程式正确的是( )
A、A+B==C+D B、A+2B==2C+D C、2A+B==2C+D D、2A+B==C+2D
10、现代医学证明,人类牙齿由一层称为碱式磷酸钙的坚硬物质保护着。碱式磷酸钙的化学式中除钙离子外还含有一个氢氧根离子和三个磷酸根离子(PO43-),则其化学式正确的是( )
A、Ca2(OH)(PO4)3 B、Ca3(OH)(PO4)3 C、Ca4(OH)(PO4)3 D、Ca5(OH)(PO4)3
11、有核电荷数小于18的X、Y两种元素,X元素原子的核电荷数为A,X3+和Y2-的核外电子数相同,则Y元素原子的核电荷数是( )
A、A-5 B、A+5 C、A-1 D、A+1
12、t℃时,在Ca(OH)2饱和溶液中加入少量CaO,恢复到原温度,不变的是( )
A、溶质的质量 B、溶液的质量 C、溶剂的质量 D、溶质的质量分数
13、下列各组是元素的原子结构示意图,其中具有相似化学性质的一对元素是( )
A、![]()
![]() B、
B、![]()
![]()
C、![]()
![]() D、
D、![]()
![]()
14、下列说法中,正确的是( )
A、含有结晶水的固体叫做晶体 B、含氧的化合物不一定是氧化物
B、pH的变化范围在1-14之间 D、能使酸或碱变色的物质叫做酸碱指示剂
15、由H+、Na+、SO42-、OH-组成的化合物一共有( )
A、3种 B、4种 C、5种 D、6种
二、选择题:以下各题有1-2个符合要求的答案(每小题2分,共10分)
16、对于“具有相同质子数的微粒”,下列叙述正确的是( )
A、一定具有相同的电子数 B、不一定是由同种元素组成的微粒
C、可能是原子和分子 D、一定是同种元素的微粒
17下面是一些学生的认识,其中正确的是( )
A、凡跟氧气发生的反应都是化合反应
B、最外层电子数为8的的微粒一定是稀有气体元素的原子
C、只用紫色石蕊试剂,能将NaCl、NaOH、稀H2SO4三种溶液鉴别开
D、在一切化学反应中,原子的数目没有增减,分子的数目也没有增减
放电
18、在雷雨中,部分氧气能转变为臭氧(O3),即3O2====2O3,下列说法正确的是( )
A、这是化学反应 B、这是物理变化
C、O2和O3 是同种物质 D、O2和O3 都是由氧元素组成的不同的单质
19、对于化学反应A+B==C+D,下列说法中,正确的是( )
A、若C、D分别为单质和化合物,则该反应一定是置换反应
B、若C、D分别为盐和水,则该反应一定是中和反应
C、若A、B、C、D都是化合物,该反应一定是复分解反应
D、若A为碱溶液,B为盐溶液,则C和D可能是两种沉淀
20、下列选项所述的两个量中,前者大于后者的是( )
A、KMnO4和K2MnO4中,锰元素的化合价 B、SO3中硫元素、氧元素的质量分数
B、稀盐酸和浓盐酸中,溶液的pH D、在化学反应中,反应物、生成物的分子个数
三、填空题:(每空1分,共36分)
21、从宏观上看,化学变化的基本特征是____________________________,从原子、分子的角度看,化学变化的实质是____________________________________________。
22、在横线上填写相应的符号:一个氢分子_______,2个氮原子_______,3个硫酸根离子________,正4价的碳元素_______。
23、写出下列物质的名称或化学式
| 物质名称 | 氧化铝 | 碱式碳酸铜 | 甲烷 | |||
| 化学式 | Fe(OH)2 | HCl | NH4HCO3 |
+6 +1 +1 -2
24、用S、 Na 、H、 O四种元素组成物质,据下表要求填空
| 物质类别 | 酸 | 碱 | 正盐 | 酸式盐 | 酸性氧化物 | 碱性氧化物 |
| 化学式 |
25、草木灰是农村常用的一种钾肥。已知草木灰的浸出液中含有K+、Cl-、CO32-,若K+与CO32-的个数比是9∶4,则K+与Cl-的个数比为_________。试写出草木灰的主要成分的化学式___________。
26、请自选反应物,按以下要求各写出一个化学方程式:
(1)属于氧化反应的化合反应________________________________;
(2)有气体生成的分解反应__________________________________;
(3)有盐生成的置换反应____________________________________;
(4)有水生成的复分解反应__________________________________。
 27、滚滚长江东流水,明日滔滔向北行,党的十六召开以后,一项总投资超过5000亿的特大型工程――南水北调工程呼之欲出。
27、滚滚长江东流水,明日滔滔向北行,党的十六召开以后,一项总投资超过5000亿的特大型工程――南水北调工程呼之欲出。
(1)南水北调工程必须遵循三个重大原则:其一,先节水后调水。下列各种标志中属于节水徽记的是_______。
其二,先治污后通水。某化工厂的废水呈现浅青绿色,经测定含有一定量的硫酸铜,只须往废水池中加入廉价、适量的______即可除去其中的Cu2+。
其三,先环保后用水。请你结合生产、生活、生态工程实际,举出三例环保措施。
①__________________________________________________________________
②__________________________________________________________________
③__________________________________________________________________
(2)水既普通又宝贵。请你归纳一下,水有哪些重要的化学性质(举三例),写出相应的化学方程式。
①__________________________________________________________________
②__________________________________________________________________
③__________________________________________________________________
28、如图是A、B、C三种物质的溶解度曲线。①其中可能是气体的是_______,②M点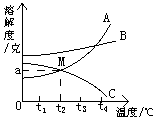 表示的意义是_________________,③t2℃时A物质饱和溶液质量分数为_____________,④t4℃时,在相同质量的溶剂中加入A、B配成饱和溶液,再降温到t1℃,析出溶质最多的是___________。
表示的意义是_________________,③t2℃时A物质饱和溶液质量分数为_____________,④t4℃时,在相同质量的溶剂中加入A、B配成饱和溶液,再降温到t1℃,析出溶质最多的是___________。
四、简答题(10分)
29、原子是由原子核和电子构成的。原子核在原子中所占体积极小,其半径约为原子半径的十万分之一,因此,相对而言,原子里有很大的空间。α粒子是带两个单位正电荷的氦原子。1911年,科学家用一束平行高速运动的α粒子轰击金箔时(金原子的核电荷数为79,相对原子质量为197)发现三种实验现象:
(1)有一小部分α粒子改变了原不的运动路径。原因是α粒子途径金原子核附近时,受到斥力而稍微改变了方向。
(2)大多数α粒子不改变原来的运动方向。原因是_______________________。
(3)极少数α粒子被弹了回来。原因是_______________________________________
____________________________________________。
30、取气密性良好的两支大小相同的医用注射器,将栓塞向外拉,分别吸入等体积的空气和水,用手指顶住针筒末端的小孔,将栓塞慢慢推入,请问哪一支针筒内的物质容易被压缩?用分子、原子的观点解释。请你再举出可以用这种原因解释的一个实例来。
五、计算题(14分)
31、有一种有毒物质,化学式为CS2,试回答:
(1)CS2的名称是____________;
(2)碳和硫的质量比是___________;
(3)CS2中硫的质量分数是__________;
(4)________克的CS2里含有6克碳。
32、某三价金属R的氧化物4g,与21g稀H2SO4恰好完全反应,测得反应后的溶液的溶质质量分数为40%,求(1)该金属的相对原子质量;(2)稀硫酸的溶质质量分数。