中考化学探究物质变化题汇编
一、选择题
1.(荆州市)对于化学反应:2KClO3+I2=2KIO3+Cl2,其反应类型属于 ( D )
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
2.(荆州市)在金属铂作催化剂和加热的条件下,氨气和氧气可发生如下反应:4NH3+5O2=4X+6H2O,其中X的化学式为 ( C )
A.N2 B.N2O C.NO D.NO2
3.(永州市)如下图所示,硅芯片是各种计算机、微电子产品的核心,工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅(SiO2+2C![]() Si+2CO↑),下列分析正确的是(C)
Si+2CO↑),下列分析正确的是(C)

A.二氧化硅发生了氧化反应 B.碳发生了还原反应
C.该反应属于置换反应 D.该反应属于复分解反应
4.(永州市)北京市为减轻大气污染,在汽车尾气排放口加装“催化净化器”,可将尾气中的有害气体CO、NO转化为参与大气循环的无毒混合气体,其反应的化学方程式可表示为:2CO+2NO![]() N2+2X,则X的化学式为(D)
N2+2X,则X的化学式为(D)
A.O2 B.H2O C.NO2 D.CO2
5.(鄂州市)在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物 质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 25 |
| 反应后质量/g | 未测 | 21 | 10 | 9 |
下列说法中不正确的是( A )
A.该反应为分解反应 B.该反应遵守质量守恒定律
C.X中未测值为零 D.若Q为氧气,则该反应为氧化反应
6.(沈阳)在食盐中加入KIO3有益于防治地方性甲状腺肿大。检验食盐中是否含有碘酸钾,可利用化学反应:![]() ,其中X的化学式为(B )
,其中X的化学式为(B )
A. HI B. KI C. ![]() D.
D. ![]()
二、填空题
1.(十堰市)阅读下列内容,解答与净化水有关的问题:
(1)用纱网捞起水面上的菜叶、塑料等,该操作利用的化学原理是____ ____;
(2)二氧化氯(ClO2)可用于自来水消毒杀菌,其中氯元素的化合价是____ __;
![]()
![]() (3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示。(其中
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示。(其中![]() 表示氯原子,
表示氯原子, ![]() 表示钠原子, 表示氧原子)
表示钠原子, 表示氧原子)
请写出反应的化学方程式_______________________________________。
(1)过滤 (2)+4价(或+4) (3)Cl2 + 2NaClO2 = 2ClO2 + 2NaCl
2.(沈阳)实验室用溶质质量分数为8%的过氧化氢溶液与二氧化锰混合制取氧气,二氧化锰在反应中起___________作用,该反应的基本反应类型为____________________。
催化 分解反应
3.(沈阳)下图中为某化学反应的微观模拟示意图:![]() 表示氮原子,
表示氮原子,![]() 表示氢原子。请你根据图示回答下列问题:
表示氢原子。请你根据图示回答下列问题:

(1)A物质由__________________元素组成;
(2)A、B、C三种物质中属于化合物的是____________________________________;
(3)该反应的化学方程式为_____________________________________________。
(1)氮(或N,或一种)(2)C(或氨气,或![]() )(3)
)(3)![]()
4.(哈尔滨)下图是甲烷与氧气反应的微观示意图:
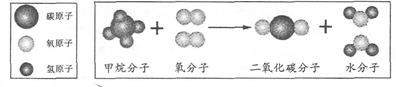
请通过比较、归纳,回答下列问题(不利用相对原子质量):
(1)一个甲烷分子和一个二氧化碳分子的不同点是 ;
(2)氧分子、二氧化碳分子、水分子的相同点是 ;
(3)根据上述示意图,请从微观角度描述你获得的关于化学变化的一个信息
。
(1)分子的构成不同(2)都含有氧原子(3)在化学变化前后原子的个数和种类不变
三、计算题
1.(重庆市)电解水时,常常要加入少量氢氧化钠使反应容易进行。现将加有氢氧化钠的水通电一段时间后,产生lg氢气,其中氢氧化钠的质量分数也由4.8%变为5%。计算:
(1)生成氧气的质量。 (2)电解后剩余水的质量。
(1) 8g (2)205.2 g
2.(鄂州市)消化药片所含的物质能中和胃里过多的胃酸。某种消化药品的标签如图4所示。医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片。试计算,患者按此处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)
解:设理论上可中和HCl的质量为X
Mg(OH)2 + 2HCl == MgCl2 + 2H2O (1分 )
58 73
2×3×250mg X (3分 )
58:73=2×3×250mg:X (1分 )
X=1880mg (1分 )
答:理论上可中和1880mg的HCl
3.(长沙)2005年5月22日上午11时08分,中国登山测量队成功登上珠峰顶,这是继1975年后我国再次对珠穆朗玛峰高度进行精确测量。氢化钙(CaH2)固体是登山队员常用的能源提供剂,用它和水反应生成氢氧化钙和氢气:
CaH2 + 2H2O == Ca(OH)2 + 2H2↑
氢气供燃烧之需。现有84g氢化钙与足量水反应,可生成多少克氢气?
解:设84g氢化钙与足量水反应生成氢气的质量为x (1分)
CaH2 + 2H2O == Ca(OH)2 + 2H2↑
42 4
84g x (1分)
![]()
![]() (2分)
(2分)
x = 8g (1分)
答:84g氢化钙与足量水反应可生成氢气8g。 (1分)