八年级科学第一章《粒子的模型与符号》测试卷
班级 姓名
(考试时间90分钟)
本卷所用的相对原子质量:H 1;O 16;Ca 40;N 14;C 12
一、选择题(每小题2分,共40分)
1、固态碘、碘溶液和碘蒸气中都存在碘分子,馒头遇到固态碘、碘溶液和碘蒸气都能
变蓝色这一实验现象说明----------------------------------------------------------------------------( )
A. 分子始终在做无规则运动 B. 分子之间存在空隙
C. 分子之间存在引力和斥力 D. 分子是保持物质化学性质的一种微粒
2、钙是构成人体骨骼和牙齿的重要成分,这里的“钙”是指-----------------------------------( )
A. 钙单质 B. 钙元素 C. 钙原子 D. 钙离子
3、道尔顿的原子学说曾经起了很大作用。他的学说中,包含下述三个论点:①原子是
不能再分的粒子;②同种元素的原子的各种性质和质量都相同;③原子是微小的实
心球体。从现在的观点看,你认为这三个论点中,不确切的是----------------------------( )
A. 只有③ B. 只有①③ C. 只有②③ D. ①②③
4、1992年,我国科学家首次发现了汞元素的一种新原子,这种汞原子的相对原子质量
为208,核电荷数为80,这种汞原子的核外电子数为-----------------------------------------( )
A. 80 B. 128 C. 208 D. 288
5、过氧化氢(H2O2)的水溶液俗称双氧水,在医疗上可作为消毒杀菌剂。每个H2O2分子是由( )
A. 氢原子和氧原子组成 B. 一个氢分子和一个氧分子构成
C. 氢元素和氧元素组成 D. 两个氢分子和两个氧原子构成
6、下列化合物中,氮元素的化合价为+2价的是----------------------------------------------------( )
A. N2O B. NO C. NO2 D. N2O5
7、2H表示---------------------------------------------------------------------------------------------------( )
A. 两个氢元素 B. 两个氢原子 C. 两个氢离子 D. 两个氢分子
8、依据卢瑟福的原子行星模型理论,在原子中绕核高速旋转的是----------------------------( )
A. 核子 B. 电子 C. 质子 D. 中子
9、我们每天都要喝水,都要用水。水是一种-------------------------------------------------------( )
A. 元素 B. 单质 C. 化合物 D. 混合物
10、现代科学又发现了H3、C60、C90、C240、N5、N60 ……据此可做出的推测是----------( )
①同一种元素可以形成多种单质 ②单质可能存在复杂的分子结构
③单质的研究具有广阔的前景 ④同种元素形成的单质之间可能存在更多的互相转化
A. 只有①② B. 只有②③ C. 只有③④ D. ①②③④
11、下列关于“O2”中数字2的说法中,正确的是-----------------------------------------------( )
A. 表示两个氧原子 B. 表示两个氧元素
C. 表示两个氧分子 D. 表示一个氧分子由两个氧原子构成
12、在5H2O和5H2SO4中,一样多的是------------------------------------------------------------( )
A. 氢原子 B. 氢分子 C. 氢元素 D. 氢元素质量分数
13、下列关于Fe、Fe2+、Fe3+说法中,正确的是-------------------------------------------------( )
A. 它们的化合价相同 B. 它们的质子数和中子数都不同
C. 它们的核外电子数不同 D. 它们的性质完全相同
14、元素周期表中前七周期元素数如下:请分析周期数与元素数的关系,然后预言第八周期
| 周期数 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
| 元素数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
最多可能含有的元素种数目为--------------------------------------------------------------------( )
A. 18 B. 32 C. 50 D. 64
15、请你分析下列事实,其中能证明分子是可分的是---------------------------------------------( )
A. 冷却热饱和硝酸钾溶液有硝酸钾晶体析出 B. 海水晒干得到食盐
C. 水通电得到氢气和氧气 D. 水受热变成水蒸气
16、下列化学式是按照物质组成及化合价变化规律排列的:P、N2、P2O3、N2O3、H3PO4、
( ),在( )中能填入的物质是-------------------------------------------------------------( )
A. P2O5 B. NO2 C. H3P D. HNO3
17、铁的相对原子质量为56,它表示-----------------------------------------------------------------( )
A. 铁单质的质量为56克 B. 一个铁原子的质量为56克
C. 铁的原子核内有56个质子 D. 一个铁原子的质量是一个碳―12原子质量1/12的56倍
18、下列是计算氢氧化钙[Ca(OH)2]相对分子质量的式子,其中正确的是---------------( )
A. 40+16+1=57 B. 40+2×(16+1)=74
C. 40×16+1=640 D. 40×2×16×1=1280
19、元素S的相对原子质量为32,它的氧化物含氧60%,则该氧化物的化学式为--------( )
A. SO2 B. SO C. SO3 D. S2O3
20、某种氮的氧化物,其中氮元素和氧元素的质量比为7∶20,则该氧化物中氮原子和
氧原子的个数比为------------------------------------------------------------------------------------( )
A .1∶2 B. 3∶2 C. 5∶2 D. 2∶5
二、填空题(每格1分,共40分)
21、⑴构成物质的微粒有 、 和 。化学变化中的最小微粒是 。
⑵构成原子核的微粒是 、 。由于 所带正电和 所带负电,
电量相等,电性相反,所以原子显电 性
22、⑴用符号表示:
2个氯原子 3个镁离子 4个氧化铜分子
正3价的铝元素 3个碳酸根离子
⑵写出下列物质的化学式:
氦气 臭氧 金刚石 硫化锌
⑶ 写出3SO42-中各数字表示的意义:
“3” “2”
“4”
23、一氧化氮会造成大气污染,可它在人体中有独特的功能。有三位科学家由于对一氧化氮的研究所取得的医学成果,获得1998年度诺贝尔医学奖。一氧化氮也被誉为“明星分子”。请写出一氧化氮的化学式 。
24、科学家在宇宙中发现了一种由氢元素组成的新物质,其化学式为H3。在一个H3分子中
有 个氢原子,H3的相对分子质量是 。
25、以下每小题由三种物质形成一组,从备选答案中找出跟它们同一类的物质,将编号填入空格。
⑴氧气、氮气、氯气、 。
A. 水蒸气 B. 氦气 C. 氢气 D. 二氧化碳
⑵铝、镁、铁、 。
A. 氯化钾 B. 锌 C. 二氧化锰 D. 高锰酸钾
⑶二氧化硫、五氧化二磷、二氧化碳、 。
A. 水 B. 氧气 C. 硫酸铜 D. 氯化钾
26、A、B2-、C+三种微粒都具有10个核外电子,A的元素符号为 ,C2B组成的化合物的化学式为 ,B元素与氢元素组成的化学式为 。
27、啤酒、红酒和白酒中都含有乙醇(C2H5OH),饮酒后乙醇可进入人体血液中,科学实验表明,当乙醇在人体血液中的含量超过80mg/100mL血(每100mL血中含有80mg乙醇)时,便会影响人的驾车或操作机器的能力;已知饮用某啤酒1大杯(0.56L),会使血液中乙醇含量升高30mg/100mL血。回答下列问题:
⑴ 乙醇中含有 种元素
⑵ 乙醇分子中碳、氢、氧原子的个数比是
⑶ 李明饮用了3大杯上述啤酒后, 其体内每 100mL 血液中乙醇的含量(理论上)升高
mg, (填“影响”或“不影响”)其驾车或操作机器的能力。
28、医药上用的阿斯匹林的组成里含有4.5%的氢、35.5%的氧、60%的碳,其分子量为180。阿斯匹林的化学式为CxHyOz,则x、y、z的值分别是 、 、 。
29、使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是 ;若CO2和CO的质量相等,则CO2和CO中的碳元素质量比为 。
30、某农田作物需施含氮元素的化肥。如果施用了尿素[化学式为CO(NH2)2]120Kg,含
氮 Kg。
三、实验设计、探究题(共20分)
31、(4分)原子由原子核和电子构成的。原子核在原子中所占体积极小,其半径约为原子半径的十万分之一,因此,相对而言,原子里有很大的空间。α粒子是带两个单位正电荷的氦原子。1911年,科学家有一束平行高速运动的α粒子轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现三种实验现象:
⑴有一小部分α粒子改变了原来的运动路径。原因是α粒子途经金原子核附近时,受到斥力而稍微改变了运动方向。
⑵大多数α粒子不改变原来的运动方向。原因是 。
⑶极少数α粒子被弹了回来。原因是 。
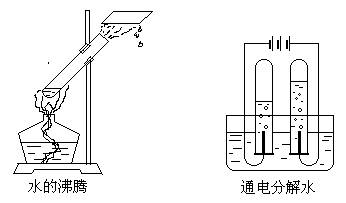 32、(8分)下图表示的是水的两种变化,请分别从宏观和微观(原子和分子的观点)两个角度描述它们的变化过程。
32、(8分)下图表示的是水的两种变化,请分别从宏观和微观(原子和分子的观点)两个角度描述它们的变化过程。
33、(8分)油炸食品、烧烤食品等被营养专家称作“垃圾食品”,这是因为在制作过程中不仅产生大量有害气体污染环境,而且食物中还会产生一些强致癌物质,故此类食品不宜多吃、常吃。如在食物的煎炸过程中会产生一种有害物质――丙烯醛,化学式为(C2H3CHO)。试回答:
⑴丙烯醛的相对分子质量。
⑵丙烯醛中各元素的质量比。
⑶丙烯醛中氧元素的质量分数。
⑷112克丙烯醛中碳元素的质量为多少克。
八年级第一章《粒子的模型与符号》 测试卷(参考答案)
班级 姓名
(考试时间90分钟)
本卷所用的相对原子质量:H 1;O 16;Ca 40;N 14;C 12
一、选择题(每小题2分,共40分)
1、固态碘、碘溶液和碘蒸气中都存在碘分子,馒头遇到固态碘、碘溶液和碘蒸气都能
变蓝色这一实验现象说明----------------------------------------------------------------------------( D )
A. 分子始终在做无规则运动 B. 分子之间存在空隙
C. 分子之间存在引力和斥力 D. 分子是保持物质化学性质的一种微粒
2、钙是构成人体骨骼和牙齿的重要成分,这里的“钙”是指-----------------------------------( B )
A. 钙单质 B. 钙元素 C. 钙原子 D. 钙离子
3、道尔顿的原子学说曾经起了很大作用。他的学说中,包含下述三个论点:①原子是
不能再分的粒子;②同种元素的原子的各种性质和质量都相同;③原子是微小的实
心球体。从现在的观点看,你认为这三个论点中,不确切的是----------------------------( D )
A. 只有③ B. 只有①③ C. 只有②③ D. ①②③
4、1992年,我国科学家首次发现了汞元素的一种新原子,这种汞原子的相对原子质量
为208,核电荷数为80,这种汞原子的核外电子数为-----------------------------------------( A )
A. 80 B. 128 C. 208 D. 288
5、过氧化氢(H2O2)的水溶液俗称双氧水,在医疗上可作为消毒杀菌剂。每个H2O2分子是由( D )
A. 氢原子和氧原子组成 B. 一个氢分子和一个氧分子构成
C. 氢元素和氧元素组成 D. 两个氢分子和两个氧原子构成
6、下列化合物中,氮元素的化合价为+2价的是----------------------------------------------------( B )
A. N2O B. NO C. NO2 D. N2O5
7、2H表示---------------------------------------------------------------------------------------------------( B )
A. 两个氢元素 B. 两个氢原子 C. 两个氢离子 D. 两个氢分子
8、依据卢瑟福的原子行星模型理论,在原子中绕核高速旋转的是----------------------------( B )
A. 核子 B. 电子 C. 质子 D. 中子
9、我们每天都要喝水,都要用水。水是一种-------------------------------------------------------( C )
A. 元素 B. 单质 C. 化合物 D. 混合物
10、现代科学又发现了H3、C60、C90、C240、N5、N60 ……据此可做出的推测是----------( D )
①同一种元素可以形成多种单质 ②单质可能存在复杂的分子结构
③单质的研究具有广阔的前景 ④同种元素形成的单质之间可能存在更多的互相转化
A. 只有①② B. 只有②③ C. 只有③④ D. ①②③④
11、下列关于“O2”中数字2的说法中,正确的是-----------------------------------------------( D )
A. 表示两个氧原子 B. 表示两个氧元素
C. 表示两个氧分子 D. 表示一个氧分子由两个氧原子构成
12、在5H2O和5H2SO4中,一样多的是------------------------------------------------------------( A )
A. 氢原子 B. 氢分子 C. 氢元素 D. 氢元素质量分数
13、下列关于Fe、Fe2+、Fe3+说法中,正确的是--------------------------------------------------( C )
A. 它们的化合价相同 B. 它们的质子数和中子数都不同
C. 它们的核外电子数不同 D. 它们的性质完全相同
14、元素周期表中前七周期元素数如下:请分析周期数与元素数的关系,然后预言第八周期
| 周期数 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
| 元素数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
最多可能含有的元素种数目为--------------------------------------------------------------------( C )
A. 18 B. 32 C. 50 D. 64
15、请你分析下列事实,其中能证明分子是可分的是---------------------------------------------( C )
A. 冷却热饱和硝酸钾溶液有硝酸钾晶体析出 B. 海水晒干得到食盐
C. 水通电得到氢气和氧气 D. 水受热变成水蒸气
16、下列化学式是按照物质组成及化合价变化规律排列的:P、N2、P2O3、N2O3、H3PO4、
( ),在( )中能填入的物质是-------------------------------------------------------------( D )
A. P2O5 B. NO2 C. H3P D. HNO3
17、铁的相对原子质量为56,它表示-----------------------------------------------------------------( D )
A. 铁单质的质量为56克 B. 一个铁原子的质量为56克
C. 铁的原子核内有56个质子 D. 一个铁原子的质量是一个碳―12原子质量1/12的56倍
18、下列是计算氢氧化钙[Ca(OH)2]相对分子质量的式子,其中正确的是---------------( B )
A. 40+16+1=57 B. 40+2×(16+1)=74
C. 40×16+1=640 D. 40×2×16×1=1280
19、元素S的相对原子质量为32,它的氧化物含氧60%,则该氧化物的化学式为--------( C )
A. SO2 B. SO C. SO3 D. S2O3
20、某种氮的氧化物,其中氮元素和氧元素的质量比为7∶20,则该氧化物中氮原子和
氧原子的个数比为------------------------------------------------------------------------------------( D )
A .1∶2 B. 3∶2 C. 5∶2 D. 2∶5
二、填空题(每格1分,共40分)
21、⑴构成物质的微粒有 原子 、 分子 和 离子 。化学变化中的最小微粒是 原子 。
⑵构成原子核的微粒是 质子 、 中子 。由于 质子(原子核) 所带正电和 电子 所带负电,
电量相等,电性相反,所以原子显电 中 性;
22、⑴用符号表示:
2个氯原子 2Cl 3个镁离子 3Mg2+ 4个氧化铜分子 4CuO
正3价的铝元素 +3Al 3个碳酸根离子 3CO32-
⑵写出下列物质的化学式:
氦气 He 臭氧 O3 金刚石 C 硫化锌 ZnS
⑶ 写出3SO42-中各数字表示的意义:
“3” 3个硫酸根离子 ; “2” 硫酸根离子带2个单位负电荷 ;
“4” 一个硫酸根离子中有4个氧原子。
23、一氧化氮会造成大气污染,可它在人体中有独特的功能。有三位科学家由于对一氧化氮的研究所取得的医学成果,获得1998年度诺贝尔医学奖。一氧化氮也被誉为“明星分子”。请写出一氧化氮的化学式 NO 。
24、科学家在宇宙中发现了一种由氢元素组成的新物质,其化学式为H3。在一个H3分子中有
3 个氢原子,H3的相对分子质量是 3 。
25、以下每小题由三种物质形成一组,从备选答案中找出跟它们同一类的物质,将编号填入空格。
⑴氧气、氮气、氯气、 C 。
A. 水蒸气 B. 氦气 C. 氢气 D. 二氧化碳
⑵铝、镁、铁、 B 。
A. 氯化钾 B. 锌 C. 二氧化锰 D. 高锰酸钾
⑶二氧化硫、五氧化二磷、二氧化碳、 A 。
A. 水 B. 氧气 C. 硫酸铜 D. 氯化钾
26、A、B2-、C+三种微粒都具有10个核外电子,A的元素符号为 Ne ,C2B组成的化合物的化学式为 Na2O ,B元素与氢元素组成的化学式为 H2O 。
27、啤酒、红酒和白酒中都含有乙醇(C2H5OH),饮酒后乙醇可进入人体血液中,科学实验表明,当乙醇在人体血液中的含量超过80mg/100mL血(每100mL血中含有80mg乙醇)时,便会影响人的驾车或操作机器的能力;已知饮用某啤酒1大杯(0.56L),会使血液中乙醇含量升高30mg/100mL血。回答下列问题:
⑴ 乙醇中含有 3 种元素
31、⑴α粒子通过原子内、原子间的空隙;⑵α粒子撞击了金原子核而被弹回;
⑵ 乙醇分子中碳、氢、氧原子的个数比是 碳∶氢∶氧=2∶6∶1 ;
⑶ 李明饮用了3大杯上述啤酒后, 其体内每 100mL 血液中乙醇的含量(理论上)升高
90 mg, 影响 (填“影响”或“不影响”)其驾车或操作机器的能力。
28、医药上用的阿斯匹林的组成里含有4.5%的氢、35.5%的氧、60%的碳,其分子量为180。阿斯匹林的化学式为CxHyOz,则x、y、z的值分别是 9 、 8 、 4 。
29、使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是 11∶14 ;若CO2和CO的质量相等,则CO2和CO中的碳元素质量比为 7∶11 。
30、某农田作物需施含氮元素的化肥。如果施用了尿素[化学式为CO(NH2)2]120Kg,含
氮 56 Kg。
三、实验设计、探究题(共20分)
31、(4分)原子由原子核和电子构成的。原子核在原子中所占体积极小,其半径约为原子半径的十万分之一,因此,相对而言,原子里有很大的空间。α粒子是带两个单位正电荷的氦原子。1911年,科学家有一束平行高速运动的α粒子轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现三种实验现象:
⑴有一小部分α粒子改变了原来的运动路径。原因是α粒子途经金原子核附近时,受到斥力而稍微改变了运动方向。
⑵大多数α粒子不改变原来的运动方向。原因是 α粒子通过原子内、原子间的空隙 。
⑶极少数α粒子被弹了回来。原因是 α粒子撞击了金原子核而被弹回 。
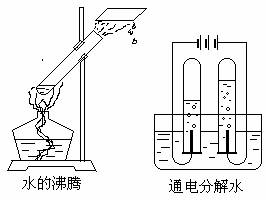 32、(8分)下图表示的是水的两种变化,请分别从宏观和微观(原子和分子的观点)两个角度描述它们的变化过程。
32、(8分)下图表示的是水的两种变化,请分别从宏观和微观(原子和分子的观点)两个角度描述它们的变化过程。
解:宏观⑴水在加热条件下发生物理变化,
由液态水变成水蒸气
⑵水在通电条件下发生化学变化,
分解成氢气和氧气
微观⑴水分子受热,分子运动速度加快,
分子间间隔变大
⑵通电条件下,水分子分解成氢、氧
原子,两个氢(氧)原子结合成一个
氢(氧)分子,很多氢(氧)分子聚
集成氢(氧)气
33、(8分)油炸食品、烧烤食品等被营养专家称作“垃圾食品”,这是因为在制作过程中不仅产生大量有害气体污染环境,而且食物中还会产生一些强致癌物质,故此类食品不宜多吃、常吃。如在食物的煎炸过程中会产生一种有害物质――丙烯醛,化学式为(C2H3CHO)。试回答:
⑴丙烯醛的相对分子质量。56
⑵丙烯醛中各元素的质量比。9∶1∶4
⑶丙烯醛中氧元素的质量分数。28.6%
⑷112克丙烯醛中碳元素的质量为多少克。72
第一章 粒子的模型与符号 测试卷(参考答案)
1、D;2、B;3、D;4、A;5、D;6、B;7、B;8、B;9、C;10、D;11、D;12、A;
13、C;14、C;15、C;16、D;17、D;18、B;19、C;20、D;21、⑴原子,分子,离子,原子;⑵质子,中子,质子,电子,中;22、⑴2Cl,3Mg2+,4CuO,+3Al,3CO32-;⑵He,O3,C,ZnS;⑶3个硫酸根离子,硫酸根离子带2个单位负电荷,一个硫酸根离子中有4个氧原子;23、NO;24、3,3;25、⑴C;⑵B;⑶A;26、Ne,Na2O,H2O;
27、⑴3;⑵2∶6∶1;⑶90,影响;28、9,8,4;29、11∶14,7∶11;30、56;
31、⑴α粒子通过原子内、原子间的空隙;⑵α粒子撞击了金原子核而被弹回;
32、宏观⑴水在加热条件下发生物理变化,由液态水变成水蒸气
⑵水在通电条件下发生化学变化,分解成氢气和氧气
微观⑴水分子受热,分子运动速度加快,分子间间隔变大
⑵通电条件下,水分子分解成氢、氧原子,两个氢(氧)原子结合成一个氢(氧)分子,很多氢(氧)分子聚集成氢(氧)气
33、⑴56,⑵9∶1∶4,⑶28.6%,⑷72;