���꼶�ϵ�һ������θ���ǿ����ϰ����һ�Σ�
һ���ᡢ��ε���ʶ��Ԫ�ط��š�Ԫ����ԭ���ŵĻ��ϼۡ�����ε���ɣ���
1��д�������ᡢ��εĻ�ѧʽ��
���������� ���� �������� ������ ����̼���� ������ ��������������
���������� ���� ������ͭ�� ���� ���������� ������ ��ˮ�� ����
�Ȼ������������ᱵ�� ����������ͭ�� ������̼��þ�������� �Ȼ���������
ʯ��ˮ����ʯ�ҡ���ʯ�� ���������ռ�������� ���� ʳ������������
ʯ��ʯ�� ���� �մ�ڼ������������� С�մ���������
2���ж��������ʻ�ѧʽ���ᡢ��Σ�
NaHCO3 ���� ��BaCl2���� ��Fe(OH) 2���� ��HClO���� ��KMnO4���� ��
NH3��H2O���� ��Ca(OH)2���� ��
3��д������������Ӷ�Ӧ��Ļ�ѧʽ��
Cl- ������SO42- ��������NO3- ������ CO32- ��������SO32-������PO43-������
4��д�����н������Ӷ�Ӧ��Ļ�ѧʽ��
Na+ ��������Ca2+ ����������Cu2+��������Fe3+��������Ba2+��������
Mg2+ �������� Al3+�������� Zn2+�������� K+������ NH4+���������� ��
3����1����H��C��O��Na����Ԫ�ذ�Ҫ��д����ѧʽ��
���嵥�����������嵥���������� �ǽ��������� ��������������������������
���������� �� ���������� ���������������� ��
��2����H��N��O����Ԫ�ذ�Ҫ��д����ѧʽ��
�����к���������嵥���������� ��������
������ľ����ȼ�����嵥�������� ������
�ǽ��������������������������� ��
������������ �� �������������������������� ��
�������ָʾ����
| ��Һ ���ָʾ�� | ���� | ���� | ʳ��ˮ | ��� | ʯ��ˮ | ��ˮ |
| ʯ����Һ | ||||||
| ��̪��Һ | ||||||
| PHֵ��>��<��=7) |
![]() ��������ε��ܽ��ԣ��ھ������ܵĴ̡����ܵĴw��
��������ε��ܽ��ԣ��ھ������ܵĴ̡����ܵĴw��
NaOH���� CuSO4������ KNO3�������� CaCO3 ���� BaSO4��������AgNO3�������� Cu(OH)2����FeCl3��������BaCO3�������� Na2SO4������ Na2CO3������ MgCl2�������� KCl������ Ca(OH)2����Al2(SO4)3������ ZnSO4�� ����CuSO4������ AgCl
�ġ���Ӧ������
1���������ᷴӦ��
�����˳�������������������������������������������������
�ж��ܷ�Ӧ�����������ܵľͽ���ѧ����ʽд������
Cu + H2SO4���������������� Zn + HNO3 ������
Fe + H2SO4���������������� Al + HCl��
Mg + H2SO4���������������� Ag + HCl��
��1����Ӧ�����ǣ��������������������������������������� ������
��2����Щ���������Ӧ��������������
���� ����������������������������������������������������������
2������������Һ��Ӧ��
�ж����з�Ӧ�ܷ�Ӧ���ܵľͽ���ѧ����ʽд������
Fe + CuSO4�� ���������������� Mg + CaCl2����������Cu + AgNO3���� �������� Cu + FeSO4�� ���������� Fe + Ag NO3��
��Ӧ������������������������ ��������������������������������
3�����ֽⷴӦ��
��Ӧ��������������������������������������������������������
�ж����з�Ӧ�ܷ������ܵľͽ���ѧ����ʽд������
HCl +��NaOH�������������������� Cu(OH)2��+��H2SO4��
H2SO4 + BaCl2��������������������AgCl + HNO3��
Cu(OH)2 + Na2CO3 ���������� ���������� NaOH + KNO3��
AgNO3 + Na Cl������������������ KCl�� +�� Na NO3��
�塢�Ĵ������Ӧ���ͣ�
1������һ����
���Ϸ�Ӧ����������������������������������������������������
�ֽⷴӦ����������������������������������������������������
�û���Ӧ�������������������������������������� ��������������
���ֽⷴӦ��������������������������������������������������
2��д�������ܷ�Ӧ�Ļ�ѧ��ʽ������������д����Ӧ���ͣ������Ĵ�Ӧ��д�����������֣�
����������������������������������������������������� ���������� ��
��ͭ��ϡ�������������������������������������������� ���������� ��
��������������ҩƷ�к�θ������������������������������������������ ����������
���������Ʒ��ڿ����б��������������������������������� ���������� ��������
������ϡ���ᷴӦ�������������������������������������� ���������� ��
��̼�����������ϣ������ԭ���������������������������� ���������� ��
������ͭ��ϡ������������������������ ������������������ ���������� ��
������������Һ����ϡ���������������������������������� ���������� ����������
����������������������������������������������������� ���������� ������������Ȼ�����Һ���������������������������������� ���������� ��
��̼��ȶ��ֽ������������������������������� �������������������� ��
�и�������ʯ��ʯ���������������������������������������� ���������� ��
����ʯ�ҷ���ˮ���������������������������������������� ���������� ��
�Ҵ���ʯ��ϡ���ᣨʵ������CO2������������������������������ ���������� ��
�Ӷ�����̼ʹ����ʯ��ˮ����������������������������������� ������ ���� ��
��̼��أ���ľ�ң����������������������������������������� ���������� ��
������ϰ����һ�Σ�
1.��07���ݣ���������ƾ�����һ�ֺ��±���ƿ��������������ƣ�Na2S2O3������
A���������B���ᡡ��C����� D����
2.(07����)���в����У�����ȷ����
A.�ý�ͷ�ι����Թ��еμ�Һ��ʱ���ѵι������Թ���
B.���������ƹ��������ƽ���̵IJ��������г���
C.��ʵ��������ȡCO2����ʱ��Ӧ�ȼ��װ��������
D.Ũ����մ��Ƥ���ϣ����ò�����Ȼ���ô���ˮ��ϴ����Ϳ��3%��5%��̼��������Һ.
3.(07����)ijͬѧ��Ƶ����и�ʵ�鷽���У�����Ϊ���ܴﵽʵ��Ŀ�ĵ���
A.��ȼ�ŵ�ľ�����������̼������
B.���������ij����ʯ��ˮ���Գ�ȥCaCl2��Һ�е�HCl
 C.��Ũ�����ȥ�����л��е�ˮ����
C.��Ũ�����ȥ�����л��е�ˮ����
D.��ʯ����Һ��������ʯ��ˮ������������Һ
4.(07�ӱ�)�������ᡢʯ��ˮ������ͭ�dz��л�ѧ�г��������ʣ��������ʼ�ķ�Ӧ��ϵ����ͼ��ʾ��ͼ����Բ�ཻ���֣�A��B��C��D����ʾ���ʼ䷴Ӧ����Ҫʵ����������������ȷ����
A�������ݲ�����������������������������������B������������
C���к�ɫ�������������������������������� D������ɫ��������
5. (07ɽ��)�����������ӵı仯��һ�����������ִ��ڱ��ʵ��������ֱ仯��
A�����ڷ����ڿ����е�����������������
B�����ڳ��ڷ��õ�Ũ������������
C�����õ���ʯ����������
D�����õ�����������������
6. (07̩��)����˵����ȷ����
A���кͷ�Ӧ���κ�ˮ���ɣ�������κ�ˮ���ɵķ�Ӧһ�����кͷ�Ӧ
B���������к�����Ԫ�أ�������Ԫ�صĻ����ﲻһ����������
C�����ж�������Ԫ�أ����Ժ�����Ԫ�صĻ�����һ���Ǽ�
D���û���Ӧһ���е������ɣ������е������ɵķ�Ӧһ�����û���Ӧ
7.(07̩��)�������ʵ���Һ���ڷ����ڿ����У���Һ����������ѧ�仯�����ٵ���
����A���ռ������B��ʯ��ˮ������������C��Ũ���ᡡ���������������� D���Ȼ���
8. (07�ϲ�)�������ʵ���;�����������������ʵ���
�� A���ɱ������˹����ꡡ���������������� B���������ڳ�����
�� C����������ҽ�Ƽ��ȡ����������������� D����ʯ�����ڸ�����������
9. (07�Թ�)����˶���������е֮ǰ���á�þ�ۡ����֣���þ�ۡ�����Ҫ�ɷ���MgCO3���Ը��ݳ������ʵ�����жϳ�MgCO3����
A��������� B���ᡡ������C��������� D����
10. (07��)�����������ʵ���Һ�����÷�̪��Һ��ͬ������֮�����Ӧ���ܼ���������� ���� ��
����A��NaOH�� Ba(OH)2�� HCl������������ B��NaOH����HCl����NaCl
C��NaOH�� H C1������HNO3������������ D��H2SO4����NaCl�� Na2SO4
11.(07��ͷ)ijͬѧ��С�ı��Ʒ�����(�Ʒ䶾Һ�ʼ���)��Ϊ�˼�����ʹ����ͿĨ
��A��Ũ���ᡡ������������������������������B��ʳ��(pH=3)
��C��ʳ��ˮ(pH=7)��������������������������D���մ�����ˮ(pH=9-10)
12. (07��ͷ)����ʵ�������ó����е�ʳ�Ρ�ʳ�ס����������������ɹ�����
���ټ�������ˮ���Ƿ��������ӣ��ڼ��鼦�����ܷ�������۳�ȥ��ˮƿ�е�ˮ����
�� A���٢ڢۡ���B���ڢۡ���C���٢ۡ���D���٢�
13. ��07��̨������������ʵ����Ƽ�������ʵ�����������������˵��C02��Na0H��Һ�����˷�Ӧ����
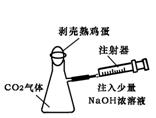
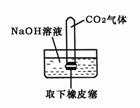
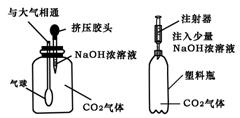
������ (A)�������������������� (B)�������������� (C)������������(D)
14.��07���쳤�������ס��ҡ���������ƿ��Һ�ֱ���K2CO3��Ba(NO3)2��H2S04��K2S04�е�һ�֣����мֱ������ҡ�������������Ӧ�����ǣ����� ��
A��K2SO4 �������� B��H2S04���������� C��Ba(NO3)2��������D��K2CO3
15.��07���쳤���������л�ѧ��Ӧ�У�������ͼ��ͨ���龰���ǣ����� ��
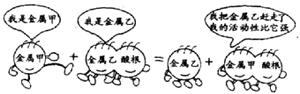 �� A��C+2CuO
�� A��C+2CuO![]() 2Cu+CO2��
2Cu+CO2��
�� B��Cu+2AgNO3===Cu(NO3)2+2Ag
�� C��Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
�� D��BaCl2+Na2SO4===BaSO4��+2NaCl
16.(07����)�����Լ��У��ܰ�KOH��Һ��ϡ���ᡢCaCl2��Һһ�μ����������
A.KCl��Һ����B. K2CO3��Һ����C. NaNO3��Һ����D.ϡ����
17.(07̩��)�������е��Լ���ȥ�����������������ʣ�����ҩƷ��������
A��NaOH��Һ�л���Na2CO3��ϡ���ᣩ����B��NaCl��Һ�л���Na2SO4 (BaC12��Һ)
C��KCl��Һ�л���K2CO3��ϡ���ᣩ����������D��CO�л���CO2 (NaOH��Һ)
18.(07̩��)���������塷��������һ�����£����������ĺ��������ˡ���Ȫ������Ȫ����������֮�������ԣ�����Ѯ�ձ�������������������ʿ���ط���ʿָ�㣬������Ϫ�ġ�����Ȫ��ˮ����תΣΪ��������Ȫ���͡�����Ȫ���������Ļ�ѧ���ʿ�����
����A��NaCl��CaCl2 �������� ��������������B��Na2SO4��KC1
����C��BaCl2��NaNO3 ��������������������D��CuSO4��Ca(OH)2
19. (07̩��)���и������ʣ�ֻ����������Һ���ϣ����ܼ����������
A��K2SO4��BaCl2��NaNO3��NaCl ��������������B��HCl��Na2CO3��BaCl2��Na2SO4
��C��KOH��Na2SO4��CuSO4��HCl ����������������D��KCl��AgNO3��KNO3��NaCl
20.. (07�ϲ�)�������ڸ��ֽⷴӦ����
|
C��H2SO4+2NaOH====Na2SO4+2H2O������ D��CH4+2O2==== CO2+2H2O
21.(07�ϲ�)�±���¼������X����Һ�ֱ���뵽�����������ʵ���Һ�в���������������X�Ļ�ѧʽ������
| �������� | ̼���� | ʯ�� | |
| ����X | ���������� | �������� | ��Һ��� |
A��Ca(OH)2���������� �������� B��CuSO4 ���������� C��HCl������������ �� D��HCl
22.(07��)�������ʷ����ı仯������ijɷ��ص��ǡ����� ��
����A�������ڿ��������⡡������������������ B����ʯ���ڿ����б���
����C���ռ�����ڿ����г��⡢���ʡ��������� D��̼�����¶���ڿ�������������
23.(07��ͷ)����ͼ������ȷ��ӳ����Ӧ������ϵ����
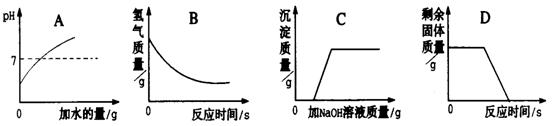 A����pH=3����Һ�в��ϼ�ˮ������������������ B��һ������ϡ������п����Ӧ
A����pH=3����Һ�в��ϼ�ˮ������������������ B��һ������ϡ������п����Ӧ
C����H2SO4��CuSO4���Һ�еμ�NaOH��Һ����D������һ��������ʯ��ʯ