08届高考化学复习模拟题三
说明:本套试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分120分.考试时间:90分钟.
可能用到的相对原子质量:C:12 H:1 O:16 Fe:56 Cl:35.5 S:32 Na:23
第Ⅰ卷(选择题,共64分)
一、选择题(本题包括16小题,每小题4分,共64分.每小题只有一个选项符合题意.)
1.目前排往大气中的二氧化碳逐年增加,下列各项叙述中,对人类影响最大的是( )
A.![]() 浓度增大,可提高粮食产量:
浓度增大,可提高粮食产量:

B.使石灰岩大量溶解而破坏自然景观、石雕和洞窟
C.使空气中氧气含量下降,导致人类窒息死亡
D.使地球温度升高,冰川融化,破坏生态平衡
2.下列叙述中,错误的是( )
A.某人根据卡车在起动或刹车时排出黑色废烟断定该车是以柴油为原料
B.相同物质的量的丙烷、甲烷、乙炔、乙烯燃烧时放出热量最大的是丙烷
C.味精的主要成分麸氨酸钠是易溶的,但麸氨酸锌是难溶的物质,所以大不宜大量食用味精
D.芳香族化合物一定有芳香气味
3.下列物质中,目前不可能制得的是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
4.10mLpH为2的硝酸溶液与100mL氢氧化钡溶液恰好完全反应,此时溶液的pH值为7,则氢氧化钡的pH值为( )
A.13 B.12 C.11 D.10
5.某温度下如下反应:![]()
![]()
![]() 在密闭容器中达到平衡,下列说法中正确的是( )
在密闭容器中达到平衡,下列说法中正确的是( )
A.降低温度,体积不变,![]() 的转化率降低 B.升高温度,加大压强,平衡都向正反应方向移动
的转化率降低 B.升高温度,加大压强,平衡都向正反应方向移动
C.温度不变,缩小体积,ClF的转化率增大 D.温度不变,增大体积,![]() 的产率提高
的产率提高
6.烟草中的剧毒物质尼古丁,其结构简式为: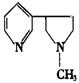 下列的有关叙述中正确的是( )
下列的有关叙述中正确的是( )
A.尼古丁分子中的C、N原子一定处于同一平面上
B.尼古丁分子中的六元环为正六边形
C.尼古丁分子中的六元环的一氯取代物有五种同分异构体
D.维生素![]()
 是尼古丁的氧化产物
是尼古丁的氧化产物
7.工业上制取硫酸铜不是直接用浓![]() 与铜反应,而是将铜丝浸入稀硫酸中,并不断地从容器底部吹入细小的空气泡,这样做的优点是( )
与铜反应,而是将铜丝浸入稀硫酸中,并不断地从容器底部吹入细小的空气泡,这样做的优点是( )
①不产生污染大气的![]() ②提高铜的利用率 ③节省能源 ④提高硫酸的利用率
②提高铜的利用率 ③节省能源 ④提高硫酸的利用率
A.①② B.①②④ C.②③④ D.全部
8.两种微粒含有相同的质子数和电子数,这两种微粒可能是①两种不同的原子;②两种不同元素的原子;
③一种原子和一种分子;④一种原子和一种离子;⑤两种不同分子;⑥一种分子和一种离子;
⑦两种不同阳离子;⑧两种不同阴离子;⑨一种阴离子和一种阳离子.( )
A.①③⑤⑥⑦⑧ B.①③④⑤⑦ C.①③⑤⑦⑧ D.全部都是
9.近年来,在许多城市街头发现不少公交车和出租车上印有“CNG”的标志,表示它们是以天然气作燃料的汽车.请回答:城市推行这一改革的主要目的是( )
A.延长发动机的寿命 B.促进地方经济的发展,增加再就业机会
C.节约能源 D.减少大气污染
10.下列关于物质的用途不正确的是( )
A.钠在冶金工业上可用作还原剂 B.过氧化钠可用作潜水时的供氧剂
C.芒硝在医药上可用作缓泻剂 D.纯碱是用来治疗胃酸过多的药剂
11.下列排列顺序中,错误的是( )
A.原子半径O<S<Na
B.稳定性:![]()
C.酸性:![]() D.碱性:
D.碱性:![]()
12.“绿色商品”是指对环境无污染的商品,下列商品不能称为绿色商品”的是( )
A.无铅汽油 B.无磷洗涤剂 C.无氟冰箱 D.无磺食盐
13.人体血液的pH为7.35~7.45,其中含有一对物质能抵御外来的少量酸或碱而保持pH基本稳定,这对物质可能是( )
A.NaCl―HCl B.![]() ―
―![]() C.NaOH―HCl D.
C.NaOH―HCl D.![]() ―NaCl
―NaCl
14.火箭起飞时,可以看到一级火箭的中部会冒出红棕色的气体,这是为了保证贮箱安全由保险活门自动开启所排出的部分高压氧化剂变化而来,所发生的变化是( )
A.![]()
![]() B.
B.![]()
![]()
![]()
C.![]() D.
D.![]()
15.1mol的钠、镁、铝与足量的稀硫酸反应,置换出氢气由多到少的顺序是( )
A.Na>Mg>Al B.Na>Al>Mg C.Mg>Na>Al D.Al>Mg>Na
16.在![]() 的反应中,当有6×6.02×
的反应中,当有6×6.02×![]() 个电子发生转移时,被氧化的氯原子与被还原的氯原子个数比为( )
个电子发生转移时,被氧化的氯原子与被还原的氯原子个数比为( )
A.6∶1 B.1∶6 C.5∶1 D.1∶5
第Ⅱ卷(非选择题,共56分)
二、(本题包括两小题,共20分)
17.(10分)实验室里有如下仪器和药品,请设计如下实验的操作步骤要点“○”可不填满),并指出可能发生的实验现象.
仪器或用品:①试管 ②烧杯 ③玻璃片 ④石棉网 ⑤滤纸
⑥火柴 ⑦镊子 ⑧酒精灯 ⑨药匙 ⑩集气瓶
药品:①金属钠(在煤油中) ②![]() 溶液 ③蒸馏水 ④细沙
溶液 ③蒸馏水 ④细沙
| 操作步骤要点 | 仪器代号 | 实验现象 | |
| 钠与氯化铝溶液反应 | ① | ① | |
| ② | ② | ||
| ○ | ○ | ||
| ○ | ○ | ||
| ○ | ○ | ||
| ○ | ○ |
18.(10分)某次测定硫酸铜晶体(![]() )中结晶水含量的实验记录如下:
)中结晶水含量的实验记录如下:
| 坩埚恒定质量
| (坩埚+硫酸铜晶体) 质量 | (坩埚+无水硫酸铜) 质量 |
| 15.0g | 17.4g | 16.6g |
(1)实验确定硫酸铜晶体的化学式为_________________________.
(2)假如每次实验的称量都是准确的,试从实验过程的操作分析,可能造成测定值比实际值偏小的原因(写出其中2点).
________________________________________________________;
________________________________________________________.
三、(本题包括两小题,共20分)
19.(10分)某有机物的相对分子质量为58,根据下列条件回答下列问题:
(1)若有机物只由碳、氢两种元素组成,则该有机物可能的结构简式为:
______________________________________________________________________________________.
(2)若为烃的含氧衍生物,且分子中有―![]() ,则可能的结构简式为:
,则可能的结构简式为:
______________________________________________________________________________________.
(3)若分子中无―![]() ,又无―OH,但能发生银镜反应,则结构简式为:
,又无―OH,但能发生银镜反应,则结构简式为:
______________________________________________________________________________________.
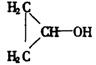
(4)分子中有―OH,无―C![]() C―,则结构简式为________________________________________________.
C―,则结构简式为________________________________________________.
20.(10分)下面是某研制人员为合成药物苯氟布洛芬所设计的线路:


回答下列问题:
(1)苯氟布洛芬的分子式为_____________;该分子最多有________个碳原子共平面.
(2)物质A、B的结构简式分别为:___________________,__________________.
(3)反应①~④中属于取代反应的是_________________________________________(填反应代号).
(4)写出反应③的化学方程式(有机物写结构简式): ____________________________________________.
四、(本题包括两小题,共16分)
21.(8分)由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲是电解质.

根据以上转化关系回答:
(1)写出下列物质的化学式:A________,B:________,乙:________,丁:________.
(2)组成A的元素在周期表中的位置是________,丙的电子式为_____________________________________.
(3)写出下列变化的方程式:
①A与NaOH溶液反应的化学方程式:_________________________________________________________.
②乙与过量的![]() 反应的离子方程式:________________________________________________________.
反应的离子方程式:________________________________________________________.
22.(8分)国家规定![]() 二级品中
二级品中![]() 质量分数不低于99%;三级品中
质量分数不低于99%;三级品中![]() 质量分数不低于98%,现称取样品0.500g,用适量蒸馏水充分溶解后,向其中加少量盐酸酸化,再加过量的KI溶液使其充分反应(化学方程式:
质量分数不低于98%,现称取样品0.500g,用适量蒸馏水充分溶解后,向其中加少量盐酸酸化,再加过量的KI溶液使其充分反应(化学方程式:![]() ),最后用0.100mol/L的标准
),最后用0.100mol/L的标准![]() 溶液滴定(化学方程式:
溶液滴定(化学方程式:![]() ),滴定到终点时用去18.17mL标准溶液,请回答:
),滴定到终点时用去18.17mL标准溶液,请回答:
(1)滴定中所用指示剂是________,终点现象是__________________________________________________.
(2)通过计算说明此样品属于哪一级产品?
参考答案
一、
1.D 空气中二氧化碳含量增加,给人类带来严重影响的是温室效应,严重破坏人类的生存环境.
2.D 卡车起动或刹车时,由于柴油分子中的碳原子较多,易在汽缸中发生不完全燃烧,产生碳粒而生成黑烟,碳原子和氢原子在燃烧中都产生大量热,由于丙烷的分子中含有的碳、氢原子比同分子中甲烷、乙烯、乙炔的含量都大,所以燃烧时放出的热量最多;由于麸氨酸锌难溶于水,多食味精易造成体内缺锌;芳香族化合物中只有少量的化合物有芳香气味.
3.D 氟是活泼的非金属元素,它可以与某些稀有气体,生成化合物如:![]() ;
;![]() ;
;![]() 等,而碳虽然是非金属但它的活泼性已远远不如氟,所以不能生成
等,而碳虽然是非金属但它的活泼性已远远不如氟,所以不能生成![]() .
.
4.C 两种溶液相混合后,混合溶液的pH为7,说明碱溶液中提供的氢氧根的物质的量和酸溶液中提供的氢离子的物质的量相等.![]() ,则
,则![]() ,根据n=Vc,则
,根据n=Vc,则![]() 根据
根据![]()
![]() 则
则![]() 溶液中的
溶液中的![]()
5.C 根据反应的特征,降低温度,缩小体积,均可使化学平衡向右移动,![]() 转化率升高C对.增大体积化学平衡向左移动
转化率升高C对.增大体积化学平衡向左移动![]() 的产率下降.D错;升高温度,将使化学平衡向左移动,而增大压强,将使化学平衡向右移动,所以升高温度,加大压强时,无法正确判断化学平衡的移动方向.B错;降低温度,化学平衡向右移动,
的产率下降.D错;升高温度,将使化学平衡向左移动,而增大压强,将使化学平衡向右移动,所以升高温度,加大压强时,无法正确判断化学平衡的移动方向.B错;降低温度,化学平衡向右移动,![]() 的转化率增大,A错.
的转化率增大,A错.
6.D 尼古丁分子中的五元环中的碳原子都是以单键与其它原子相连,它们都是四面体构型,而六元环的C、N在一平面上而与五元环上的C、N就不可在同一平面上;尼古丁分子的六元环有一个N原子,不是正六边形,且只有4个氢原子,所以六元环上的一氯取代物只有四种;若把尼古丁分子中的五元环看成一烃基,则被酸性的![]() 溶液氧化时,则该烃基被氧化成羧基,所以维生素
溶液氧化时,则该烃基被氧化成羧基,所以维生素![]() 是尼古丁的氧化产物,选D.
是尼古丁的氧化产物,选D.
7.B 两种方法中发生的化学反应如下:
与浓硫酸直接反应:![]()
与稀硫酸反应:![]() ;
;![]()
相比较可得出结论:①与稀硫酸反应省能源(不加热),②硫酸利用率高1倍,③无![]() 产生无污染,则选B.
产生无污染,则选B.
8.C 质子数和电子数相同的微粒的种类很多,如分子中有![]() 、
、![]() 、
、![]() 和Ne原子等,阳离子中有
和Ne原子等,阳离子中有![]() 、
、![]() 、
、![]() 等,阴离子中有
等,阴离子中有![]() ,
,![]() ,
,![]() ,
,![]() 等,原子中有
等,原子中有![]() ;
;![]() ;H、D、T等,答C.
;H、D、T等,答C.
9.D 使用天然气,能使气缸内的积炭减少,可延长发动机的寿命,甲烷因含碳量低,所以燃烧较完全,但空气中的![]() 和
和![]() 在放电时仍要产生氮的氧化物.所以,推行这一改革的主要目的是减少大气污染.
在放电时仍要产生氮的氧化物.所以,推行这一改革的主要目的是减少大气污染.
10.D 纯碱碱性太强,对口腔、咽有刺激.
11.B 原子的半r(O)<r(S),r(S)<(Na),A正确;同周期元素气态氢化物从左到右稳定性增强,故稳定性:![]() ,而同主族元素气态氢化物的稳定性从上到下逐渐减弱,故稳定性:
,而同主族元素气态氢化物的稳定性从上到下逐渐减弱,故稳定性:![]() ,B错误;同周期元素从左到右,其最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,C,D均正确.故本题答案为B.
,B错误;同周期元素从左到右,其最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,C,D均正确.故本题答案为B.
12.D
13.B 当在![]() 与
与![]() 混合溶液滴入少量酸,
混合溶液滴入少量酸,![]() 与
与![]() 结合生成
结合生成![]() 而溶液中
而溶液中![]() 基本不变.当滴入少量碱,
基本不变.当滴入少量碱,![]() 与
与![]() 作用生成
作用生成![]() ,而溶液中c(OH-)基本不变,故
,而溶液中c(OH-)基本不变,故![]() 与
与![]() 的混合液可抵御少量外来少量酸碱保持血液中的pH基本不变.
的混合液可抵御少量外来少量酸碱保持血液中的pH基本不变.
14.B 考察四个选项,因![]() 不是氧化剂,故排除A、C、D,选B.
不是氧化剂,故排除A、C、D,选B.
15.D Na、Mg、Al与硫酸反应的化学方程式如下:
![]()
![]()
![]()
由于述方程可知,当Na、Mg、Al为1mol时,产生的![]() 的物质的量之比为:
的物质的量之比为:![]() ,故答案为D.
,故答案为D.
16.C 此题关键要清楚氧化剂![]() 中+5价的氯在还原产物中的价态是0价,其反应情况如下:
中+5价的氯在还原产物中的价态是0价,其反应情况如下:
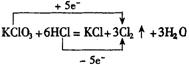
故答案为C.
二、
17.①用镊子取出钠后用小刀切取一小块 ②用滤纸吸干煤油 ③放入盛有![]() 的小烧杯中 ④盖上玻璃片 ②③⑤⑦
的小烧杯中 ④盖上玻璃片 ②③⑤⑦
①剧烈反应 ②熔成光亮的小球 ③四处游动并发出声响 ④浮在液面上 ⑤溶液中有白色絮状物生成 ⑥白色沉淀最后可能溶解(或减少)成无色溶液
18.(1)![]()
(2)①加热后,放在空气中冷却 ②两次称量的质量差超过0.1g就结束实验 ③蓝色硫酸铜晶体未完全变白就停止加热.
三、
19.(1)![]()
(2)
(3)![]()
(4)
20.(1)![]() 14
14
(2)![]()
(3)①③④
(4)

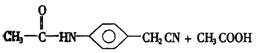
四、
21.(1)Al ![]()
![]()
![]()
(2)第三周期ⅣA族 ![]()
(3)①![]()
②![]()
22.(1)淀粉溶液 蓝色恰好消失
(2)![]()
