高一年级化学第一学期期中考试
高一年级化学试题
命题:邵群玲
本试卷分第Ⅰ卷(选择题,共54分)和第Ⅱ卷(非选择题,共46分)两部分,共100分,考试时间100分钟.
第Ⅰ卷(选择题 共54分)
可能用到的相对原子质量:H 1、 Li 7、 C 12、 N 14、 O 16、 Na 23、 S 32、 Cl 35.5
一.选择题(本题包括18小题,每小题3分,共54分。每小题只有一个选项符合题意)
1. 下列物质中既能导电,又属于强电解质的一组物质是
A. 石墨、醋酸溶液、食盐晶体 B. 熔融的KOH、NaCl、KCl
C. 稀H2SO4、NaOH溶液、稀HNO3 D. 氯水、石灰水、水银
2. 下列关于氧化还原反应的叙述正确的是
A.肯定有一种元素被氧化,另一种元素被还原
B.在反应中不一定所有元素的化合价都发生变化
C.置换反应和复分解反应不可能是氧化还原反应
D.化合反应和置换反应一定是氧化还原反应
3. 下列物质中,既能与NaOH溶液反应,又能与盐酸反应的是
A.Na2CO3 B. CuSO4 C. NaCl D. NaHCO3
4. 已知反应C+CO2=2CO是吸热反应,下列说法正确的是
A. CO的总能量大于C和CO2的总能量
B. C和CO2的总能量大于CO的总能量
C. C和CO2的总能量等于CO的总能量
D. 以上叙述都不对
5. 下列关于 Li、Na、k、Rb、Cs的叙述不正确的是
A. 它们的单质都能与水反应放出氢气
B. 它们的氧化物都溶于水生成ROH型化合物
C. 它们的氢氧化物的碱性随着核电荷数的递增而增大
D. 它们都能形成+1或+2价的离子化合物
6.钠与水反应时的现象与钠的下列性质无关的是
A. 钠的熔点低 B. 钠的密度小 C. 钠的硬度小 D. 有强还原性
7.将一小块钠投入盛5mL澄清石灰水的小烧杯里,不可能观察到的现象是
A. 钠熔成小球并在液面上游动 B. 有气体产生
C. 溶液底部有银白色物质生成 D. 溶液变浑浊
8.向紫色石蕊溶液中加入过量的Na2O2粉末振荡,可观察到的现象为
A.溶液仍为紫色 B.溶液最终变为蓝色
C.最终溶液褪色,而无其它现象 D.溶液中有气泡产生,溶液最终变为无色
9.下列关于Na2CO3和NaHCO3的性质的比较中,不正确的是
A.热稳定性Na2CO3>NaHCO3
B.常温下在水中的溶解度Na2CO3>NaHCO3
C.与稀盐酸反应的剧烈程度Na2CO3>NaHCO3
D.等质量的固体与足量盐酸反应放出CO2的质量Na2CO3<NaHCO3
10. 下列各组离子在酸性溶液中能大量共存的是
A.K+、Na+、CO32-、Cl- B.Na+、Cu2+、Cl-、SO42-
C.Ba2+、Cl-、K+、SO42- D.K+、Na+、Cl-、OH-
11.下列离子方程式正确的是
A.金属钠与水的反应:Na+2H2O=Na++2OH-+H2↑
B.石灰石与盐酸反应:CO32-+2H+=CO2+H2O
C.氢氧化钡溶液与稀硫酸反应:H++OH-=H2O
D.过量二氧化碳和石灰水反应 :CO2+OH-=HCO3-
12.已知离子反应:①2Fe3++2I-=2Fe2++I2 ②2Fe2++Cl2=2Fe3++2Cl- 判断下列物质的氧化能力由强到弱的顺序中正确的是
A.Cl2> Fe3+ >I2 B.Fe3+> Cl2> I2
C. I2> Cl2> Fe3+ D. Cl2> I2> Fe3+
13.与Na、Na2O、Na2O2、NaOH、Na2CO3、NaHCO3六种物质都能反应的是
A.H2O B.CO2 C.H2SO4 D.Ca(OH)2
14.下列各组物质及其用途的关系不正确的是
A.过氧化钠:供氧剂 B. 烧碱:治疗胃酸过多的一种药剂
C.小苏打:膨松剂的主要成分 D.纯碱:制玻璃、造纸
15.向含有Cl-、CO32-、HCO3-、OH-离子的溶液中加入一小块金属钠,反应后溶液中离子数目保持不变的是
A.CO32- B.Cl- C.OH- D.HCO3-
16.用光洁的铂丝蘸取某无色溶液,在无色火焰上灼烧时观察到火焰呈黄色,则下列有关叙述中正确的是
A.只有Na+ B.一定有Na+,也可能有K+
C.既有Na+,又有K+ D.可能含有Na+或K+的一种
17.将等质量的①Na、②Na2O、③Na2O2、④NaOH、⑤Na2CO3・10H2O露置于空气中,最后质量由小到大的顺序是
A.⑤<④<③<②<① B. ①<②<③<④<⑤
C. ⑤<④<②=③<① D. ⑤<③<④<②<①
18.2.3g金属钠与100g质量分数3.6%的稀盐酸充分反应后,溶液中的溶质为
A.只有NaOH B.只有NaCl C.NaOH和NaCl D.NaOH和HCl
第Ⅱ卷 (非选择题 共46分)
二、填空题(本题包括4小题,共34分)
19.(5分)试分析3NO2 + H2O = 2HNO3 + NO反应中化合价变化的关系,标出电子转移的方向与数目,指出 是氧化剂, 是还原剂,氧化剂与还原剂的质量比是 。
 20.(共15分)
20.(共15分)
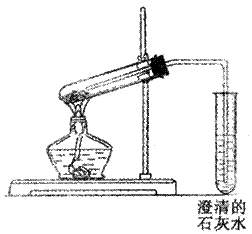
(Ⅰ).(5分)在实验室里常用加热法除去Na2CO3固体 中混有的少量NaHCO3。右图是某学生设计的装置图,请改正图中的错误,将改正结果填入表中:
| 改正结果 |
(Ⅱ).(10分)用(Ⅰ) 改正好的装置做分解NaHCO3的实验,主要实验步骤有:
①用酒精灯加热; ②熄灭酒精灯; ③检查装置气密性;
④在试管里加入NaHCO3固体; ⑤导管口撤离石灰水。
⑴正确的操作顺序为(填各操作的序号) 。
⑵在实验过程中,可观察到的现象为 。
⑶实验过程中发生反应的化学方程式为 。
⑷该实验证明了NaHCO3比Na2CO3的稳定性 (填“强”或“弱”)。
21.(6分)一瓶溶液里可能含有OH-、Cl-、NO3-、CO32-和SO42-五种阴离子中的某几种。现分别取该溶液少量装入两支试管,进行以下实验:
①向第一支试管中滴加酚酞试液,溶液变红。
②向第二支试管中滴加足量的硝酸钡溶液,生成白色沉淀。过滤并将滤液移入第三支试管,在沉淀中加入稀硝酸,沉淀逐渐消失并有无色无味气体产生,该气体通入澄清石灰水,石灰水变浑浊。
③向第三支试管中加入少量硝酸银溶液,无现象。
⑴通过以上实验可以判断溶液中含有的离子为 ,不含有的离子为 。
⑵写出实验②中有关反应的离子方程式。
![]()

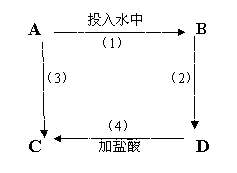 22.(8分)已知A为单质,B、C、D为含A元素的三种
22.(8分)已知A为单质,B、C、D为含A元素的三种
不同的化合物, 用铂丝蘸取B、C、D的溶液进行焰
色反应,都呈黄色。按如图转化关系,写出有关化学
反应方程式:
⑴
⑵
⑶
⑷
三、计算题(12分)
23.(6分)有氧化钠和过氧化钠的混合物5g,投入到95g水中,生成0.80g气体。计算:
⑴混合物中过氧化钠的质量是多少克?
⑵所得溶液中溶质的质量分数为多少?
(说明:计算结果小数点后保留两个有效数字,写出计算过程)
24.(6分)在一定条件下,使H2和O2的混合气体26g充分反应后,将所得产物在适当温度下跟足量的固体Na2O2反应,使固体增重2g。求原混合气体中H2和O2的质量?
高一年级化学试卷
班级 姓名 分数
一.选择题(本题包括18小题,每小题3分,共54分。每小题只有一个选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | |||||||||
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
| 改正结果 |
二、填空题(本题包括4小题,共34分)
19.(5分)电子转移的方向与数目表示为:3NO2 + H2O = 2HNO3 + NO
, , ,
20.(共15分)
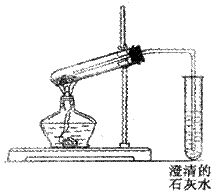 (Ⅰ).(5分)
(Ⅰ).(5分)
(Ⅱ).(10分)
(1) ;
(2) ;
(3) 、
;
(4) 。
21.(6分)
(1) 、 ;
(2)
22.(8分)
![]()

 ⑴
⑴
⑵
⑶
⑷
三、计算题(12分)
23.(6分)有氧化钠和过氧化钠的混合物5g,投入到95g水中,生成0.80g气体。计算(计算结果小数点后保留两个有效数字,写出计算过程):
⑴混合物中过氧化钠的质量是多少克?
⑵所得溶液中溶质的质量分数为多少?
24.(6分)在一定条件下,使H2和O2的混合气体26g充分反应后,将所得产物在适当温度下跟足量的固体Na2O2反应,使固体增重2g。求原混合气体中H2和O2的质量?