高一化学第一学期期中考试卷
高一化学
(90分钟 100分)
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 S—32 Cl—35.5
第Ⅰ卷 (选择题 共48分)
一、选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意。)
1.实验室中的药品常按物质的性质、类别等有规律地放置。做“酸的性质”实验时,实验桌上部分药品的摆放如下图。某同学取用KOH溶液后,应把它放回的位置是( )
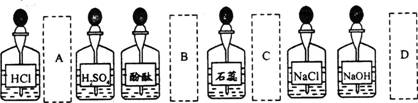
2.下列实验操作中错误的是 ( )
A. 用规格为10mL的量筒量取6mL的液体
B. 用药匙或者纸槽把粉末状药品送入试管的底部
C. 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D.如果没有试管夹,可以临时手持试管给固体或液体加热
3.已知HClO是弱酸,在水溶液中只部分电离。新制氯水中微粒(离子、分子)的种类有( )
A.8种 B.7种 C.6种 D.5种
4.摩尔是
A.国际单位制的一个基本物理量 B.表示物质质量的单位
C.计量微观粒子的物质的量的单位 D.表示6.02×1023个粒子的集体
5.胶体分散系与其它分散系的本质差别是( )
A.分散质直径大小 B.是否有丁达尔现象
C.是否稳定 D.分散质粒子是否带电
6.下列反应肯定不属于氧化还原反应的是( )
A.化合反应B.分解反应C.置换反应D.复分解反应
7.用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1 NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl- 个数为1 NA
8.对于相同物质的量的SO2和SO3,下列说法中正确的是( )
A.硫元素的质量比为5∶4 B.分子数之比为1∶1
C.原子总数之比为4∶3 D.质量之比为1∶1
9.下列化合物在溶液中不能与氯气反应的是( )
A.KF B. NaBr C. KI D. NaOH
10.用简便的方法鉴别硫酸铜、碳酸钠、氢氧化镁三种白色固体粉末,应选用的试剂是( )
A.稀盐酸 B。紫色石蕊试液
C.水 D。氢氧化钠溶
11.同温同压下,等质量的下列气体所占有的体积最大的是
A.O2 B.CH4 C.CO2 D.SO2
12.下列关于Na和Na+的叙述中,错误的是
A.它们相差一个电子层 B.它们的化学性质相似
C.钠原子,钠离子均为同一元素 D.灼烧时,它们的焰色反应都呈黄色
13.下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是( )
A.150 mL 1 mol·L-1的NaCl溶液 B.75 mL 2 mol·L-1 NH4Cl溶液
C.150 mL 2 mol·L-1的KCl溶液 D.75 mL 1 mol·L-1的FeCl3溶液
14.放射性同位素![]() I可用于治疗肿瘤。该同位素原子核内的中子数与核外的电子数之差是( )A
I可用于治疗肿瘤。该同位素原子核内的中子数与核外的电子数之差是( )A
A.72 B.19 C.53 D.125
15.下列化合物中,不能通过单质间化合直接制取的是 ( )
A.HCl B.CuCl2 C.FeCl2 D.Fe3O4
16.在KClO3+6HCl KCl+3Cl2↑+3H2O中,被氧化与被还原的氯原子个数比为( )
A.1:6 B.6:1 C.1:5 D.5:1
第Ⅱ卷(非选择题 共52分)
二、填空题(本题包括3小题,共22分。)
17、(6分)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2↑+CO2↑。其中被还原的元素是 ,被氧化的元素是 ,氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 。
18、(6分)483g Na2SO4·10H2O中所含的Na+的物质的量是 和SO42—的物质的量是 ,所含H2O分子的数目是 个。
19、(10分)下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3
(1)以上四组物质中与别不同的物质依次是(填化学式)A ;B ;C ;D 。
(2)这四种物质相互作用可生成一种新物质(碱式碳酸铜,化学式Cu2(OH)2CO3),该反应 氧化还原反应(填“是”或“否”)。
三、实验题(每空2分,共22分。)
20. (8分)实验室配制0.5mol·L-1的NaOH溶液500mL,有以下仪器:
①烧杯 ②胶头滴管 ③1000mL容量瓶 ④500mL容量瓶 ⑤玻璃棒
⑥托盘天平(带砝码) ⑦酒精灯
(1)配制时,必须使用的仪器有 (填代号)
(2)该实验两次用到玻璃棒,其作用分别是 、
(3)配制时一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④转移 ⑤洗涤
⑥定容 ⑦摇匀 ⑧冷却
其正确的操作顺序为②①③
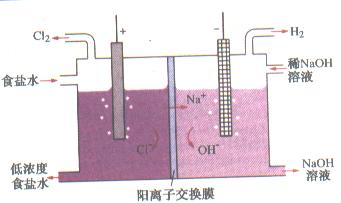 21、(6分) 右图是工业电解饱和食盐水的装置,在阴极(与电源负极相连的电极)产生的是______,阳极(与电源正极相连的电极)产生的是________,反应原理是(用化学方程式表示)___________________________________。
21、(6分) 右图是工业电解饱和食盐水的装置,在阴极(与电源负极相连的电极)产生的是______,阳极(与电源正极相连的电极)产生的是________,反应原理是(用化学方程式表示)___________________________________。
22、(8分) 选择下列实验方法分离物质,将分离方法的序号填在横线上。A.萃取分液B.升华C.结晶D.分液 E.蒸馏 F.层 析 G.过滤
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
四、计算题(共8分)
23、实验室常用盐酸的溶质质量分数为36.5%,密度为1.20g/㎝3。
⑴此浓盐酸的物质的量浓度是多少?(列式计算)
⑵配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL ?(列式计算)
⑶用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填写序号): 。
①计算 ②装瓶③用50 mL量筒量取一定体积的浓盐酸④洗涤⑤移液⑥稀释⑦定容⑧摇匀
附加题、(5分) 在25℃、l0lkPa条件下,将15L O2通入10L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气中: V(CO)=___________L,V(H2)=____________L。
(2)若剩余气体的体积为aL,则原CO和H2的混合气中: V(CO):V(H2)=___________________。
(3)若剩余气体的体积为aL,则a的取值范围是___________________________
高一年级化学试卷答题卷
一.请把正确答案填入对应题号中(48分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | ||||
| 答案 |
二.填空题(22分)
17、________;________;________;________ ;_______ ;________ 。
18、________;________;________.
19、(1)A______;B______;C______;D_______。(2)______。
三.实验题(22分)
20、(1)_______________;(2)_________;_________; (3)_____________。
21、_______ 、_______ 、______________________________。
22、(1)_____(2)_____(3)_____(4)_____。
四.计算题(8分)
23、实验室常用盐酸的溶质质量分数为36.5%,密度为1.20g/㎝3。
⑴此浓盐酸的物质的量浓度是多少?(列式计算)
⑵配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL ?(列式计算)
⑶用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填写序号): 。
①计算 ②装瓶③用50 mL量筒量取一定体积的浓盐酸④洗涤⑤移液⑥稀释⑦定容⑧摇匀
附加题、(5分) 在25℃、l0lkPa条件下,将15L O2通入10L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气中: V(CO)=___________L,V(H2)=____________L。
(2)若剩余气体的体积为aL,则原CO和H2的混合气中: V(CO):V(H2)=___________________。
(3)若剩余气体的体积为aL,则a的取值范围是___________________________。
宁波至诚高中第一学期期中考试高一年级化学试卷参考答案
一.选择题(每小题3分,共同体48分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | D | D | B | C | A | D | B | B | A | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | B | B | D | B | C | D |
二.填空题(共22分)
17、氮和硫;碳;KNO3和硫;碳 ;CO2 ;K2S和NO2 。(每空1分)
18、3mol 1.5mol 15NA (每空2分)
19、(1)A CO2;BCu;CO2 ;DH2O。(2)是 (每空2分)
三.实验题(共22分)(每空2分)
20、(1)①②④⑤⑥ ; (2)搅拌、 引流 ; (3)⑧④⑤⑥⑦
21、氢气 、氯气功 、2NaCl + 2H2O = 2NaOH + H2↑+ Cl2↑
22、(1)G (2)C (3)D (4)E
四.计算题(8分)
23、(1)C=1000×1.20×36.5%÷36.5=12.0mol/L (3分)
(2)设需浓盐酸XmL
100mL×3.00mol/L= 12.0mol/L·X
X=25 mL (3分)
(3) ①③⑥⑤④⑦⑧② 。(2分)
附加题:(5分)
(1)。V(CO):5L ; V(H2):5L 。 (2分)
(2)。V(CO)/V(H2):(a-10)/(20—a) (1.5分)
(3)。a的取值范围是:10<a<20 (1.5分)