高一化学上学期期末模拟试题
命题人:邵明升
可能用到的数据:H―1 C―12 O―16 S―32 N―14 Na―23 Mg―24 Al―27 Fe―56 Ag―108 K―39 Ca―40 Cl―35.5
第Ⅰ卷(共44分)
一、 选择题(本题包括22个小题,每题只有1个选项符合题意,每题2分,共44分)
1、下列反应中,属于有水参加的氧化还原反应、且水只做氧化剂的是 ( )
A.![]() B.
B.![]()
|
2、自然界里常见金属元素存在最多的是Al,其次是铁,铜的含量较少。然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来,究其原因,合理的是 ( )
A.矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发
B.铜矿颜色较深,易发现,铝矿颜色较浅,不易发现
C.铜矿较易还原,铝矿很难还原
D.以上说法是错误的
3、把碘从碘水里分离出来,有下列基本操作:①静置后分液 ②充分振荡 ③把碘水倒入分液漏斗,再加入萃取剂四氯化碳。其正确的操作顺序是
A.①②③ B.③②① C.②③① D.③①②
4、下列物质中属于电解质的是 ( )
① KOH ② CuSO4 ③ Al ④HCl ⑤ 蔗糖
A.①② ③ B.②③④ C.③④ D.①②④
5、电影《闪闪的红星》中,为让被困的红军战士吃上食盐,潘冬子将浸透食盐水的棉袄裹在身上,带进山中……假如潘冬子在实验室中,欲从食盐水中提取出食盐,最好采用的 方法是 ( )
A.过滤 B.萃取 C.蒸发 D.蒸馏
6、2005年3月,京沪高速公路淮安段一辆载有约35吨液氯的槽罐车与一辆货车相撞,导致槽罐车中液氯大面积泄漏,造成多人伤亡。下列处理方法和过程合理的是 ( )
A.将人群转移到地势较低的地方,等待营救
B.将槽罐车推入附近的水塘中,撒上石灰
C.用高压水枪向空中喷洒大量浓氨水溶液
D.被转移人群可戴上用NaOH处理过的口罩
7、如果你家里的食用花生油混有水份,你将采用下列何种方法分离 ( )
A.过滤 B.蒸馏 C.分液 D.萃取
8、下列反应一定属于氧化还原反应的是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
9、下列事实与胶体性质无关的是 ( )
A.纳米科技的发展有赖于胶体化学原理与方法
B.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
C.一束平行光线照射豆浆时,可看到光亮的通路
D.万里长江流入大海处,形成长江三角沙洲
10、下列气体不能用排水集气法收集的是 ( )
A .NO B .NH3 C .O2 D.CO
| 选项 | A | B | C | D |
| 试剂 | 氯水 | 氢氧化钠溶液 | 铁屑 | KSCN溶液 |
| 现象 | 出现黄褐色 | 生成红褐色沉淀 | 绿色加深 | 有较浅的血红色 |
11、实验室有一瓶购置时间较长绿矾(FeSO4•7H2O),老师将其交给化学研究小组某同学检验药品是否有变质现象,这位同学取绿矾做了简单的检验,得出的结论是:已经开始氧化。该同学所用的试剂和判断依据是 ( )
12、下列各组中的离子,能在溶液中大量共存的是 ( )
A. H+ Na+ CO32- Cl- B. Ba2+ Na+ Cl- SO42-
C. K+ H+ SO42- OH- D . Ag+ Al3+ NO3- H+
13、下列离子方程式书写正确的是 ( )
A.C12与氢氧化钠溶液反应 C12+2NaOH==2Na++C1-+ClO-+H2O
B.二氧化硅与氢氧化钠溶液反应 SiO2+2OH-=SiO32-+H2O
C.大理石与盐酸反应 CO32-+2H+ ==H2O+CO2↑
D.氯化铁溶液与铁单质反应 Fe3++Fe ==2Fe2+
14、等质量的铜分别与足量浓硫酸、稀硝酸充分反应,下列说法正确的是 ( )
A.被还原的酸的物质的量相等 B.被氧化的铜的物质的量硝酸多
C.提供H+ 的酸的物质的量相等 D.转移电子的物质的量相等
15、下列化合物不能由单质直接化合得到的是 ( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D.![]()
16、下列四组溶液中每组都是三种,其中可用稀硫酸进行鉴别的是 ( )
A.BaCl2溶液 Ba(NO3)2溶液 NaCO3溶液
B.NaCO3溶液 BaCl2溶液 NaCl溶液
C.Ba(NO3)2溶液 KCl溶液 MgCl2溶液
D.NaCO3溶液 K2CO3溶液 NaCl溶液
17、下列变化中,必须加入氧化剂才能发生的是 ( )
A.SO2→S B.SO32―→SO2 C.I―→I2 D.HCO3―→CO32―
18、某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
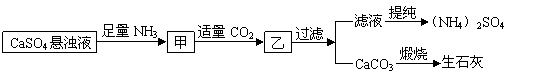 |
下列推断不合理的是 ( )
A.直接蒸干滤液得到纯净的(NH4)2SO4
B.生成1mol(NH4)2SO4至少消耗2molNH3
C.CO2可被循环使用
D.往甲中通CO2有利于(NH4)2SO4生成
19、下列说法不正确的是 ( )
A.大量使用的不是纯金属而是它们的合金
B.目前已制得的纯金属只有90多种,但制得的合金已达几千种
C.钢是最纯的铁
D.废弃铝质包装既浪费金属材料又造成环境污染
20、下列有关实验的做法,正确的是 ( )
A.实验完毕自由离开实验室,想做实验随便进入实验室
B.不慎将酸溅到眼中,应立即用清水冲洗,边洗边眨眼睛
C.洒出的酒精在桌上燃烧起来,立即用干抹布扑盖
D.不报告老师随意增加别的实验,随便动用仪器、药品及其他实验材料
21.某同学用一小块铝片和盐酸反应制取H2,实验现象如下表:
| 时间 | 1 min | 2 min | 5 min | 15 min | 20 min |
| 现象 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
反应1~15min内,铝与盐酸的反应速率变化的可能原因是 ( )
A.该反应是放热反应,温度升高 B.反应过程中盐酸的浓度增大
C.随着反应的进行,铝片表面积变小 D.Cl-离子是该反应的催化剂
22.下列各组物质发生反应后,能生成盐和O2的是 ( )
A.Na和H2O B.Na2O和H2O
C.Na2O2和H2O D.Na2O2和CO2
第Ⅱ卷(共56分)
二、填空题 (每空2分,共12分)
23、(1)实验室盛装氢氧化钠的试剂瓶用橡皮塞而不用玻璃塞,这是为了防止发生反应:(用化学方程式表示) ,而使瓶塞和瓶口粘在一起。
(2)、红热木炭和浓硫酸反应的化学方程式 ,
浓硫酸的作用是 ,氧化剂与还原剂的物质的量之比 。
(3)、某溶液与碱共热,有无色、刺激性气味的气体发出,该气体使湿润的红色石蕊试纸变蓝,该溶液一定含有 ,写出该反应的离子方程式:
三、推断题(12分)
24、下列各物质均是中学化学中常见的物质.室温下,A、B、C为单质,且B在常温下为气体,A为固体,在一定条件下,它们可以按框图进行反应(有些反应条件已知略去)。又知D、E 、F为化合物且D为固体,请按要求回答下列问题:
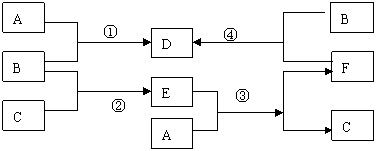
(1)A元素是____ B是 (化学式)
(2)若C是非金属,指出C在工业生产中的一种应用(用化学方程式表示)
。
若C是金属,C早在古代就可以通过湿法进行冶炼,则C是 (化学式)
(3)写出反应④的离子方程式为:
(4)写出实验室用一种黑色粉末制取气体B的离子方程式:
。
四、实验题(本题包括两个小题,共20分)
25、(13分)在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:
(填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物
是
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号
及实验中观察到的现象。
| 同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | ||
| 第二种方法 |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子
是 若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,
你认为是否可行? 理由是:
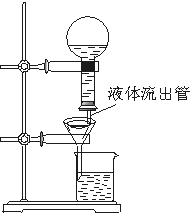 26、(7分)某学生为了使过滤操作能自动添加液体,设计
26、(7分)某学生为了使过滤操作能自动添加液体,设计
了“自动加液过滤器”,如图所示。在倒置的烧瓶中盛放
待过滤的液体,液体从“液体流出管”流入漏斗。为使液
体顺利流下,还需插入“空气导入管”与大气相通。
(1)“空气导入管”下口应在____ ,上口应在_______ 。
A.滤纸边沿下方 B.滤纸边沿上方
C.待过滤液液面上 D.待过滤液中
E.A和B项均可 F.C和D项均可
(2)试简要说明自动加液过滤的原理。
五、计算题(12分)
27、某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,化学原理为:
2FeCl3+Cu=2FeCl2+CuCl2
某化学研究性学习小组的甲、乙、丙三位同学为分析该厂生产印刷电路后所得废液(记为A)的组成,各取50.0mL A进行实验,结果如下:
| 甲 | 向50.00mL A中加入足量的AgNO3溶液,析出沉淀43.05 g |
| 乙 | 向50.00mL A中试探性的加入0.70 g铁粉,结果全部溶解未见固体析出 |
| 丙 | 向50.00mL A中加入20.0 mL稀硝酸,产生0.224L NO(标准状况) |
结合三位同学实验提供的信息,请回答下列问题:
(1)该厂所使用的FeCl3溶液的物质的量浓度(反应前后溶液的体积变化忽略不计)
(2)A中c(Cu2+)的取值范围: _________________________。
(3)若向乙同学实验后的溶液中加入足量的稀硝酸,结果生成0.56L NO(标准状况),则A中Cu2+的物质的量浓度为________________________。
本学期期末诊断试题参考答案
一、选择题(每小题2分,共44分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| D | C | B | D | C | B | C | C | B | B | D |
| 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| D | B | D | D | B | C | A | C | B | A | D |
二、填空题(每题2 分,共12分)
23、(1)SiO2+2NaOH===Na2SiO3+2H2O
(2)、C+2H2SO4===CO2+2SO2+2H2O;氧化剂;2:1。
(3)、NH4+; NH4++OH-△NH3+H2O
三、推断题(每空2分,共12分)
24、(1)Fe ;Cl2
(2)写出用氢气冶炼金属或作为能源的方程式均可 Cu
(3)2Fe2++ Cl2=2Fe3++ 2Cl- (4)MnO2+4H+=Mn2++Cl2↑+2H2O
四、实验题
25、(1)Br2(2分);Fe3+(2分)
(2)
| 乙 (1分) 同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | C(1分) | 有机层无色(1分) |
| 第二种方法 | D(1分) | 溶液变红(1分) |
(3)Fe2+(2分);不可以,因为Br2和Fe3+都能把I―氧化成I2(2分)
26、解析:(1)若“空气导入管”的下口在滤纸边沿上方,则待过滤液体的液面高于滤纸,会使部分待滤液不经过滤纸而沿滤纸与漏斗间的间隙流下,起不到过滤作用,故“空气导入管”下口应在滤纸边沿下方。若“空气导入管”的上口接在待过滤液中,则此管会有液体流下,不能使内外气体相通,起不到自动加液的作用。(2)待过滤的液体沿液体流出管流入漏斗,当漏斗中的液面封住空气导入管的下口时,空气停止进入烧瓶,液体不再流入漏斗;随着过滤的进行,当漏斗里的液面降到空气导入管的下口以下时,空气又进入烧瓶,液体又流入漏斗。
(1)A(2分) C(2分)
(2)待过滤的液体沿液体流出管流入漏斗,当漏斗里的液面封住“空气导入管”的管口时,空气停止进入烧瓶,液体停止流入漏斗;随着过滤的进行,当漏斗里的液面降到空气导入管的下口以下时,空气又进入烧瓶,液体又流入漏斗。(3分)
27、(12分)(1)2mol/L (4分)
(2) 0.30 mol≤ c(Cu2+)≤0.75 moL(4分) (3)0.375 mol/L(4分)