高一化学必修①期中教学质量诊断试卷
期中考试化学试卷
(考试时间:90分钟 满分:100分)
命题人:厦门英才学校高一化学备课组
第Ⅰ卷 ( 选择题)
解题可能要用的相对原子质量:H:1 O: 16 C: 12 N: 14
Cl: 35.5 S: 32 Na:23 Al: 27 Mg: 24 Zn:65
一、选择题:(以下各题均只有一个答案符合题意。本大题共有道17小题,每小题3分,共51分)
1、下列物质中属于氧化物的是( )
A、O2 B、Na2O C、NaClO D、FeSO4
2、根据厦门气象台报道,近年每到春季,厦门市经常出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的( )
A、溶液 B、悬浊液 C、乳浊液 D、胶体
3、下列反应中必须加入还原剂才能进行的是
A、Cl2→Cl- B、Zn→ Zn2+ C、H2→H2O D、CuO→CuCl2
4、将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是( )
A、冷水 B、沸水 C、NaOH溶液 D、NaCl溶液
5、某溶液中只含有Na+, Al3+,Cl-,SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为( )
A、1:2 B、1:4 C、3:4 D、3:2
6.能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可以加热)( )
A.BaCl2 B.NaOH C.Ba(OH)2 D.AgNO3
7、从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
A、2NaBr+Cl2=2CaCl+Br2
B、AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
C、2H2S+SO2=2H2O+3S↓
D、C+H2O![]() CO+H2
CO+H2
8、在下列反应中, HCl 作氧化剂的是( )
A、NaOH+HCl=NaCl+H2O
B、Zn+2HCl=ZnCl2+H2↑
C、MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D、CuO+2HCl=CuCl2+H2O
9、如果你家里的食用花生油混有大量水份,你将采用下列何种方法分离( )
A.过滤 B.蒸馏 C.分液 D.萃取
10、下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
11、下列叙述正确的是( )
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
12、已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
A.16g B.32g C.64g /mol D.32g /mol
13、科学家已发现一种新型氢气分子,其化学式为H3,在标况下,等质量的H3和H2相同的是( )
A.原子数 B.分子数 C.体积 D.物质的量
14、标准状况下,等质量的下列气体所占有的体积最大的是( )
A.O2 B.CH4 C.CO2 D.SO2
15、用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,溶有1.06g Na2CO3的溶液中含有的Na+离子数为0.02 NA
C.通常状况下,1 NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol・/L的MgCl2溶液中,含有Cl- 个数为1 NA
16、根据元素的核电荷数,不能确定的是( )
A.原子核内质子数 B.原子核内中子数
C.原子最外层电子数 D.原子核外电子数
17、据报载我国最近合成了多种元素的新的同位素,其中一种是![]() (铪),它的中子数是( )
(铪),它的中子数是( )
A.72 B.113 C.185 D.257
 厦门市集美区2006年11月《化学必修①》期中教学时段教学质量诊断
厦门市集美区2006年11月《化学必修①》期中教学时段教学质量诊断
高一化学期中考试化学试卷
(考试时间:90分钟 满分:100分)
| 题 序 | 一 | 二 | 三 | 四 | 五 | 总 分 |
| 得 分 |
|
|
|
|
|
|
| 评卷人 |
|
|
|
|
|
|
第Ⅱ卷 (非选择题)
一、请把第Ⅰ卷答案填入下列空格内(每小题3分,共51分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
|
|
|
|
|
|
|
|
|
|
| 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
|
|
|
|
|
|
|
|
|
|
|
二、填空题:(本大题共有3道小题,共23分)
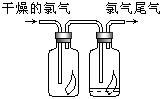 18、(8分)(1)如图所示,将氯气依次通过盛有干燥红色布条的广口瓶和盛有潮
18、(8分)(1)如图所示,将氯气依次通过盛有干燥红色布条的广口瓶和盛有潮
湿红色布条的广口瓶,可观察到的现象是 ________________。
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用 溶液吸收多余的氯气,原理是(用化学方程式表示)
________ _______。
(3)根据上述原理,工业上常用廉价的石灰乳吸收氯气制得漂白粉,漂白粉的有效成分是次氯酸钙,已知次氯酸钙会和盐酸、碳酸等酸性物质反应生成次氯酸而显漂白性,故长期露置于空气中的漂白粉会失效。漂白粉失效的化学方程式是
19、(7分)请填写下列物质的化学式并按物质组成分类法填写物质类别
| 名称 | 生石灰 | 硫酸铜 | 氖 气 | 氯化铁 | 氢氧化铝 |
| 化学式 | CaO | Ne | |||
| 类别 | 碱 |
20、(8分)选用下列物质:氯气、铁、溴化钾溶液、氢氧化钠溶液,写出符合下列要求的化学方程式。并请标出(1)电子转移的方向与数目。
⑴一种单质氧化另一种单质 。
⑵一种单质氧化溴化钾溶液中的阴离子 。
⑶氯气在反应中既是还原剂又是氧化剂:
三、实验题:(本大题共有2道小题,共10分)
21、(4分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液 B.升华 C.蒸发结晶过滤 D.分液
E.蒸馏 F.层 析 G.溶解过滤
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾.
(3)______分离水和汽油的混合物
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
22、(6分)实验室配制0.5mol・L-1的NaOH溶液500mL,有以下仪器:
①烧杯 ②胶头滴管 ③1000mL容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦酒精灯
(1)配制时,必须使用的仪器有 (填代号)
(2)该实验两次用到玻璃棒,其作用分别是 、
(3)配制时一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④转移 ⑤洗涤 ⑥定容 ⑦摇匀 ⑧冷却
其正确的操作顺序为②、①、③、 、 、 、 、 、
四、选做题:(8分)[一级达标校学生解答23(A);其它学校学生解答23(B)]
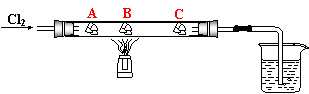
23(A)、(8分)某研究性学习小组设计了如下图所示的实验,以此来验证氯、溴、碘三种卤素单质的氧化性顺序。图中A、 B、 C分别是浸有饱和溴化钠溶液、饱和碘化钾溶液、淀粉水溶液的棉球,烧杯D中盛有氢氧化钠溶液。实验时从左端导管口缓慢通入氯气,待A处出现明显现象而B没有变化时,停止通入氯气, 再依次对A、B棉球进行加热。请利用资料卡片提供的信息,结合所学知识,完成下列问题:
D
资料卡片
| 卤素 单质 | 颜色和状态 | 蒸气颜色 | 在水中的溶解度 | 水溶液的颜色 | 熔点 /℃ | 沸点 /℃ |
| Cl2 | 黄绿色气体 | 黄绿色 | 从Cl2→I2在一定量水中溶解的物质的量逐渐减少 | 淡黄绿色 | -101 | -34.6 |
| Br2 | 深红棕色液体 | 红棕色 | 橙红色 | -7.2 | 58.78 | |
| I2 | 紫黑色固体 | 紫色 | 黄褐色 | 113.5 | 184.4 |
(1)棉球A的现象:
(2)棉球B上反应的化学方程式:
若反应中有0.1mol的电子转移,被氧化的物质的物质的量是
(3)棉球C的现象:
23(B)、(8分)厦门市集美区某企业的一个储氯罐某日发生液氯泄漏事故,如果你是该企业管理者,又恰好在现场,你当如何处置?(至少答出四点合理的处置意见)
五、计算题(8分)
24、(8分)将3.25g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:(1)反应中生成的H2在标准状况下的体积
(2)所用盐酸中HCl的物质的量浓度。
高一化学期中考试试卷
参考答案及评分标准
一、填空题:(51分) 每题3分,凡多答、漏答、错答均不得分。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| B | D | A | B | A | C | C | B | C |
| 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
|
| D | C | D | A | B | B | B | B |
|
二、填空题:共23分
18、(8分) (1)干燥的布条不褪色(1分),湿润的布条红色褪去(1分)
(2)NaOH 或答 碱性 或答成其它合理答案(2分)
原理:2NaOH+Cl2==NaCl+NaClO+H2O (2分)
![]() (3)Ca(ClO)2 + CO2 + H2O ====CaCO3
+ 2HClO (2分)
(3)Ca(ClO)2 + CO2 + H2O ====CaCO3
+ 2HClO (2分)
凡化学式写错的不得分,未配平的得1分
19、(共7分) 每空1分
| 名称 | |||||
| 化学式 | CuSO4 | FeCl3 | Al(OH)3 | ||
| 类别 | 氧化物 | 盐 | 单质 | 盐 |
20、(8分) 每小题2分,化学方程式(2分)电子转移的方向及数目(2分)
![]()
![]()
![]() 6e-
6e-
(1)
2Fe + 3Cl2 =![]() ==== 2FeCl3
==== 2FeCl3
(2) Cl2 + 2KBr ==== 2KCl + Br2
![]() (3) Cl2 + 2NaOH ==== NaCl + NaClO
+ H2O
(3) Cl2 + 2NaOH ==== NaCl + NaClO
+ H2O
21、(4分) (1) G (2) C (3) D (4) E (每空1分)
22、(6分) (1) ①②④⑤⑥ (2) 搅拌溶解 (1分)、 引流移液(1分)
(3)⑧④⑤⑥⑦ (每空2分)
四、选做题(8分)
23、(A)(1)白色棉花逐渐变为橙红色;加热产生红棕色气体。
(2)2KI + Br2 ===== 2KBr + I2 0.1 mol
(3)白色棉球逐渐变成蓝色 (每空2分)
23、(B) (1) 指挥现场人员到各车间紧急疏散员工;
(2) 联系周边的街道做好人员转移的准备
(3)让所有非现场抢修人员用湿布(蘸取纯碱溶液)捂住口鼻,逆风转移到上风口地势较高处;
(4) 指挥现场抢修人员戴上防毒面具,用高压水枪向储氯罐及空中喷洒稀碱液并设法堵住氯气泄漏口;
(5)及时拨打电话119,请求帮助,并及时向上级有关部门汇报;
(每条2分,答对4条给满分8分。其它合理答案酌情给分)
五、计算题(8分)
解:3.25gZn的物质的量为:3.25g/65g.mol-1 ==0.05mol (2分)
![]() Zn
+ 2HCl ==== ZnCl2 + H2
Zn
+ 2HCl ==== ZnCl2 + H2
1mol 2mol 22.4L
0.05mol 200×10-3L×C(HCl) V(H2) (2分)
0.05mol×22.4L
![]() (1)、V(H2)==
== 1.12L
(2分)
(1)、V(H2)==
== 1.12L
(2分)
1mol
2mol×0.05mol
![]() (2)、C(HCl)==
==0.5mol・L-1
(2分)
(2)、C(HCl)==
==0.5mol・L-1
(2分)
1mol×0.2 L
答:标准状况下生成氢气1.12L;盐酸中氯化氢的物质的量浓度为0.5mol・L-1
其他合理的解法,可参照此标准给分。