高一化学上学期半期考试题
高 一 化 学 试 卷
(完卷时间:90分钟 满分:100分)
本卷可能用到的相对原子质量:
H:1 C:12 O:16 S:32 Mg:24 Na:23
一、选择题(每小题只有一个选项正确,每题2分,共44分)
1、下列物质中属于电解质的是( )
A.铁 B.酒精 C.食盐水 D.氢氧化钾
2、下列物质中,含有氯分子的混合物是( )
A.液氯 B.盐酸 C.次氯酸 D.氯水
3、下列叙述正确的是( )
A. 1mol H2OSO4的质量为98g・mol-1
B. H2SO4 的摩尔质量为98g
C. 98gH2SO4含有NA个H2SO4分子
D. 6.02×1023个H2SO4分子的质量为9.8g
4、如果你家里的食用花生油混有水份,你将采用下列何种方法分离( )
A.过滤 B.蒸馏 C.分液 D.萃取
5、下列反应进行分类时,既属于氧化还原反应又属于化合反应的是( )
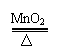 A.
A.![]() B.
B.![]()
![]()
C.![]() D.
D.![]()
6、Na与Na+比较,相同的是( )
A.半径 B.化学性质
C.最外层电子数 D.焰色反应的颜色
7、下列几种气体中,在同温同压下,等质量时所占体积最大的是( )
A.一氧化碳 B.甲烷
C.二氧化碳 D.氢气
8、下列实验设计方案中,可行的是( )
A. 用加入适量铜粉的方法除去Cu(NO3)2溶液中混有的NaNO3
B. 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体
C. 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的![]()
D. 先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
9、448mL某气体在标准状况下的质量为0.64g,该气体的摩尔质量约为( )
A.32g B.32 C.32g・mol-1 D.32g・mol
10、放射性同位素12553I可用于治疗肿瘤,该同位素原子核内的中子数与核外电子数之差为( )
A.72 B.19 C.53 D.125
11、与50mL 0.1mol/L的Na2CO3的溶液中Na+物质的量浓度相同的溶液是( )
A.50mL 0.1mol/L NaCl溶液 B.10mL 0.2mol/L NaCl溶液
C.25mL 0.2mol/L Na2CO3溶液 D.10mL 0.5mol/L Na2CO3溶液
12、氢化钠(NaH)是一种“生氢剂”,它与水反应的化学方程式为:
NaH+H2O=NaOH+H2↑ 其中,水的作用是( )
A.溶剂 B.还原剂 C.氧化剂 D.催化剂
13、鉴别Cl-、Br-、I-三种离子,不宜选用的试剂组是( )
A.溴水和淀粉溶液 B.AgNO3溶液和稀HNO3
C.氯水和CCl4溶液 D.氯水和淀粉溶液
14、新制氯水与久置氯水相比较,下列结论不正确的是( )
A.颜色相同 B.前者能使有色布条褪色
C.都含有H+ D.加AgNO3溶液都能生成白色沉淀
15、将4gNaOH溶于水,配成1L溶液,从中取出10mL,这10mL溶液的物质的量浓度为( )
A.10mol/L B.1mol/L C.0.1mol/L D.0.01mol/L
16、1molSO2和1molSO3具有相同的①分子数 ②原子数 ③S原子数 ④O原子数。( )
A.①② B.①③ C.①④ D.②④
17、配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A. 容量瓶中原有少量的蒸馏水
B. 移液时,不慎将液体流到瓶外
C. 溶解后没有冷却就转移到容量瓶中
D. 定容时俯视观察刻度线和液面
18、下列物质与其用途相符合的是( )
①Cl2――做消毒剂 ②AgBr――制胶卷、感光纸 ③AgI――人工降雨 ④碘――预防甲状腺肿大 ⑤淀粉――检查I2的存在 ⑥NaClO――漂白纺织物
A.②③④⑤⑥ B.①②③④⑤ C.②③④⑤ D.全部
19、下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
A.碘水 B.溴水 C.氯化钠溶液 D.氯水
20、下列各物质互为同位素的是( )
A.![]() B.H2O和D2O
B.H2O和D2O
C.金刚石和石墨
D.![]()
21、下列氯化物既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是( )
A.CuCl2 B.FeCl3 C.FeCl2 D.AlCl3
22、为实现我国2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在。已知溶液中![]() 可以与I-发生如下的反应:
可以与I-发生如下的反应:
![]()
据此反应,可用试剂和一些生活中常见的物质进行试验,证明在食盐中存在着![]() 。可供选用物质是:①自来水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤食糖 ⑥食醋 ⑦白酒。进行上叙实验时必须使用的物质是――――――( )
。可供选用物质是:①自来水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤食糖 ⑥食醋 ⑦白酒。进行上叙实验时必须使用的物质是――――――( )
A.①③ B.③⑥ C.②④⑥ D.①②④⑤⑦
二、填空题(24分)
23、(6分)(1)Na2SO4的相对分子质量是
,(2)摩尔质量为
,(3)1mol Na2SO4的质量为
,含有
个氧原子,完全电离时可生成Na+和![]() ,其电离方程式为
。
,其电离方程式为
。
24、(6分)现有磷酸、纯碱、甲烷、碳粉、熟石灰、四氧化三铁六种物质,将他们的化学式分别填入相应的空格内。
(1)单质 (2)氧化物
(3)酸 (4)碱
(5)盐 (6)有机物
25、(6分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(2)漂白粉的有效成分是(填名称) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) 。
26、(6分)已知:Fe2O3+2CO 2Fe+3CO2
(1) 标出该反应中电子转移的方向和数目
(2) 指出该反应中,氧化剂是 ,还原剂是 ;
(3) 在该反应中,若有2mol e-发生转移,要标准状况下,可生成CO2的体积为 。
三、推断题(8分)
27、(8分)现有X、Y、Z三种元素,已知有如下情况:
① X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易深于水,在水溶液中电离出X+、和Z-。XZ的水溶液可使石蕊试液变红。
④ 两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
完成下列问题:
(1)写出XZ和X2Y的化学式:XZ X2Y
(2)Z的单质溶于X2Y后,溶液起漂白作用的物质是 (写化学式)。
(3)写出X的单质在Z的单质中燃烧的化学方程式
(4)Z的单质能否与氢氧化钠溶液发生反应: (填“能”、或“否”),若能,请写出反应的化学方程式: 。
(若不能反应,则此空不必填写)。
四、综合实验题(12分)
28、(6分)实验室用固体烧碱配制500mL 0.1000mol/L的NaOH溶液。
(1)需称量 g 烧碱。
(2)配制过程中,不需要的仪器(填写代号)
A、烧杯 B、量筒 C、玻璃棒 D、100mL容量瓶
E、漏斗 F、胶头滴管 G、药匙 H、洗瓶
(3)根据实验需要和(2)所列仪器判断,完成实验还缺少的仪器是
(4)在容量瓶中确定溶液体积的过程中,最后加入少量水的做法是
29、(6分)实验室用下列仪器和药品制取干燥纯净的氯气。
(1)、按气流从左到右,装置正确的连接( )接( )接( )接( )接( )接( )接( )接( )(填各接口字母)
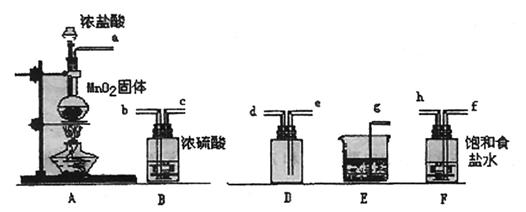
(2)装置F的作用是 ,装置E的作用是 。
(3)装置A中的反应化学方程式为:
五、计算题(12分)
30、(3分)用4克NaOH配制成250mL溶液,求此溶液的物质的量浓度
31、(9分)实验室利用高锰酸钾和浓盐酸反应制取Cl2,己知方程式为
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
要制得Cl2 11.2L(标准状况下)
求:(1) 参加反应的高锰酸钾物质的量
(2)被氧化的HCl的物质的量
(3)若反应后溶液的体积为200mL,求C(MnCl2)
参考答案:
一、选择题(本题包括22小题,每小题只有一个选项正确,每小题2分,共44分)
| 题序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 答案 | D | D | C | C | C | D | D | D | C | B | B |
| 题序 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| 答案 | C | A | A | C | B | B | D | C | D | D | B |
二、填空题(24分)
23、(1)142 (2)142g/mol (3)142g,2.408×1024,Na2SO4=2Na++SO2-4
24、(1)C (2)Fe3O4 (3)H3PO4
(4)Ca(OH)2 (5)CaCO3 (6)CH4
25、(1)2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
(2)钙
(3)Ca(ClO)2+CO2+H2O=CaCO3+2HclO
(4)反应(1)
26、
化合价降低得2×3e―被还原
|
![]()
![]()
![]()
![]() (1)Fe2O3+2CO 2Fe
+ 3CO2
(1)Fe2O3+2CO 2Fe
+ 3CO2
化合价升高得3×2e―被氧化
(2)Fe2O3 ,CO
(3)22.4
三、推断题(8分)
27、(1)HCl ,
H2O
(2)HClO (3)![]()
(4)Cl2+2NaOH=NaCl+NaClO+H2O
四、综合实验题(12分)
28、(1)2.000 (2)D、E (3)500mL容量瓶
(4)在1~2cm处改用胶头滴管视线与最低凹液面相平
29、(1)a f h b c e d g
(2)除去多余的HCl,将生成的氯气反应消耗掉。
(3)![]()
五、计算题(12分)
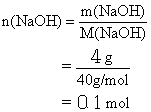 30、解:
30、解:
∵
又∵n=C・V
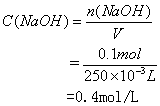 |
∴
答:此溶液的物质的量浓度为0.4mol/L。
31、解:(1):设参加反应的高锰酸钾物质的量为X。
2KmnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
2mol 10mol 2mol 5mol
x y z 0.5mol
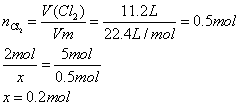
答:参加反应的高锰酸钾物质的量为0.2mol。
(2)∵参加被氧化的HCl是10mol
设被氧化的HCl物质的量为y
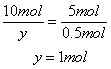
答:被氧化的HCl的物质的量为1mol。
(3)设MnCl2物质量为Z
∵n(MnCl2)=C(MnCl2)・V(MnCl2)
∴![]() 错误!未找到引用源。
错误!未找到引用源。
答:MnCl2的物质的量浓度为1mol/L。