��һ��ѧ��һѧ�����п���
����ѧ���ԡ��⡡��
���Ծ��ֵ�I����ѡ���⣩�͵�II������ѡ���⣩�����֣�����100�֣�����ʱ��90���ӡ�
�����õ������ԭ��������H-1��C-12�� N-14��O-16��Na-23��S-32��C l-35.5��Zn-65
��I����ѡ���⣬��50�֣�
��ܰ��ʾ��
1�����I��ǰ��������ؽ��Լ������������Ժš����Կ�Ŀ���Ծ�������Ǧ��Ϳд�ڴ���ϣ�
2����I��ÿС��ѡ���𰸺���Ǧ�ʰѴ���϶�Ӧ��Ŀ�Ĵ𰸱��Ϳ�ڣ�����Ķ�������Ƥ���ɾ�����ѡͿ�����𰸣����ܴ����Ծ��ϡ�
ѡ���⣺�����20��С�⣬1��10��ÿС��2�֣�11��20��ÿС��3�֣���50�֡���ÿС��������ĸ�ѡ���У�ֻ��һ���Ƿ�����ĿҪ��ġ�
1��ʪ�����ɫʯ����ֽ����ʢ��Cl2�ļ���ƿ�У��Թ۲쵽������������ȷ����
������ A����졡������B���ȱ����ס�����C�������ɫ��������D������ɫ
2�������������ڴ��������
A��Ư�ۡ�����B����ˮ����������������C��Һ�ȡ����������������� D������
��������ȥС�մ���Һ�е������մ����ʣ�����ѡ�ü����������
A��CO2����������������B�����ᡡ������ ������C���Ȼ��ơ��������� D����������
�������и����е����ӣ���ɫ������������Һ�д����������
A��Na+��Mg2+��Cl����CO![]() ��������������B��K+��Cu2+��SO
��������������B��K+��Cu2+��SO![]() ��NO
��NO![]()
C��K+��Na+��ClO����Cl�������������������� D��Mg2+��Al3+��NO![]() ��SO
��SO![]()
5����Fe(OH)3�����м���ij�����ʣ�����۲쵽��ʼ�����������������������ʱ���������ܽ⣬�����Ŀ����ǣ�
����A��NaCl��Һ�������������� B��ϡ���ᡡ��������������C��ˮ������ D��MgSO4��Һ
6������������ȷ����
�� A��Ԫ�ش������̬ʱһ������ǿ������
B���õ���Խ���������������������Խǿ
C��������ֻ�ܵõ����ӱ���ԭ����������
D��Ԫ�ص��ʿ���������ԭ����Ԫ�صĻ��������Ƶ�
������֪ijǿ������Һ�к���Fe2+��Ba2+��Na+�������Һ�����ܴ��ڵ���������
����A��Cl��������B��NO![]() ����
C��SO
����
C��SO![]() ����
D��HCO
����
D��HCO![]()
������ʵ�����У��������¹ʻ�ҩƷ�Ĵ�����ȷ����
A���д���������й©ʱ���÷���ˮ��ʪ�������棬��Ѹ���뿪�ֳ�
B���������Ż�ȼ��ʱ������ĭ��������
C������Ũ����մ��Ƥ���ϣ�����������������Һ��ϴ
D��������ķ�Һ����ˮ�أ���ˮ������ˮ��
������NA��ʾ�����ӵ�������ֵ������������ȷ���ǡ�������
A��Ħ���ǹ��ʵ�λ�����߸�����������֮һ
B����״���£�22.4Lˮ�������еķ�����ΪNA
C�����³�ѹ��,1.06g Na2CO3���е�Na+������Ϊ0.02 NA
D�����ʵ���Ũ��Ϊ0.5mol��L��1��MgCl2��Һ�У�����Cl�� ����ΪNA
10��Na2O��Na2O2 ��������һ�������������Ƶġ�����
A������������ ����B��ˮ��Һ�ʼ��� ��C�������ԡ� D��Ư����
11����������ȵ�����2%ת��Ϊ�����Լ�ǿ�ġ��������������ܼ�������˥�ϣ�����Ϊ������ɱ�֡������ú���Ԫ�أ�Se���Ļ������������ƣ�Na2SeO3��������������ȵĻ��������ɴ��ƶ�Na2SeO3��������
A������ԭ������������������ B����������
C������������������ԭ������ D���Ȳ����������ֲ�����ԭ��
12�����й��ڵ���ʡ��ǵ���ʵ�˵����ȷ����
�� A����������ˮ����ˮ������Һ�ܵ��磬��������ǵ����
B��CaCO3������Һ����������������CaCO3���������
C��HF��ˮ��Һ�м���H+��F�������д�����HF���ӣ����HF���������
D����������������Һ�϶���������ʵ���Һ
13��ͬ��ͬѹ�£���������HCl������������е�NH3��������ԭ�Ӹ�����ȣ���ס��������������֮��Ϊ��
A��1:1������������������B��1:2������������������C��2:1������������������D��1:4
14���������ӷ���ʽ��ȷ���ǡ�
A������ϡ���ᷴӦ��2Fe+6H+ = 2Fe3++3H2��
B��������þ�������Mg(OH)2+2H+ = Mg2++2H2O
C��ͭƬ���Ȼ�����Һ��Ӧ��Cu+Fe3+ = Cu2++Fe2+
D���Ʒ���ˮ�У�Na+H2O = Na++OH��+H2��
15����1.15���Ʒ���ˮ�У�Ҫʹ100��ˮ����������1�������ӣ������ˮ������Ϊ��
A��115g����������������B��100g����������������C��90.9g�������������������� D��90g
16����ij�����ˮ��Һ�м���Fe2+����Һ������������ͨ������Cl2���Һ���ֺ�ɫ����ô��˵õ��Ľ������������ǡ�
����A���þ����к���SCN�����ӡ�����B��Fe3+������������Cl2ǿ
C��ԭ��Һ�в���Fe3+���ӡ����� D��Fe2+��SCN�����Ӳ����γɺ�ɫ����
17�����������ĸ���Ӧ
��1��H2S+I2 = 2H++2I��+S������������������2��2H2S+3O2 = 2H2O+2SO2
��3��2I��+Br2 = 2Br��+I2�������������������� ��4��SO2+I2+2H2O = H2SO4+2HI
ȷ��Br����I����H2S��SO2��ԭ����ǿ������˳���ǡ�
A��H2S> SO2>I��>Br������������������ B��Br��>I��> SO2>H2S
C��I��>SO2>H2S>Br��������������������D��I��>Br��>H2S> SO2
18��ij�������Ħ������ΪMg��mol-1������״���µĸ�����VL�ܽ���1000gˮ�У������岻��ˮ��Ӧ��������Һ�ܶ�Ϊ��g��cm-3����������Һ�����ʵ����ʵ���Ũ��Ϊ��
������ A��![]() ������ ����B��
������ ����B��![]()
������ C��![]() ��������D��
��������D��![]()
19����״���£��� 6.72L NH3�� �� 1.204��1023�� H2S�� �� 6.4g CH4��
��0.5mol HCl �����й�ϵ��ȷ���ǡ�
����A�������С:�� ��>��>��>�١� B��ԭ����Ŀ:�� ��>��>��>��
����C���ܶȴ�С������>��>��>�١� D��������С������>��>��>��
20����x R+ + yH++ O2 = m R2++ nH2O���ӷ�Ӧ����ʽ�У�mֵ�ǡ�
A��2x���� B��4������C��3���� D��2
��һ��ѧ��һѧ�����п���
����ѧ���ԡ��⡡��
�ɼ�ͳ�Ʊ�(������Ҫ��д)
| ��� | 21 | 22 | 23 | 24 | 25 | 26 | 27 | �ܷ� |
| �÷� |
��II��������ѡ���� ��50�֣�
��ܰ��ʾ��
1���뽫��д�ڴ�����ϣ������Ծ��ϵ���Ч��
2�����ǰ��������ܷ����ڵ���Ŀ��д�����
| �� �� | ������ |
21����7�֣��ڷ�Ӧ![]() �У���������____________����ԭ����__________������������_____________����Ӧ�е���ת������Ϊ_________���÷�Ӧ���������______________________�ԣ��������ͻ�ԭ�������ʵ���֮��Ϊ _________��
�У���������____________����ԭ����__________������������_____________����Ӧ�е���ת������Ϊ_________���÷�Ӧ���������______________________�ԣ��������ͻ�ԭ�������ʵ���֮��Ϊ _________��
| �� �� | ������ |
22����8�֣���1������������Na+��K+��Cu2+��H+��NO![]() ��Cl����CO
��Cl����CO![]() ��OH���������ܴ���������ͬһ��Һ������������Ƿֳ�A��B���飬����ÿ���о������������Ӻ����������ӡ�
��OH���������ܴ���������ͬһ��Һ������������Ƿֳ�A��B���飬����ÿ���о������������Ӻ����������ӡ�
������ A��_______________________________________
������ B��_______________________________________
��2����ͬŨ�ȵ�AgNO3��Һ�ֱ���ͬŨ�ȵ������NaCl��MgCl2��AlCl3��Һ��Ӧʱ�� ����AgNO3��Һ�������Ϊ_________________________��
������ ����ͬŨ�ȵ������AgNO3��Һ�ֱ����Ũ�ȵ�NaCl��MgCl2��AlCl3��Һ��Ӧʱ������������������Һ�������Ϊ______________________��
| �� �� | ������ |
23����11�֣���֪A��BΪ���嵥�ʣ�DΪ���嵥�ʣ�CΪ���������֮��������ת����ϵ��
 ����������������������������������������������������������������������������������������������������������������������������������
����������������������������������������������������������������������������������������������������������������������������������
��1����д��A��B��C��D�Ļ�ѧʽ��
�� A______________��B______________��C______________��D______________��
��2��д��C��ˮ��Һ��D��Ӧ�����ӷ���ʽ��______________________________;
F+D��Ӧ�����ӷ���ʽ��_____________________________________________��
��3������F�������ӵ��Լ������ã�____________________________________;
�����ǣ�________________________________________________________;
��4��E+NaOH������_________________________________________________;
��Ӧ�Ļ�ѧ����ʽΪ��____________________________________________;
������������������������ ____________________________________________��
| �� �� | ������ |
24����6�֣�������װ��ͼ����ʵ�飬��д�й�����ѧ����ʽ��
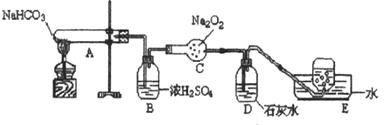
����
��A��������______________________________________________________________
��B��Ũ�����������______________________________________________________
��C�з�����Ӧ�Ļ�ѧ����ʽΪ______________________________________________
��D��������______________________________________________________________,
��Ӧ�Ļ�ѧ����ʽ��______________________________________________________
��E���ռ���������________________________________________________________
����
| �� �� | ������ |
25����6�֣�������ͼ��ʾ��װ���ռ�����7�����壺
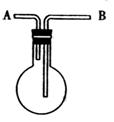 ��H2������Cl2�� ��CO2�� ��HCl�� ��NH3�� ��NO�� ��NO2����
��H2������Cl2�� ��CO2�� ��HCl�� ��NH3�� ��NO�� ��NO2����
��1������ƿ�Ǹ���ģ�����B�ڽ��������ռ���������___________������ţ���ͬ��������A�ڽ��������ռ��������� ______________________________��
��2��������ƿ�ڳ���ˮ�����ռ���������____________������Ӧ��___________�ڽ��룻
��3������ƿ��װ������Ũ���ᣬ���������������������_______________________������Ӧ��_______________________�ڽ��롣
| �� �� | ������ |
26����6�֣���9.75gп���뵽100 ml 2mol��L-1��������,����Ӧ����������
��1������ZnCl2�����ʵ���;
��2�����ɵ������ڱ�״���µ����.
| �� �� | ������ |
��7��(6��)ij��������16.80 g, ��Na2CO3��NaHCO3�е�һ�ֻ�������ɣ��Լ��㣨С���������λ���֣���
��1������Ʒ���������ᷴӦ������CO2�����ڱ���µ����V�����ֵ��____________�� ����HCl�����ʵ���n�����ֵ��_____________;
��2������������ȣ���ָ������ȴ���ù���13.70g���Լ���ԭ������и��ɷֵ����ʵ���Ϊ���٣�
|
��һ��ѧ��һѧ�����п���
��ѧ������������
�ɼ�ͳ�Ʊ�(������Ҫ��д)
| ��� | 21 | 22 | 23 | 24 | 25 | 26 | 27 | �ܷ� |
| �÷� |
��II�����������ѡ���� �� 50�֣�
��ܰ��ʾ��
1���뽫��II���𰸰�Ҫ��д��ָ��λ��;
2������ʱֻ�������II�������;
3�����ǰ���ܷ�������Ŀ��д���������ʱ����ֱ��д�ڴ�����ϡ�
21��(7��)_____________________,_______________________,______________________,
_______________________,________________________,_______________________��
22��(8��)
(1)A��_______________________________��B��____________________________
�� (2) __________________________________��________________________________��
23����11�֣�
��1��A__________��B__________��C__________��D_________��
��2��Cˮ��Һ��D��Ӧ��_________________________
���������� F+D�ķ�Ӧ��_________________________
��3���Լ���______________������____________________________________________
��4���֡���____________________________________________
��������ʽ��___________________________________________
���������� ___________________________________________
24��(6��)
��______________________________________________________________________
��______________________________________________________________________
��______________________________________________________________________
��______________________________________________________________________
______________________________________________________________________
��______________________________________________________________________
25����6�֣�
��1��__________________________________��____________________��
��2��__________________________________��____________________��
��3��__________________________________��____________________��
|
| �� �� | ������ |
26����6�֣�
| �� �� | ������ |
27����6�֣�
��1�����V��_______________________________
���� HCl���ʵ���n��_______________________
��2��
��һ��ѧ��һѧ�����п���
��ѧ����ο��𰸡�������������
һ��ѡ���⣨��50�֣�1-10ÿ��2�֣�11-20ÿ��3�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | B | C | A | D | B | D | A | A | C | B |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | A | C | C | B | C | B | A | D | B | B |
������ѡ���⣨��50�֣�
21��(7��)��![]() ��ԭ�ԡ����ԣ�2�֣�����ÿ��1�֣���1:��
��ԭ�ԡ����ԣ�2�֣�����ÿ��1�֣���1:��
22����8�֣�ÿ��2�֣�
��1��H+��Cu2+��Cl����NO![]() ������ OH����CO
������ OH����CO![]() ��Na+��K+���� ��2��1:2:3 6:3:2
��Na+��K+���� ��2��1:2:3 6:3:2
23����11�֣�ÿ��1�֣�
��1��Cl2�� H2�� HCl��Fe�� ��2��2H++Fe = H2��+Fe2+����2Fe3++Fe = 3Fe2+��������
��3��NaOH��Һ������NaOH��Һ���к��ɫFe(OH)3��������
��4�����ɰ�ɫ������Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ
FeCl2+2NaOH = Fe(OH)2��+2NaCl����4Fe(OH)2+O2+2H2O= 4Fe(OH)3����
24����6�֣�ÿ��1�֣�
���Թ��ڱ�����ɫҺ��
�����ڸ���CO2���壨������ˮ������
������![]()
������ʯ��ˮ����ǡ�����![]()
������O2
25����6�֣�ÿ��1�֣�
��1��2��3��4��7�������������������� 1��5��
��2��1��6������������������������ ����A����
��3��1��2��3��4��6��7���������� B����
26����6�֣�
��ʾ�����ж�Zn ������2�֣�����1��0.1 mol��2�֣�����2��2.24L��2�֣�
27����6�֣�
��1��4.48�� 0.32 ����1�֣�����2��NaHCO3 0.10mol;�� Na2CO3��0.08mol ����2�֣�