��һ��ѧģ��ѧҵ��������
����ѧ1������
˵�������Ծ�4ҳ����100�֣�����ʱ��90����
�����õ������ԭ��������H��1 O��16 C��12 N��14��Na��23 S��32 Cl��35��5 Ba��137
����������� �������������� �������������� ���ɼ���������
��һ����ѡ���⣨48�֣�
һ��ѡ���⣨�������16С�⣬ÿС��3�֣���48�֡�ÿС��ֻ��һ��ѡ��������⣩
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| �� |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1��ij�л���б��ӡ����Լ�ƿ�������±�ʶ��
������������������������������  ��������������
�������������� ��������������
��������������
������־�ĺ�����
A����Ȼ��Ʒ����ȼ ��B����ʴ�ԡ��ж���C����ը�ԡ���ʴ�ԡ� D�����������ж�
2��Ũ��Ϊ2mol/L��NaOH��Һ����ȷ������
A����2Lˮ������80�˵�NaOH���� �� B��80��NaOH����2Lˮ��ɵ���Һ
C��ÿ����Һ�к���80��NaOH�������� D��ÿ2L��Һ�к���80��NaOH
3�����˺��ʳ��ˮ�Ժ��п����Ե�CaCl2��MgCl2��Na2SO4 �����ʣ�ͨ�����¼���ʵ�鲽�裬���Ƶô�����ʳ��ˮ���� �����Թ�����Na2CO3��Һ���� �����Թ�����NaOH��Һ���� �����Թ�����BaCl2 ��Һ���ܵ���ϡ�����������ݲ������� ����
���в���˳������������
A���ۢڢ٢ݢܡ��� B���ۢ٢ڢݢܡ��� C���ڢۢ٢ݢܡ��� D���٢ۢڢܢ�
4������������������
A��0.012kg12C�к���Լ6.02��1023��̼ԭ��
B��1mol�κ����ʶ�����Լ6.02��1023��ԭ��
C����ʹ��Ħ����ʾ���ʵ����ĵ�λʱ��Ӧ�û�ѧʽָ�����ӵ�����
D�����ʵ����ǹ��ʵ�λ�����߸�����������֮һ
5����״���£����������к���ԭ�Ӹ���������
A��3.01��1024��H2���ӡ���B��22.4 L H2O������C��23 g C2H5OH������D��22.4 L NH3
6������һƿ���ҵĻ�����֪���ҵ�ijЩ�������±���ʾ���ݴˣ������һ������ķ�����

A����ȡ���������� B������������������C�������������� D�����˷�
7����a g CO2��b�����ӣ����ӵ�������ֵΪ
A��ab/28���������� B��ab/14�������� C��28/b�������� D��44b/a
8���������������ڵ���ʵ���
�� KOH ���� CuSO4������ Al���� ��HCl���������� ���ǡ�
A���٢� �ۡ�������B���ڢۢܡ������� C���ۢܡ������� D���٢ڢ�
9���������ӷ���ʽ��д��ȷ���� ������������������������������������������
A������Ͷ�뵽NaOH��Һ�У�2Al+2OH���T�T 2AlO2��+H2��
B��AlCl3��Һ�м��������İ�ˮ��Al3++ 3OH�� �T�T Al(OH)3��
C�����Ȼ�����Һ�м������ۣ�![]()
D��FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2=2Fe3++2Cl��
10�� ֻ�������Լ��е�һ�֣����ܽ�FeCl3��NH4Cl��NaCl������Һ�����ǡ���
A��KSCN��Һ����B��BaCl2��Һ������C��NaOH��Һ����D��AgNO3��Һ
11���ڻ����� ��KOH ��Al(OH)3����HNO3�У������������������Һ���ɷ�Ӧ����
������������������������������������������������������������������������������������������������������������������������ A��ֻ�Тڡ� ���� B���ٺۡ͢������� C���ںۡ͢�������D���٢ڢ�
12���輰�仯�����ڲ���������Ӧ�ù㷺��������������ȷ���ǡ���������
A���赥�ʿ���������̫���ܵ�ء������� B���赥�������첣������Ҫԭ��
C��ʯӢ��SiO2����������������Ʒ������ D������������������ά�IJ���
13�����и����е����ӣ�������Һ�д���������ǡ�����������������������
A��H����Na����CO32���������������� B��Cl����Ba2����SO42�� ����
C��H����OH����SO42�� �������������� D��H����Ag����NO3��
14�����й����У��漰��ѧ�仯���ǡ�����������������������������������
A������ͨ��ˮ������ˮ������������ B�����Ȼ�̼��ȡ��ˮ�еĵ�
C������̿ʹ��īˮ��ɫ������������ D��������ˮ����Ϊ����ˮ
15.���������У�������Ũ�������������������Ƹ������
����A.CO2������������ B.N2���������� C.SO2������������ D.NH3
16����NaOH��������һ�����ʵ���Ũ�ȵ�NaOH��Һ�����в�������ȷ���ǡ���
A������ʱ��������NaOHֱ�ӷ�����ƽ������
B���������õĹ���NaOH��������ƿ�У�������ˮ�ܽ�
C������ʱ�����ˮ�����˿̶��ߣ��ý�ͷ�ι�ֱ���������ಿ��
D�����ձ����ܽ����NaOH������Һ����ȴ�����º�ת��������ƿ��
�ڶ���������ѡ���⣬��52�֣�
�������������3С�⣬��22�֣�
17����6�֣�ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϣ�
A�����ˡ�B���ᾧ C����Һ��D������E����ȡ��Һ��F��������
��1������������ ����ˮ�����Ȼ�̼�Ļ���
��2������������ �����Ȼ�����Һ��ɳ�ӵĻ���
��3������������ ������غ��Ȼ��ƵĻ����Һ�л������أ�
��4������������ ����ƾ����е�Ϊ78.1�棩�ͼױ�(�е�Ϊ110.6��)�Ļ���
��5������������ ����ʳ�κ͵�Ļ���
��6������������ �ӵ�ˮ����ȡ�ⵥ�ʡ�
18����8�֣�ʵ����������ͼ��ʾװ�ý���NaHCO3�����ȷֽ�ʵ�顣��ش�
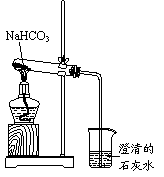 ��1������һ��ʱ����ձ��й۲쵽��ʵ����
��1������һ��ʱ����ձ��й۲쵽��ʵ����
�������������������������������� ��
��2��ʵ�����ʱ����ȷ��������������������ţ���
��������������������������� ��
�� �Ƚ����ܴ�Һ�����Ƴ�����Ϩ��ƾ���
�� ��Ϩ��ƾ��ƣ��ٽ����ܴ�Һ�����Ƴ���������
��3��NaHCO3���ȷֽ�Ļ�ѧ����ʽ��
������������������������������������������������ ��
19����8�֣��ڻ�ѧ���ϣ�Χ��Ũ����Ļ�ѧ���ʽ���������ʵ��̽���������������Ƿ����ձ��У����뼸��ˮ��������ȡ�Ȼ���ټ�������Ũ���ᣬѸ�ٽ��裬�ų��������ȣ�ͬʱ�۲쵽������ڣ�������ͣ��������̼�����ζ�����塣
��ش�
��1�����ɵĺ�ɫ�������������� ���ѧʽ����
��2���̼�����ζ��������Ҫ�ɷ������������� ���ѧʽ��������������Ļ�ѧ����ʽΪ������������������������������������������������������������ ��
��3����������ʵ��������Ũ������������������������� ������ţ���
�� ���ԡ��������� ��ˮ�ԡ����� �� ��ˮ�ԡ����� �� ǿ������
�����ƶ��⣺���������2С�⣬��24�֣�
20������9�֣���X��Y��Z����Ԫ�أ�
��1��X��Y��Z�ĵ����ڳ����¾�Ϊ���壻
��2��X���ʿ�����Z�ĵ�����ȼ�գ�������ΪXZ������ʲ�ɫ��
��3��XZ��������ˮ����ˮ��Һ�е����X+��Z-����ˮ��Һ��ʹ��ɫʯ����ֽ��죻
��4��ÿ2��X2��������1��Y2���ӻ��ϳ�2��X2Y���ӣ�X2Y������ΪҺ�壻
��5��Z��������X2Y�У�������Һ����Ư���ԡ�
��д����Ԫ�ط��ţ�X_______��Y_______�� Z_______���Լ�������ķ���ʽ��
XZ_______��X2Y_________����2����Ӧ�Ļ�ѧ����ʽ������������������������������������
��4����Ӧ�Ļ�ѧ����ʽ������������������������������������
21����13�֣���ͼ��ʾA����E���ֺ��������ת���Ĺ�ϵͼ������A��B��C��D�����¶������壬BΪ����ɫ��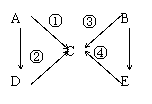
д���������ʵĻ�ѧʽ��A_______��B_______�� C_______��D_______ ��E_______
������Ӧ�Ļ�ѧ����ʽ��
����������������������������������������������������������������������������������������������������������������
���������������������������������������������������������������������������������� ������������������������������������
������������������������������������������������������������������������������������������������������������������������
����������������������������������������������������������������������������
22�������⣨8�֣�ȡ17.3g��NH4Cl��(NH4)2SO4���������ˮ��ȫ�ܽ����50mL��BaCl2��Һ��ǡ�÷�Ӧ��õ�11.65g�İ�ɫ�������Լ������������NH4Cl�����ʵ�����BaCl2��Һ�����ʵ���Ũ�ȡ�
��������������
��һ����ѡ���⣨48�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| �� | B | C | D | B | B | C | D | D | D | C | A | B | D | A | B | D |
�ڶ����ַ�ѡ���⣨52�֣�
17����6�֣�C,A,B,D,F,E
18����8�֣�
��1�������ʯ��ˮ����ǡ���������������������������������2��
��2���١�����������������������������������������������2��
���� ��������������������������������������������������2��
�������� ��3��2NaHCO3������ Na2CO3 + CO2��+ H2O ����������������2��
19����8�֣���1��C ��������������������������������������������������2��
��������2��SO2��������������������������������������������������2��
������C + 2H2SO4(Ũ)����������CO2�� + 2SO2�� + 2H2O������2��
�������� ��3���ڢۢܡ�����������������������������������������������2��
20������9�֣�
X:�� H2��Y: O2�� Z: C l2:��XZ: H C l ��X2 Y:�� H2O����2��Cl2��H2 === 2HCl����������������������������
��4��2H2 + O2 ===2H2O
21����13�֣�
A:��N2��B :NO2�� C: NO��D :NH3 ��E :HNO3
����N2+O2![]() 2NO �� 4NH3+5O2
= 4NO+6H2O ��3NO2+H2O = 2HNO3+NO
2NO �� 4NH3+5O2
= 4NO+6H2O ��3NO2+H2O = 2HNO3+NO
��3Cu+8HNO3��ϡ��=3Cu��NO3��2+2NO��+4H2O
22��8�֣�0.2mol��1mol/L