高一化学模块学业考试试题
《化学1》试题
说明:1、本卷分为第一卷和第二卷。第一卷为选择题,共70分;第二卷为非选择题,共30分。全卷共100分,考试时间90分钟。
第一卷(70分)
可能用到的相对原子质量:H: 1 C: 12 O: 16 S:32
一、单项选择题(本题包括25小题,只有一个选项符合题意。每小题2分,共50分)
1.下列物质中,不属于合金的是
A.硬铝 B.黄铜 C.钢铁 D.水银
2.下列物质中,能够导电的是
A.二氧化碳气体 B.盐酸溶液 C.蔗糖溶液 D.固体氯化钠
3.铝在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一加以控制。铝及其化合物在下列场合的合用须加以控制的是
①制铝锭 ②制易拉罐 ③制电线、电缆 ④制包糖果用的铝箔 ⑤用明矾净水 ⑥制炊具 ⑦用明矾和苏打作食物膨胀剂 ⑧用氢氧化铝制胃药 ⑨制防锈油漆
A.①②④⑤⑥⑦⑧ B.②⑤⑥⑦⑧
C.②④⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
4.下列各组中的离子,能在溶液中大量共存的是
A.K+ 、H+ 、SO42-、OH- B.Na+、Ca2+、CO32-、NO3-
C.Na+、H+ 、Cl-、CO32- D. Na+、Cu2+、Cl-、SO42-
5.下列物质中,主要成分不是硅酸盐的是
A.陶瓷 B.大理石 C.玻璃 D.水泥
6.现有硫酸钠、硫酸铝、硫酸镁三种无色溶液,若有一种试剂将它们区别开来,该试剂是
A.纯水 B.盐酸 C.硝酸银溶液 D.氢氧化钠溶液
7.现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁含有Cu2+
C.苹果汁含有OH− D.苹果汁含有Na+
8.在实验室里,储存在棕色瓶中的药品是
A.浓盐酸 B.浓硝酸 C.浓硫酸 D.氯化钠
9.若NA表示阿伏加德罗常数,下列关于0.3mol /L的MgCl2溶液的说法正确的是
A.100毫升的溶液中含有Mg2+、Cl―总数为0.3NA
B.100毫升的溶液中含有Mg2+数目是0.1NA
C.1升溶液中Mg2+的浓度是0.3mol / L
D.1.5升溶液中含有Cl―的浓度是4.5mol / L
10.以下实验装置一般不用于分离物质的是
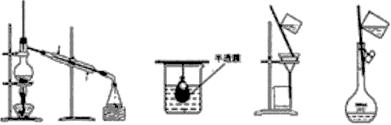
A B D
11.用铜锌合金制成的黄铜制品常被误作黄金。下列方法不能区分其真伪的是
A.观察外表 B.放入硝酸中 C.测定密 D.放入盐酸中
12.下列关于SO2的说法中,不正确的是
A.SO2是硫及某些含硫化合物在空气中燃烧的产物
B.SO2具有漂白性,可以使品红溶液褪色
C.SO2溶于水后生成H2SO4
D.SO2是一种大气污染物
13.某物质在灼烧时透过蓝色钴玻璃看到火焰呈紫色,说明该物质中一定含有
A.钾原子 B.钾离子 C.钾元素 D.钾的化合物
14.检验氨气可以用
A.湿润的红色石蕊试纸 B.干燥的红色石蕊试纸
C.干燥的蓝色石蕊试纸 D.湿润的蓝色石蕊试纸
15.用金属铜制取硝酸铜,从节约原料和防止环境污染考虑,最好的方法是
![]() A.铜 硝酸铜 B.铜
硫酸铜
硝酸铜
A.铜 硝酸铜 B.铜
硫酸铜
硝酸铜
![]()
![]() C.铜
氯化铜
硝酸铜 D.铜
氧化铜
硝酸铜
C.铜
氯化铜
硝酸铜 D.铜
氧化铜
硝酸铜
16.下列各组分散系,需用丁达尔效应区分的是
A.溶液与浊液 B.胶体与胶体 C.溶液与胶体 D.溶液与溶液
17. 检验下列离子时,选用的试剂错误的是
A.Fe2+ (KSCN溶液) B.Cl- (稀硝酸酸化的AgNO3溶液)
C. NH4+ (NaOH溶液) D.SO42- (盐酸酸化的BaCl2溶液)
18. 下列有关钠的物理性质的叙述中正确的是
①银白色金属 ②质软 ③可以用小刀切割 ④熔点低于100℃
⑤密度比水小 ⑥热和电的良好导体
A.①②③ B.①②③④ C.②③④⑤⑥ D.①②③④⑤⑥
19. 鉴别Na2CO3与NaHCO3两种固体,最好的方法是
A. 加热 B. 加水 C. 加NaOH溶液 D. 加Ca(OH)2溶液
20. 铝具有较强的抗腐蚀性能,主要是因为
A.与氧气在常温下不反应 B.铝性质不活泼
C.铝表面能形成了一层致密的氧化膜 D.铝耐酸耐碱
21. 要除去FeCl2溶液中的少量氯化铁,可行的办法是
A.滴入KSCN溶液 B.通入氯气 C.加入铜粉 D.加入铁粉
22.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是
 |
注 (腐蚀品) (爆炸品) (有毒气体) (易燃液体)
A B C D
23.实验室做化学实验,发生下列事故,处理方法不正确的是
A.金属钠着火,用泡沫灭火器扑灭
B.实验台上的酒精灯碰翻着火,立即用湿抹布扑灭
C.皮肤溅上浓H2SO4, 立即用大量水冲洗
D.汞洒落地面,应立即撒上一层硫黄粉
24. 化学“家庭小实验”是利用家庭日常生活用品在安全条件下进行化学学习和探究的活动。下列实验能利用“家庭小实验”进行的是:①证明马铃薯中含有淀粉;②除去热水瓶中的水垢;③证明炉子生火产生的气体中含有一氧化碳;④淀粉溶液具有丁达尔现象
A.①②③④ B.①③④ C.①②③ D.①②④
25.下列气体中,既能用浓硫酸干燥,又能用氢氧化钠干燥的是
A.CO2 B.N2 C.SO2 D.NH3
二、选择题(本题包括5小题,每小题4分,共20分。每小题有个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只先一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题就为0分)
26.下列化学方程式中,不能用离子方程式H++OH-= H2O表示的是
A.2NaOH + H2SO4 = NaSO4+2H2O B. Ba(OH)2 +2 HCl = BaCl2+2H2O
C. Ba(OH)2 + H2SO4 = BaSO4↓+2H2O D. Na2CO3 + H2SO4 = Na2SO4+2H2O+CO2↑
27.石英砂(主要成分为SiO2)是一种常用的工业原料,其中常混有少量碳酸钙,要除去石英砂中的少量碳酸钙,应采用的方法是
A.用水溶解后过滤分离 B.用稀硫酸溶解后过滤分离
C.用酒精灯加热 D.用稀盐酸溶解后过滤分离
28.农药波尔多液不能用铁制容器盛放,是因铁能与该农药中的硫酸铜起反应。在该反应中,铁
A.是氧化剂 B.是还原剂 C.被氧化 D.被还原
29 .下列描叙中,正确的是
A.Cl2以液态形式存在时可称作氯水或液氯 B.玛瑙的主要成分是二氧化硅
C.加碘食盐中所加的“碘”是KIO3 D.漂白粉的主要成分是次氯酸钙
30.除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:
①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;
⑤加过量的氯化钡溶液。下列正确的操作顺序是:
A. ①④②⑤③ B. ②⑤④①③ C. ⑤②①④③ D. ④①②⑤③
第二卷 (30分)
三、(本题包括2小题,共14分)
31、(6分)某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”
的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向溶液中滴加稀硫酸至溶液pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、 、 等玻璃仪器。
(2)步骤1过滤的目的是 。
(3)步骤1反应的化学方程式为 。
(4)步骤2中溶液的pH较难控制,可改用 。
32、(8分)某同学按下列步骤配制500ml0.2mol・L-1KCl溶液,请回答有关问题。
| 实验步骤 | 有关问题 |
| (1)计算所需KCl的质量 | 需要KCl的质量为 g |
| (2)称量KCl固体 | 称量过程中主要用到的仪器是 ; |
| (3)将KCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施 ; |
| (4)将烧杯中溶液转移至500mL容量瓶中 | 为了防止溶液溅出,应采取什么措施 ; |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意什么问题 ; |
你认为按上述步骤配制的KCl溶液的浓度是否为0.200mol・L-1,请说明理由。
四、(本题包括2小题,共16分)
33.(8分)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究.下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来,并说明理由。
| 物质组 | 不属于同一类的物质 | 理由 |
| (1)Mg、O2 、N2、NO | ||
| (2)NaOH、Na2CO3、CH4、KCl | ||
| (3)H2CO3、H2SO4、NH3・H2O、H2SiO3 | ||
| (4)CaO、SO2 、CO2、SiO2 |
34.(8分)下图表示A――E五种含氮物质相互转化的关系图。其中A、B、C、D常温下都是气体,B为红棕色,写出各步反应的化学方程式。
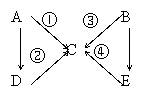 |
各步反应的化学方程式:
①
②
③
④
模块学业考试《化学1》试题
答案及评分标准
一、选择题(只有一个选项符合题意。每小题2分,共50分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| D | B | C | D | B | D | A | B | C | D | A | C | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| A | D | C | A | D | A | C | D | D | A | D | B |
二、选择题(本题包括5小题,每小题4分,共20分。每小题有个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只先一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题就为0分)
| 26 | 27 | 28 | 29 | 30 |
| CD | D | BC | BD | B |
三、(本题包括2小题,共14分)
31、(每空1分,化学方程式2分,共6分)
(1) 烧杯、漏斗
(2) 将杂质铁分离出来
(3) 2Al+2NaOH+2H2O==2NaAlO2+3H2↑
(4)稀盐酸
32、(8分)
| 实验步骤 | 有关问题 |
| (1)计算所需KCl的质量 | 需要KCl的质量为 7.5 g |
| (2)称量KCl固体 | 称量过程中主要用到的仪器是托盘天平 |
| (3)将KCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施适当加热 |
| (4)将烧杯中溶液转移至500mL容量瓶中 | 为了防止溶液溅出,应采取什么措施 转移过程中用玻棒进行引流 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意什么问题 当加水至离刻度线1-2厘米时,改用胶头滴管加水至凹液面与刻度线相切. |
不能。因为用托盘天平称取的溶质的质量只能精确到0.1克,故无法达到0.2000mol・L-1的要求.
四、(本题包括2小题,共16分)
33、(每空1分,共8分)
| 物质组 | 不属于同一类的物质 | 理由 |
| (1)Mg、O2 、N2、NO | NO | NO是化合物 |
| (2)NaOH、Na2CO3、CH4、KCl | CH4 | CH4是有机物 |
| (3)H2CO3、H2SO4、NH3・H2O、H2SiO3 | NH3・H2O | NH3・H2O是碱 |
| (4)CaO、SO2 、CO2、SiO2 | CaO | CaO是金属氧化物 |
34.(化学方程式2分,共8分)
①N2+O2![]() 2NO
2NO
② 4NH3+5O2 = 4NO+6H2O
③3NO2+H2O = 2HNO3+NO
④3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O