高一化学水平测试
化学(必修)
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,全卷满分100分,考试时间90分钟。第I卷答案请用2B铅笔填涂到答题卡上,第II卷用黑色字迹的钢笔或签字笔直接在试卷指定位置作答。
可能用到的相对原子质量: H:1 C:12 N:14 O:16 S:32
第I卷(选择题,共75分)
一、选择题(本题包括30小题,每小题2分,共60分。每小题只有一个选项符合题意)
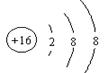
1.某些建筑材料中含有放射性元素![]() (氡),会对人体产生一定危害。该原子的中子数和质子数之差是
( )
(氡),会对人体产生一定危害。该原子的中子数和质子数之差是
( )
A.50 B.86 C.136 D.222
2.关于能量转化的叙述不正确的是 ( )
A.反应物总能量高于生成物的总能量的反应为放热反应
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.氧化还原反应的化学能才能转化为电能
D.需要加热才能发生的反应都是吸热反应
 3.下列化学用语中,正确的是
3.下列化学用语中,正确的是
A.丙烷的分子式:C3H6 B.硫离子结构示意图:
C.苯的结构简式:![]() D.氯化钠的电子式
D.氯化钠的电子式![]()
4.下列说法不正确的是 ( )
A.![]() H和
H和![]() H互为同位素
B.
H互为同位素
B. 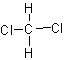 和
和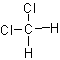 互为同分异构体
互为同分异构体
C.C3H6和C2H4可能互为同系物 D.石墨和金刚石互为同素异形体
5.下列是含有共价键的离子化合物的是 ( )
A.NaOH B.CaCl2 C.HClO D.H2O2
6.下列四个反应不属于氧化还原反应的是 ( )
A.Cl2和H2O B.NO2和H2O C.Na和H2O D.NH3和H2O
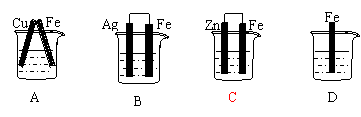
7.下图各容器中盛有稀硫酸,能形成原电池且铁为正极的是: ( )
8.某反应物A的浓度是2.0mol/L , 5min后,A的浓度变为0.5mol/L ,在这5min内A的化学反应速率是: ( )
A. 0.4 mol・L-1・min-1 B. 0.3 mol・L-1・min-1
C. 0.1 mol・L-1・min-1 D. 0.3mol/L
9.家庭使用的天然气(主要成分为CH4)、液化石油气(主要成分为C3H8)燃烧反应的主要化学方程式为CH4+2O2![]() CO2+2H2O;C3H8+5O2
CO2+2H2O;C3H8+5O2![]() 3CO2+4H2O
3CO2+4H2O
现有一套以液化石油气为原料的灶具,欲改为烧天然气,应采取的措施是: ( )
A.减少空气进量,增大天然气进量 B.减少空气进量,减少天然气进量
C.增大空气进量,增大天然气进量 D.增大空气进量,减少天然气进量
10.下列反应不属于取代反应的有 ( )
A.甲烷与氯气 B.苯与浓硝酸 C.乙酸与乙醇 D.乙烯水化制乙醇
11.下列物质能发生水解反应且水解产物只有一种的是 ( )
A.蛋白质 B.淀粉 C.蔗糖 D.葡萄糖
12.下列物质中可用来鉴别乙酸、乙醇、苯的是
A.水 B.溴水 C.氢氧化钾溶液 D.碳酸钠溶液
13.下列工艺原理不属于化学变化的是 ( )
A.煤干馏 B.石油分馏 C.石油的裂解 D.煅烧石灰石
14.我国城市环境中的大气污染物主要是 ( )
A.CO2、Cl2、N2、酸雨 B.SO2、NO2、CO、可吸入颗粒物
C.NH3、CO2、NO2、雾 D.HCl、SO2、N2、可吸入颗粒物
15.下列离子方程式错误的是 ( )
A.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
B.盐酸与氢氧化钡溶液:H++OH-=H2O
C.碳酸钙与稀硝酸:CaCO3+2H+=Ca2++CO2↑+H2O
D.硫酸铜溶液与氢氧化钡溶液:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓
16.下列不属于分散系 ( )
A.硫酸铜溶液 B.氢氧化铁胶体 C.液氨 D.牛奶
17.在强碱性溶液中能够大量共存且溶液为无色透明的离子组是 ( )
A.Na+ 、 NH4+ 、 NO3- 、 Cl- B.Na+ 、 K+ 、 CO32- 、 NO3-
C.K+ 、 Ba2+ 、 HCO3- 、 Cl- D.Na+ 、 K+ 、MnO4- 、 SO42-
 18.下列有关实验安全问题的叙述中不正确的是 (
)
18.下列有关实验安全问题的叙述中不正确的是 (
)
A. 为了标示不同类的危险品装运乙醇的包装箱应贴的图标是
B. 少量的浓硫酸沾到皮肤上时,直接用大量的水冲洗,再涂上小苏打溶液
C. 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂
D. 闻化学药品的气味都不能使鼻子凑近药品
19.不能与钠反应产生氢气的是 ( )
A.水 B.乙醇 C.苯 D.乙酸
20.下列各选项中,所表示的粒子的物质的量最多的是 ( )
A.在0℃和101KPa下,11.2L水中的H B.在0℃和101KPa下,11.2L H2中的H
C.98gH2SO4中的H D.2L 1.0mol/L 硝酸溶液中的H+
21.下列物质①NaHCO3 ②Al ③Al2O3 ④Al(OH)3中,既能与盐酸反应,又能与氢氧化钠溶液反应的是 ( )
A.③④ B.①③④ C.③ D.全部
22.下列物质不能用金属跟氯气直接反应制取的是 ( )
A.FeCl2 B.FeCl3 C.CuCl2 D.AlCl3
23.从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是 ( )
A.铜和浓硝酸 B.铜和稀硝酸
C.氧化铜和硝酸 D.氯化铜和硝酸钠
24.有甲、乙、丙、丁四种金属,把甲、丙浸入稀硫酸中,用导线连接时丙为负极;把乙、丁分别浸入稀硫酸中,丁产生气泡的速率更大;把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出;把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出。这四种金属的活动性由强到弱的顺序是
A.甲>乙>丙>丁 B.丙>丁>乙>甲 C.丙>丁>甲>乙 D.丁>乙>甲>丙
25.实验室制取乙酸乙酯,除试管、导气管、胶头滴管外,还一定需要的玻璃仪器( )
A.烧杯 B.酒精灯 C.量筒 D.铁架台
26.下列说法正确的是
A.无论怎样控制反应条件,2molSO2与1molO2反应都不会生成2molSO3
B.任何化学反应中的反应物都能全部转化成生成物
C.化学反应的限度决定于反应物的性质,与外界的条件无关
D.可逆反应中,使用催化剂只能增大正反应的化学反应速率
27.利用下列物质冶炼金属时,需要加入还原剂的是 ( )
A.HgO B.Al2O3 C.Fe2O3 D.NaCl
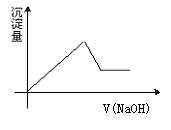 28.向一无色透明的溶液中滴加氢氧化钠溶液时有沉淀生成,且所得沉淀量与所加氢氧化钠溶液体积的关系如图所示,则原溶液可能是 ( )
28.向一无色透明的溶液中滴加氢氧化钠溶液时有沉淀生成,且所得沉淀量与所加氢氧化钠溶液体积的关系如图所示,则原溶液可能是 ( )
A.Al2(SO4)3溶液
B.AlCl3与MgCl2的混合溶液
C.AlCl3和CuSO4的混合溶液
D.MgCl2与NaCl的混合溶液
29.下列说法正确的是 ( )
A.能和新制的氢氧化铜反应的物质一定含有葡萄糖
B.遇碘酒变蓝的物质一定含有淀粉
C.油脂不能使溴水褪色
D.油脂的水解产物中一定有高级脂肪酸
30.不能提高镁与水反应速率的方法是( )
A. 增大水的量 B. 用镁粉代替镁条
C.加热 D. 加入几滴硫酸铜溶液
| X | Y | |
| Z |
二、选择题(本题包括5小题,每小题3分,共15分。每小题只有一个选项符合题意)
31、X、Y、Z三种短周期非金属元素在元素周期表中的位置如右图所示:
下列说法正确的是
A.原子的半径:Y大于Z B.氢化物的稳定性:X高于Y
C.高价氧化物水化物的酸性:X大于Y D.原子序数:Z=Y+7
| 32、过滤后的食盐水仍含有少量可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤 。正确的操作顺序是 ( ) |
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
33.某有机物结构简式为![]() 它不可能具有的性质是
(
)
它不可能具有的性质是
(
)
A.在一定条件下发生加成反应 B.能水解
C.能使酸性高锰酸钾溶液褪色 D.能与Na2CO3溶液反应
34.已知MgO、MgCl2的熔点分别为2800℃、604℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁,正确的方法是 ( )
A. 海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B. 海水![]() MgCl2溶液
MgCl2溶液![]() MgCl2熔融
MgCl2熔融![]() Mg
Mg
C. 海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液 ![]() MgCl2熔融
MgCl2熔融![]() Mg
Mg
35.某混合气体中可能含有Cl2 、O2 、SO2 、NO 、NO2 中的两种或多种气体。现将此无色混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
A.肯定有SO2 和NO 、Cl2 B.肯定没有Cl2 、O2和NO2
C.可能有Cl2和O2 D.肯定只有NO
高一化学水平测试
化学(必修)
| 题号 | 一 | 二 | 三 | 四 | 总分 |
|
|
|
|
|
|
|
第II卷(非选择题,共25分)
三、(本题包括3小题,共18分)
36.(6分)X、 Y、 Z三种短周期元素, X原子半径是所有元素中最小的,Y的最外层电子数比次外层多4个电子,Z的化合物进行焰色反应时火焰为黄色;又知Z、Y形成甲、乙两种固体化合物,乙中Z和Y的原子数比为1:1。则:
⑴X、Y、Z分别为:X__ ____、Y__ ____、Z__ ____;
⑵甲、乙化学式分别为______ ____;
⑶Z的原子结构示意图为________________________________。
37.(6分)某研究性学习小组,将锌片加入到盛有20 mL某浓度的硫酸样品的烧杯中。发现锌片的表面有大量无色气泡冒出,同时还异常地嗅到了一股刺激性气味。
【提出问题】该刺激性气体是什么?
【作出假设】请提出一种假设?
。
【实验设计】请设计实验验证你的假设(要求写出所用试剂、操作、现象、结论)
。
![]() 38.(6分)A
38.(6分)A![]() B
B![]() C
C![]() D
D
E
如上图所示,已知A的产量是一个国家石油化工水平的标志,D具有酸性。E是具有香味的不溶于水的液体。
(1) 写出D的官能团名称: C的结构简式:
(2) A→B的化学反应方程式:
反应类型为:
(3)写出B+D→E的化学反应方程式:
反应类型为:
四、(本题包括1小题,共7分)
39.(7分)0.1mol某烃完全燃烧需要消耗0.8mol氧气,生成标况下11.2LCO2 和10.8g 液态水,通过计算求该烃的分子式。写出该烃可能的结构简式。
高一化学必修部分水平参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | D | B | B | A | D | C | B | A | D |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | B | D | B | B | A | C | B | C | C | A |
| 题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| 答案 | D | A | C | B | B | A | C | B | B | A |
| 题号 | 31 | 32 | 33 | 34 | 35 | |||||
| 答案 | D | A | D | D | B |
二、非选择题
36.⑴ H、O、Na (各1分) ⑵ Na2O、Na2O2 (各1分) ⑶ 略 (1分)
37. 答案一:
(1)该刺激性气体可能是Zn片与浓H2SO4反应生成的SO2气体。(2分)
(2)在已检查过气密性的气体简易装置(1分)中分别加入适量的Zn片与H2SO4样品,将生成的气体通入品红溶液中(1分)。如果红色的品红溶液褪色(1分),则证明该气体是SO2。(1分)
答案二:
(1)该刺激性气体可能是Zn片中的杂质与稀H2SO4反应生成的H2S气体。(2分)
(2)在已检查过气密性的气体简易装置(1分)中分别加入适量的Zn片与H2SO4样品,将生成的气体通入硫酸铜溶液中(1分)。如果生成黑色沉淀(1分),则证明该气体是H2S。(1分)
答案三:
(1)该刺激性气体可能是H2SO4样品混有的盐酸挥发出HCl气体。 (2分)
(2)在已检查过气密性的气体简易装置(1分)中分别加入适量的Zn片与H2SO4样品,将生成的气体分别通入品红和硝酸银溶液中(1分)。如果品红不褪色且生成白色沉淀(1分),则证明该气体是HCl。(1分)
![]() 38. (1)羧基 CH3CHO
38. (1)羧基 CH3CHO
(2)CH2=CH2+H2O ![]() CH3CH2OH 加成反应
CH3CH2OH 加成反应
(3)CH3COOH+HO-C2H5 ![]() CH3COOC2H5+H2O 取代反应
CH3COOC2H5+H2O 取代反应
39.设此有机物的化学式为CXHY
CXHY+(x+![]() )O2
)O2 ![]() xCO2 +
xCO2 + ![]() H2O
H2O
1 22.4x L 9y
0.1
11.2L
10.8![]()
则x=5 ,
则y=12,则化学式为:C5H112
结构简式:CH3CH2 CH2 CH2 CH3 CH3CH(CH3)CH2CH3 CH3C(CH3)3